Мертвая или живая вакцина краснухи
Россия – единственная страна в мире, в которой зарегистрированы уже три вакцины от коронавируса. Однако специалисты говорят, что им практически ничего не известно о двух из них – «ЭпиВакКороне» и «КовиВаке», вся информация по разработкам засекречена. «Доктор Питер» выяснил, что их настораживает в препарате, который вот-вот начнут использовать в массовой вакцинации населения.
Напомним, прививать «Спутник V» начали еще в конце 2020 года. В феврале в гражданский оборот поступила вакцина «ЭпиВакКорона» новосибирского научного центра «Вектор» Роспотребнадзора. В середине марта обещают первые дозы «КовиВака» московского центра им. Чумакова.
Как быть обычному человеку, который хочет получить надежную и эффективную вакцину от коронавируса? Как разобраться в обилии самых противоречивых мнений и выводов, которыми заполнены тематические группы «про вакцины» в социальных сетях? Самая обсуждаемая на сегодня вакцина – «ЭпиВакКорона» – стала таковой, благодаря добровольцам, участвующих в клинических испытаниях. Они сами сдают тесты на антитела, анализируют полученные данные с помощью молекулярных биологов. В обсуждении свойств вакцины принимают участие известные ученые. Так что же такое «ЭпиВакКорона» – живая или мертвая вода — попытался выяснить «Доктор Питер».
Вечная проблема российской фармы
Со «Спутником V» ясность, наконец, появилась – после публикации в самом авторитетном медицинском издании «Ланцет» сомнения в ее качестве и эффективности отпали сами собой. Но многие ждут именно «ЭпиВакКорону» и «КовиВак», интуитивно возлагая на эти вакцины большие надежды. Интуитивно потому что, к примеру, о чумаковской вакцине пока неизвестно вообще ничего, кроме противопоказаний и того, что она рекомендована людям от 18 до 60 лет. Сейчас идет вторая фаза клинических испытаний (третья фаза – в марте и в ней примет участие три тысячи человек). То же самое можно сказать об «ЭпиВакКороне», созданной в центре «Вектор», она поступила в гражданский оборот 18 февраля. О ней известно чуть больше, чем о «КовиВаке», но ясного представления эта информация все равно не дает.
– Главная проблема этой вакцины, как и многих других вакцин в России, это отсутствие публикаций результатов клинических исследований – публикаций в научных журналах или доступ к части регистрационного досье, не содержащей коммерческий тайны, – говорит врач-биофизик Кирилл Скрипкин. -Разработчик «ЭпиВакКороны» (заведующий отделом зоонозных инфекций и гриппа научного центра «Вектор» Роспотребнадзора Александр Рыжиков – Прим. ред.) ещё 27 ноября 2020 года сообщил в интервью, что публикация подготовлена. Но её до сих пор нет. При этом «Вектор» умеет публиковаться. К примеру, результаты доклиники по другой антиковидной вакцине (на основе мРНК) уже опубликованы в научном журнале из второго квартиля поScopus (авторитетная база данных, в которой хранятся рецензируемые научные работы).
Сейчас, как сообщает пресс-служба Роспотребнадзора, «Вектор» направил результаты клинических исследований вакцины фазы I—II в зарубежные научные рецензируемые журналы – «их публикация ожидается в ближайшее время». Но окончательные итоги клинических исследований первой и второй фаз станут известны только в мае 2021 года – через девять месяцев после вакцинации последнего добровольца. 12 февраля были внесены изменения в клинические испытания «ЭпиВакКороны» – срок окончания I—II стадий клинических испытаний был перенесён с сентября 2020 года на май 2021-го. Тогда жебудут известны результаты исследования о влиянии вакцины на внутриутробное развитие плода и репродуктивные функции.
– Меня как сотрудника фармотрасли и гражданина беспокоит, что наши власти регистрируют лекарственные средства вообще без открытых публикаций и прочего информирования граждан, – говорит профессор Сколковского института науки и технологий (Сколтеха) Дмитрий Кулиш. – Причём эта проблема существует давно и с ней связаны все фуфломициновые скандалы. Однако необходимость выбора вакцин потребителем заострила проблему. Дайте хоть какую-то информацию. «ЭпиВакКорону» зарегистрировали без единой публикации и отчёта, то же самое с вакциной Центра имени Чумакова. В просвещенный 21-й век неприлично ничего не публиковать. Я бы очень хотел, чтобы в России приняли, наконец, закон, заставляющий публиковаться людей, регистрирующих лекарственные средства.
Безопасные пептиды
«ЭпиВакКорона» создана на основе трех синтетических пептидов SARS-CoV-2. Пептиды — это короткие фрагменты белков, на которые формируется иммунный ответ организма. По сути, у «Вектора» в вакцину входит всего три маленьких пептида из всего большого S-белка. По словам заведующего отделом зоонозных инфекций и гриппа научного центра «Вектор» Роспотребнадзора Александра Рыжикова, пептидную платформу для вакцин центр «Вектор» разрабатывает больше 20 лет, за это время она уже использовалась при создании вакцины от лихорадки Эбола. В вакцине нет ни живого вируса, ни элементов вирусного генома, поэтому, как заявляют разработчики, вакцина абсолютно безопасна для человека, не вызывает никаких побочных эффектов и обладает фантастической 100-процентной иммунологической защитой (для сравнения, эффективность «Спутника V» составляет 91,6 %).
Но, как оказалось, в новосибирскую вакцину некоторые ученые не верят изначально, считают, что в мире отсутствуют рабочие вакцины на подобной — пептидной- платформе. К примеру, один известный российский вирусолог считает, что новосибирская вакцина «работать не может, в принципе» именно из-за того, что она пептидная.
– Это какая-то ошибка, – говорит профессор Сколтеха Дмитрий Кулиш. – Уже много лет в мире известны десятки успешных пептидных вакцин. Последний патент «Вектора» весьма похож на аналогичную тайваньскую вакцину (в феврале 2020 года тайваньские ученые начали разработку синтетической пептидной вакцины против коронавируса, тестирование на людях началось осенью, – Прим. ред). Это значит, что в мире есть как минимум один серьезный аналог «ЭпиВакКороны». И когда критики вакцины заявляют, что «эпиваковские» пептиды гарантированно бессмысленны и там защиты быть не может, они, мягко говоря, лукавят. Главная тема, которую сейчас обсуждают в связи с новосибирской вакциной, это то, что уважаемые китайские коллеги, которые провели очень качественное исследование иммуногенности пептидов не смогли доказать, что те пептиды, которые выбрал «Вектор», достаточно иммуногенны. Но при этом, они не доказали, что выбранные пептиды не иммуногенны. Поэтому когда некоторые ученые вопиют, что вакцина, якобы, пустышка, которой обманывают россиян, они поступают неэтично и непрофессионально. Давайте все-таки дождёмся результатов клинических испытаний и потом будем делать выводы.
Читайте также: Петербургский инфекционист: Как разные вакцины от COVID-19 заставляют работать иммунитет
Антитела «неизвестно к чему»
Антитела после вакцинации – ключевой показатель эффективности вакцины, и тут участников клинических испытаний новосибирской вакцины ждало разочарование.
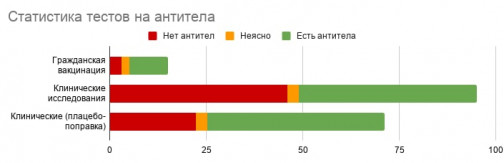
«У меня вся семья, четыре человека, привились «ЭпиВакКороной». Вторую дозу вкололи 18 января, 6 февраля сдали кровь на антитела – результат отрицательный. В медицинском центре нам посоветовали связаться с «Вектором». Позвонили туда, оказалось, что тесты на выявления антител от «ЭпиВакКороны» есть только у «Вектора», они пока коммерчески недоступны», – рассказывает один из привившихся. И похожих историй, если почитать чат в «Телеграме», много. Разработчики вакцины предоставили участникам клинических испытаний свою тест-систему, но и она показала низкий уровень антител. Результаты этих тестов были опубликованы в группе.

– Антитела обнаружены, защищают ли они — нам пока неизвестно, – говорит Андрей Криницкий, создатель сообщества в «Телеграме». При этом добровольцы рассказывают о том, что уже есть заболевшие ковидом после вакцины (12 человек), причем из группы участников клинических испытаний, получивших именно прививку, а не плацебо.
По мнению молекулярного биолога (свое имя он просил не называть), который принимал участие в клинических испытаниях вакцины как доброволец, антитела у части вакцинированных получены «неизвестно к чему, так как тест-система «Вектора» определяет антитела, которые с коронавирусными антигенами могут быть никак не связаны».
– Наличие антител (гуморальный иммунитет) – это важный, но не единственный момент, – говорит врач-биофизик Кирилл Скрипкин. – Просто оценивать его легче всего. Есть клеточный иммунитет (к которому тоже есть вопросы по этой вакцине). Есть антитело-зависимая клеточная цитотоксичность. По поводу антител у добровольцев: есть мнение, что эти антитела к технической His-tag метке в составе вакцины, которая не была убрана из неё для удешевления процесса производства.
Как объясняет эксперт, «ЭпиВакКорона» – это три пептида спайк-белка, которые конъюгированы на белке-носителе. Белок-носитель – это химерный (состоящий из частей двух разных организмов) белок. Одна часть – это N-белок (нуклеопротеин) коронавируса. А другая часть – это pMBP белок кишечной палочки. Обе части соединены вместе технической меткой His-tag. Нуклеопротеин коронавируса для вакцины производится в кишечной палочке, а для его последующей очистки нужна эта метка. В идеале её нужно было удалить после очистки, так как она потенциально может вызывать выработку антител на себя, но для удешевления процесса производства вакцины разработчики решили не усложнять, объясняя это тем, что белок-носитель все равно экранируется пептидами спайк-белка.
– Но это слова, никто это мнение ни опроверг, ни подтвердил, – уточняет Кирилл Скрипкин. – С другой стороны есть положительные результаты протективного (защитного) действия вакцины в нагрузочных испытаниях на хомяках и хорьках, которые были опубликованы в патентах.
Известно, что для доклинических исследований «Вектор» использовал около полутора тысяч лабораторных животных — мышей, крыс, морских свинок, кроликов, хомяков, хорьков и приматов. Испытания на них показали, что вакцина защищает от развития пневмонии, создает высокий уровень иммунного ответа, она также безвредна для них и легко переносится. Но достаточно ли этого, чтобы сделать вывод о 100-процентной эффективности вакцины для человека? По словам Кирилла Скрипкина,результаты исследования протективных свойств вакцины опубликованы в патентах только для хомяков и хорьков. У этих животных после вакцинации все равно поражались легкие, но степень поражения была меньше, чем в контрольной группе. Элиминация (выведение из организма) вируса из дыхательных путей по результатам ПЦР наступала раньше.
Читайте также: «Плацебники» «Вектора» обратились в Минздрав – хотят привиться до окончания клинических исследований
Цель — защитить людей от ковида
Добровольцы 3-й фазы клинических испытаний, не обнаружив у себя антитела после вакцинации, отправляли открытое письмо в Роспотребнадзор, Минздрав и другие ведомства. Добились в итоге личной встречи с разработчиками вакцины, протокол беседы после недельного согласования в Роспотребнадзоре был выложен в сеть. Неподготовленному человеку читать его сложно из-за обилия профессиональных терминов. Профессор Сколтеха Дмитрий Кулиш переводит для читателей «Доктор Питера» часть беседы добровольцев с разработчиками вакцины на «человеческий язык»: «Почему мы не видим антительный ответ, – спрашивают добровольцы?» «Вектор» отвечает: «Потому что наши пептиды вызывают конкретный и четкий ответ, который защитит вас от вируса, но этот ответ не виден на стандартных ИФА-панелях (иммуноферментный анализ). Единственный способ увидеть эти антитела – это наша собственная ИФА-панель, но даже здесь они видны слабо». Люди спрашивают: «Почему вы не могли сделать ИФА-панель, на которой они видны сильно?» «Вектор» отвечает, что у них не было цели делать тонкую диагностику, главная цель — защитить людей от ковида, и вот сейчас, когда дойдут до конца клинические испытания, «мы все торжественно опубликуем, и тогда вы увидите, что все работает».
– Если «Вектор» опубликуется в хорошем журнале, и ему хватит силы доказать, что вакцина работает, то все остальное окажется неважным, – говорит профессор Кулиш. – Потому что, действительно, стандартные ИФА-панели могут не видеть «эпиваковские» антитела, а пептиды могут быть получены собственными «векторовскими» технологиями, а не китайскими. Но сейчас нам просто нечего обсуждать, потому что состав вакцины «ЭпиВакКорона» полностью засекречен.
Обновленная версия патента
К публичному обсуждению свойств новосибирской вакцины вслед за добровольцами подключились ученые. Бывшие и нынешние сотрудники института молекулярной биологии, в том числе экс-сотрудники «Вектора» – активно комментируют, многие под псевдонимами, заявленную 100-процентную эффективность «ЭпиВакКорону» в социальных сетях. Оценка в основном критическая.
Молекулярный биолог Ольга Матвеева одна из первых, кто обратил внимание на качество защитных свойств вакцины. «Когда вакцина начала выпускаться и презентоваться, о ней говорили как о дающей меньше побочных эффектов, и о том, что она будет безопасна для тех, кому противопоказан «Спутник». Не исключено, что «ЭпиВакКорона» действительно не дает побочных эффектов, но все-таки главное в вакцине — это ее способность защитить от заболевания. Про это свойство «ЭпиВакКороны» для людей нам ничего не известно. Вместо заявленной 100-процентной эффективности мы пока что имеем большую научную непрозрачность», – написала она в своей статье в научном журнале «Троицкий вариант».
– Основныхпретензий к вакцине две, – рассказала «Доктору Питеру» Ольга Матвеева. – Первая — то, что вакцину выпустили в гражданский оборот, не завершив I—II фазы клинических исследований. Это беспрецедентная история. Вторая — нет нейтрализующих антител у вакцинированных. У тех, у кого антитела все-таки появились, очень маленький титр и мы не знаем, являются ли эти антитела защитными.
На днях стало известно, что разработчики «ЭпиВакКороны» отошли от композиций, перечисленных в изначальном патенте. И сейчас, говорят эксперты, видна определенная аналогия выбранных пептидов с пептидами из тайваньской вакцины.
– Только 20 февраля 2021 года стал известен состав пептидов, вошедших в «ЭпиВакКорону» – и то, исключительно благодаря публикации патента , – рассказывает врач-биофизик Кирилл Скрипкин. – Нужно понимать, что «Вектор», аналитически (то есть с применением специальных программ, использующих математический анализ и компьютерное моделирование – in silico, и предсказавших пептиды, которые будут обладать максимальной иммуногенностью) выбирал пептиды для вакцины в условиях дефицита времени. А мои коллеги оценивают выбранные пептиды «Вектора» не по аналитическим, а по экспериментальным работам (это методы in vitro, то есть «в пробирке» – когда нарезают все возможные пептиды спайк белка с определенным шагом и смотрят, какой из них лучше всех реагирует с антителами переболевших). Причём результаты некоторые этих экспериментальных работ противоречат друг другу. Есть вероятность, что аналитически выбранные пептиды «Вектора» не совсем удачны, проверить это можно в ходе клинического исследования, результаты которого находятся в регистрационном досье, доступ к которому ограничен. Замкнутый круг. И ещё один момент: существует мнение, что «Вектор» выбирал свои пептиды наугад. Это не так. В результатах других аналитических работ по выбору пептидов из сторонних лабораторий есть совпадения с пептидами «Вектора».
По словам Кирилла Скрипкина, определенно сказать, какова эффективность новосибирской вакцины можно только после того, как будут опубликованы результаты клинических исследований.
Читайте также: Инфекционист Боткинской больницы объяснил, почему кому-то не нужна прививка от коронавируса, а нужен тест на антитела
– Или после открытия доступа к регистрационному досье, что прописано в федеральном законе, – говорит он. – Американское FDA не скрывает данные регистрационных досье, при этом никто не умер из-за потери своей коммерческой тайны.
Не исключено, допускают эксперты «Доктора Питера», что позиция скептиков резко изменится после итоговых научных публикаций. Еще свеж пример со «Спутником V», который тоже сильно критиковали за «непрозрачность» клинических исследований, а после публикации в «Ланцете» вакцина стала гордостью России.
– В любом случае, если по результатам клинических испытаний «ЭпиВакКорона» окажется не эффективной для первичной вакцинации, это совершенно не повод ставить на ней крест, – считает Кирилл Скрипкин. – С большой долей вероятности она может быть полезна для ревакцинации после «Спутника V» или для стимуляции иммунитета после перенесённого заболевания.
Тем временем, гражданская вакцинация «ЭпиВакКороной», которая началась еще в середине декабре 2020 года, когда первую партию вакцины получила Новосибирская область (как сообщалось, для врачей, преподавателей и работников бюджетной сферы), только набирает обороты. Сейчас, по информации «Доктора Питера», новосибирской вакциной прививаются сотрудники Роспотребнадзора и Минздрава, члены Госдумы, вакцина также есть в клинике Управделами президента. Директор государственного научного центра вирусологии и биотехнологии «Вектор» Ринат Максютов в эфире телеканала «Россия 1» заявил, что центром получено более 45 обращений из других стран о проведении исследований и начале производства вакцины «ЭпиВакКорона».
Профессор СПбГУ: Прививка от коронавируса для переболевших COVID-19 — большой риск
Ирина Фигурина
© Доктор Питер
Источник
МНН: Вакцина против краснухи
Производитель: Serum Institute of India Ltd
Анатомо-терапевтическо-химическая классификация: Rubella, live attenuated
Номер регистрации в РК:
№ РК-БП-5№013465
Информация о регистрации в РК:
09.09.2014 – 09.09.2019
Торговое название
Вакцина против краснухи живая аттенуированная лиофилизированная
Международное непатентованное название
Нет
Лекарственная форма
Лиофилизат для приготовления раствора для подкожного введения
10 доз во флаконе в комплекте с растворителем 5мл в ампуле
Состав
Одна доза (0,5 мл) содержит
активное вещество – вирус краснухи не менее 1000 ТЦД50,
вспомогательные вещества: частично гидролизованный желатин, сорбитол, гистидин, L-аланин, трицин , L-аргинина гидрохлорид,
лактабумина гидролизат.
Растворитель – вода для инъекций 0,5 мл.
Описание
Однородная, пористая масса желтовато-белого цвета, гигроскопична. После растворения прозрачная бесцветная или светло-желтого цвета жидкость.
Растворитель: прозрачная бесцветная жидкость.
Фармакотерапевтическая группа
Противовирусные вакцины. Вакцины против краснухи. Вирус краснухи – живой ослабленный.
Код АТХ J07BJ01
Фармакологические свойства
Фармакокинетика
Для вакцин не требуется оценка фармакокинетических свойств.
Фармакодинамика
Вакцина против краснухи живая аттенуированная лиофилизированная приготовлена из аттенуированного штамма випуса краснухи Wistar RA 27/3. Вирус выращивается на человеческих диплоидных клетках (ЧДК). Вакцина стимулирует активный иммунитет против вируса краснухи путем индуцирования производства антител IgG к краснухе, который развивается в течение 15 дней после вакцинации и сохраняется не менее 16 лет. Серо-конверсия наблюдается у 95-100% привитых пациентов. При проведении серологического исследования результат считается положительным при разведении не менее 1/20 (в РТГА): в этом случае пациент расценивается как обладающий специфическим иммунитетом и вакцинации для него не требуется. При разведении менее 1/20 результат считается отрицательным.
Вакцина соответствует требованиям Всемирной Организации здравоохранения.
Показания к применению
Профилактика краснухи
Первичная вакцинация
– активная иммунизация против краснухи детей в возрасте 12 месяцев и старше
– вакцинация юношей и мужчин в целях профилактики и контроля распространения краснухи в локализованных коллективах
– вакцинация восприимчивых девочек-подростков и небеременных женщин детородного возраста, а также женщин в послеродовом периоде
Вакцинация половозрелых девочек и женщин, не имеющих иммунитета к краснухе, обеспечивает индивидуальную защиту от заражения вирусом краснухи во время беременности, что в свою очередь предупреждает инфицирование плода и развитие врожденной краснухи.
Ревакцинация
– дети, впервые иммунизированные в возрасте до 12 месяцев, а также дети, иммунизированные согласно календарю в возрасте 12 месяцев и старше, в случаях, если первичная вакцинация была не эффективна (защитный титр менее 1/20)
Данную вакцину рекомендуется использовать у детей в соответствии с Национальным Календарём прививок и для проведения экстренной иммунизации у взрослых лиц до 30 лет по эпидпоказаниям (Рекомендации ВОЗ).
Способ применения и дозы
Вакцина должна быть разведена только прилагаемым растворителем (стерильная вода для инъекций) с использованием стерильного шприца. Сухая вакцина легко растворяется при осторожном встряхивании. Однократная доза препарата (0,5 мл) вводится только глубоко подкожно! в переднебоковую верхнюю часть бедра новорожденным и в плечо детям старшего возраста. Каждую дозу из 10 доз во флаконе следует набирать стерильной иглой и шприцем при строгом соблюдении правил асептики и антисептики во избежание загрязнения содержимого флакона. Многодозовая вакцина должна быть использована сразу же после разведения. Если растворенная вакцина до конца была не использована, то закрытый флакон хранят в защищенном от света месте при температуре от 2°С до 8°С не более 6 часов, затем неиспользованную ее часть необходимо уничтожить.
Прилагаемый растворитель специально изготовлен для данной вакцины. Допускается использование только прилагаемого растворителя. Не используйте растворители для вакцин других типов и вакцин против краснухи других производителей. Использование несоответствующих растворителей может привести к изменению свойств вакцины и тяжелым реакциям у реципиентов.
Перед тем, как вводить препарат, необходимо произвести визуальный осмотр растворителя и разведенной вакцины, чтобы определить наличие хлопьев и/или отклонений в физических характеристиках. В случае неудовлетворительных результатов визуального осмотра растворитель или разведенную вакцину использовать нельзя.
Побочные действия
Определение частоты побочных эффектов: очень частые(≥1/10, более 10%); частые (≥1/100, но <1/10, более 1%, но менее 10%); нечастые (≥1/1,000, но <1/100, более 0,1%, но менее 1%); редкие (≥1/10,000, но <1/1,000, более 0,01%, но менее 0,1%); очень редкие (<1/10,000, менее 0,01%), включая единичные сообщения
Очень часто
– умеренная болезненность в месте инъекции в течение 24 часов после вакцинации
– умеренное повышение температуры
– артралгии и артрит у девочек-подростков и взрослых женщин, которые длятся от нескольких дней до 2 недель
Часто
– сыпь
Редко
– лимфаденопатия
– миалгии и парестезии
Очень редко
– тромбоцитопения (менее 1:30000)
– анафилактический шок
Противопоказания
– гиперчувствительность к компонентам вакцины (на неомицин и яичный белок)
– лихорадочное состояние
– острые инфекционные заболевания
– беременность и период лактации
– лейкемия
– выраженная анемия и другие тяжелые заболевания крови, включая злокачественные
– тяжелые нарушения функций почек
– заболевания сердца в стадии декомпенсации
– злокачественные новообразования
– иммунодефицитные состяния с поражением клеточного иммунитета
– предшествующее вакцинации применение кортикостероидов, имму-нодепресантов или лучевая терапия
– предшествующее вакцинации применение гаммаглобулинов или трансфузия крови
– анафилактические или анафилактоидные реакции на введение вакцины в анамнезе
Лекарственное взаимодействие
Возможно одновременное (в один день) назначение вакцины против краснухи с вакцинами против коклюша, дифтерии, столбняка; дифтерии и столбняка; столбнячным анатоксином; полиовакциной (живой и инактивированной); вакциной против Haemophilus influenzae типа b; вакциной против вируса гепатита В без риска осложнений или снижения эффективности, вакциной против желтой лихорадки. При этом вакцины вводят в разные участки тела разными шприцами.
Вакцину против краснухи не следует назначать раньше чем через 3 месяца после введения иммуноглобулинов и содержащих их продуктов крови (цельной крови, плазмы), поскольку при этом может произойти инактивация вакцины. По этой же причине иммуноглобулины не следует назначать в течение 2 недель после вакцинации.
У лиц, получающих кортикостероиды и другие иммунодепрессанты или радиотерапию, может наблюдаться недостаточный иммунный ответ.
Особые указания
ВНИМАНИЕ!
1. Вакцина должна вводиться глубоко подкожно. Поскольку любой компонент вакцины может вызвать развитие анафилактической реакции, наготове должен быть раствор адреналина (1:1000) для внутрикожной или внутримышечной инъекции. Для лечения тяжелой анафилаксии первоначальная доза адреналина составляет 0,1-0,5 мг (0,1-0,5 мл инъекции 1:1000) и вводится внутримышечно или подкожно. Разовая доза не должна превышать 1 мг (1 мл). Для младенцев и детей рекомендованная доза адреналина составляет 0,01 мг/кг (0,01 мл/кг инъекции 1:1000). Разовая педиатрическая доза не должна превышать 0,5 мг (0,5 мл). Это поможет эффективно устранить анафилактический шок / анафилактическую реакцию. Адреналин следует вводить при первом же подозрении на развитие анафилактического шока.
2. Лицо, получившее прививку, должно находиться под наблюдением медицинского персонала в течение 30 минут после введения вакцины, что необходимо для своевременного распознавания аллергических реакций немедленного типа. В пункте вакцинации должны быть в наличии преднизолон и/или другие антигистаминные препараты для инъекций, а также другие средства: кислородный дыхательный аппарат и т.д.
ВИЧ-инфекция
Живая вакцина против краснухи может назначаться детям с ВИЧ – инфекцией без клинических проявлений.
Беременность и период лактации
Запрещается вводить вакцину во время беременности!
Исследований по влиянию вакцины на лактацию не проводилось.
Вакцинированным женщинам не рекомендуется зачатие в течение одного месяца после вакцинации.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Нет никаких доказательств того, что вакцина против краснухи влияет на способность управлять транспортными средствами и движущимися механизмами.
Передозировка
Случаев передозировки отмечено не было.
Форма выпуска и упаковка
Вакцина. По 10 доз вакцины в стеклянных флаконах коричневого цвета. По 50 флаконов с инструкцией по медицинскому применению на государственном и русском языках в картонной коробке.
Растворитель. По 5 мл в ампуле из бесцветного прозрачного стекла 1 гидролитической группы.
По 50 ампул ампул с инструкцией по медицинскому применению на государственном и русском языках в картонной коробке или по 10 ампул в контурную ячейковую упаковку (блистер) из композиционного материала полиамид/алюминий ПВХ и фольги алюминиевой печатно-лакированной;
по 5 контурных ячейковых упаковок (блистеров) с инструкцией по медицинскому применению на государственном и русском языках в картонной коробке.
Условия хранения
Вакцина. Хранить в в защищенном от света месте при температуре от
2 С до 8 С. Не замораживать.
Растворитель. Хранить при температуре от 5 С до 30С.
Не замораживать.
Восстановленная вакцина может храниться в защищенном от света месте при температуре от 2 С до 8 С не более 6 часов.
Хранить в недоступном для детей месте!
Срок хранения
Вакцина – 2 года
Растворитель – 5 лет
Не использовать после истечения срока годности.
Условия отпуска из аптек
По рецепту (для лечебно-профилактических учреждений)
Производитель
Serum Institute of India Ltd
212/2, Хадапсар, Пуне 411 028, Индия
Владелец регистрационного удостоверения
Serum Institute of India Ltd
212/2, Хадапсар, Пуне 411 028, Индия
Адрес организации принимающей претензии от потребителя по качеству препарата на территории Республики Казахстан
ТОО «Альбедо», Республика Казахстан, 050035, г.Алматы, 10 мкр-он,
д. 32, тел. +7 727 303 21 00, +7 727 303 06, факс +7 727 303 21 03,
e-mail: albedo@vaccina.kz
| 567236891477976647_ru.doc | 73.5 кб |
| 116369111477977787_kz.doc | 79 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Источник
