Клинические рекомендации по лечению кандидоза беременных

В настоящее время частота гнойно–воспалительных заболеваний в акушерстве не имеет явной тенденции к снижению. Во многих странах мира, в том числе и в России, отмечен рост вагинальных инфекций, которые прочно занимают ведущее место в структуре акушерско–гинекологической заболеваемости [1, 2].
Внедрение современных технологий в клиническую микробиологию позволило расширить исследования и показать, что отрицательное воздействие факторов внешней среды на микрофлору макроорганизма ведет к разнообразной патологии как воспалительного, так и невоспалительного генеза. Несмотря на значительные успехи, достигнутые в диагностике, терапии и профилактике дисбактериозов влагалища, их частота не имеет отчетливой тенденции к снижению. Последнее связано также с ростом иммунодефицитных состояний на фоне ухудшения экологической обстановки, неправильного питания, частых стрессов, бесконтрольного применения лекарственных средств, в первую очередь, антибиотиков. Чаще всего половая инфекция бывает обусловлена несколькими патогенными факторами – вирусами, микробами, грибами, простейшими, которые вызывают похожие по клиническому течению, но различные по патогенезу и методам лечения заболевания.
Особо важное значение вагинальные инфекции приобретают в акушерской практике, так как являются частой причиной развития воспалительных осложнений во время беременности, в родах и послеродовом периоде. К осложнениям гестационного периода и родов, связанным с различными нарушениями микроценоза влагалища, относят угрозу прерывания, самопроизвольные выкидыши, преждевременные роды, хориоамнионит, несвоевременное излитие околоплодных вод, рождение детей с малой массой тела, хронической гипоксией и/или признаками внутриутробной инфекции, возникновение раневой инфекции родовых путей, эндометрита в послеродовом периоде.
Нарушение микроценоза влагалища наиболее часто связано с кандидозной инфекцией. По данным литературы, 75% женщин репродуктивного возраста переносят, по крайней мере, один эпизод вагинального кандидоза [3]. В настоящее время известно 196 видов грибов рода Candida. Из них со слизистых оболочек человека выделяют более 27 видов. По сводным данным, Candida albicans обнаруживают в кишечнике у 20–50% здоровых людей, на слизистой оболочке полости рта – у 20–60%, во влагалище – у 10–17% небеременных женщин. Вагинальный кандидоз у беременных встречается в среднем в 30–40% случаев, а перед родами – до 44,4%.
75% женщин репродуктивного возраста переносят, по крайней мере, один эпизод вагинального кандидоза.
Необходимо отметить, что кандидоз мочеполовых органов в 2–3 раза чаще встречается при беременности, чем у небеременных женщин. Столь высокая частота возникновения кандидоза влагалища в период гестации обусловлена рядом факторов: изменениями гормонального баланса; накоплением гликогена в эпителиальных клетках влагалища; иммуносупрессорным действием высокого уровня прогестерона и присутствием в сыворотке крови фактора иммуносупрессии, связанного с глобулинами. Установлена прямая связь между сроком гестации и частотой возникновения вагинального кандидоза.
Основная роль в возникновении вагинального кандидоза принадлежит грибам рода Candida albicans, выделяемым в 95% случаев. Для вагинального кандидоза во время беременности характерны бессимптомное течение и частые рецидивы. В связи с увеличением числа факторов риска и широким распространением кандидозной инфекции, появлением новых данных о патогенезе на фоне иммунодефицитных состояний, вопросы профилактики и лечения кандидоза в настоящее время представляют весьма сложную проблему [1, 4, 5]. Особое значение эта проблема приобретает в период гестации из–за высокого риска поражения плода. Беременные и родильницы с вагинальным кандидозом могут быть источником как внутриутробного, так и постнатального инфицирования новорожденных. За последние 20 лет частота кандидоза среди доношенных новорожденных возросла с 1,9% до 15,6%.
Важным представляется знание патогенеза данной инфекции. В развитии кандидоза различают следующие этапы: прикрепление (адгезию) грибов к поверхности слизистой оболочки с ее колонизацией, внедрение (инвазию) в эпителий, преодоление эпителиального барьера слизистой оболочки, попадание в соединительную ткань собственной пластинки, преодоление тканевых и клеточных защитных механизмов, проникновение в сосуды, гематогенная диссеминация с поражением различных органов и систем.
При вагинальном кандидозе инфекционный процесс чаще всего локализуется в поверхностных слоях эпителия влагалища. На этом уровне инфекция может персистировать длительное время ввиду возникновения динамического равновесия между грибами, которые не могут проникнуть в более глубокие слои слизистой оболочки, и макроорганизмом, сдерживающим их, но не способным полностью элиминировать возбудитель. Нарушение этого равновесия приводит либо к обострению заболевания, либо к ремиссии или выздоровлению.
В зависимости от состояния вагинального микроценоза выделяют 3 формы Candida–инфекции влагалища:
1. Бессимптомное кандидоносительство, при котором отсутствуют клинические проявления заболевания, дрожжеподобные грибы выявляются в низком титре (менее 104 КОЕ/мл), а в составе микробных ассоциантов вагинального микроценоза абсолютно доминируют лактобациллы в умеренно большом количестве.
2. Истинный кандидоз, при котором грибы выступают в роли моновозбудителя, вызывая клинически выраженную картину вагинального кандидоза. При этом в вагинальном микроценозе в высоком титре присутствуют грибы Candida (более 104 КОЕ/мл) наряду с высоким титром лактобацилл (более 106 КОЕ/мл) при отсутствии диагностически значимых титров других условно–патогенных микроорганизмов.
3. Сочетание вагинального кандидоза и бактериального вагиноза, при котором дрожжеподобные грибы участвуют в полимикробных ассоциациях, как возбудители заболевания. В этих случаях дрожжеподобные грибы (чаще в высоком титре) обнаруживают на фоне большого количества (более 109 КОЕ/мл) облигатных анаэробных бактерий и гарднерелл при резком снижении концентрации или отсутствии лактобацилл.
Клиническая картина вагинального кандидоза обычно характеризуется следующими симптомами:
• обильными или умеренными творожистыми выделениями из половых путей;
• зудом, жжением, раздражением в области наружных половых органов;
• усилением зуда во время сна или после водных процедур и полового акта;
• неприятным запахом, усиливающимся после половых контактов.
В настоящее время принято различать 3 клинические формы генитального кандидоза:
1. Кандидоносительство
2. Острый урогенитальный кандидоз
3. Хронический (рецидивирующий) урогенитальный кандидоз.
Одной из основных особенностей течения генитального кандидоза является нередкое сочетание кандида–инфекции с бактериальной условно–патогенной флорой, обладающей высокой ферментативной и литической активностью, что создает благоприятные условия для внедрения грибов в ткани.
Диагностика вагинального кандидоза должна быть клинико–микробиологической, а среди лабораторных методов приоритет должен быть отдан посеву вагинального отделяемого. Этот метод позволяет установить этиологию заболевания, видовую принадлежность возбудителя и дать его количественную оценку. Культуральное исследование является методом выбора и при контроле эффективности лечения. Параллельно проводимая микроскопия вагинального мазка, окрашенного по Граму, позволяет дать оценку сопутствующей грибам микрофлоры (облигатные анаэробы или лактобациллы), от которой должен зависеть выбор рациональной этиотропной терапии.
Лечение вагинального кандидоза
Препараты, применяемые у беременных для лечения вагинального кандидоза, должны отвечать следующим требованиям: отсутствие токсичности для плода и для матери, высокая эффективность, хорошая переносимость, минимальная частота возникновения резистентности у возбудителей и т.д. Интравагинальное применение антимикотиков следует признать предпочтительным из–за очень низкой системной абсорбции препаратов, что сводит к минимуму возможность нежелательных эффектов [1, 4]. Кроме того, быстрее наступает уменьшение клинической симптоматики и выздоровление. Существует множество препаратов и схем лечения вагинального кандидоза во время беременности. Однако пока нет оптимального препарата, который бы отвечал всем требованиям и имел бы стопроцентную эффективность.
Препараты для лечения вагинального кандидоза подразделяют на следующие группы:
• антибиотики (нистатин, леворин, пимафуцин, амфотерицин В);
• имидазолы (клотримазол, кетоконазол, миконазол, гино–певарил);
• триазолы (флуконазол, итраконазол);
• комбинированные препараты (полижинакс, клион Д, пимафукорт, макмирор комплекс);
• препараты разных групп (дафнеджин, йодат поливинилпирролидон, гризеофульвин, флуцитозин, нитрофунгин).
При лечении вагинального кандидоза эффективность клотримазола составляет 70–82%, миконазола – 80%, кетоконазола – 68%, полижинакса – 85,5%, гино–певарила – 86,7%, дафнеджина – 93,5%, флуконазола – 93,3% [1, 3, 4, 5]. Однако использование некоторых противогрибковых препаратов (например, флуконазола) ввиду их возможного тератогенного воздействия в период гестации противопоказано.
В последние годы для лечения вагинального кандидоза при беременности стали широко применять пимафуцин (натамицин), который является противогрибковым полиеновым антибиотиком из группы макролидов, имеющим широкий спектр действия. Он оказывает фунгицидное действие. Натамицин связывает стеролы клеточных мембран, нарушая их целостность и функции, что приводит к гибели микроорганизмов. К натамицину чувствительны большинство дрожжеподобных грибов, особенно Candida albicans, менее чувствительны к данному препарату дерматофиты. Важными характеристиками препарата являются отсутствие резистентных штаммов, а также отсутствие токсичности, что позволяет применять его на любом сроке беременности и в период лактации.
Клинические испытания препарата проводились при лечении большого количества больных, страдающих цервиковагинитами и вульвовагинитами, вызванными простейшими и грибами. Была доказана эффективность пимафуцина, во всех исследованиях отмечался высокий процент полного выздоровления с исчезновением клинических симптомов и нормализацией результатов бактериоскопического и бактериологического анализов.
Применяя пимафуцин для лечения вагинального кандидоза у беременных в течение последних 5 лет, мы подтвердили его высокую эффективность и безопасность. При этом соблюдался принцип индивидуального подхода к каждой беременной с учетом срока гестации, клинической формы заболевания, результатов микробиологического анализа. Пимафуцин назначали после 12 недель гестации, при острой форме ВК – по 1 вагинальной свече (100 мг натамицина) 1 раз на ночь в течение 6 дней, при рецидиве хронической инфекции – в той же дозировке, длительностью 9 дней. Одновременно предупреждали о необходимости лечения супруга (например, 2% крем пимафуцин – местно). Данные опроса пациенток показали, что уже на 2–3 день лечения отмечалось улучшение состояния. После окончания курса терапии у подавляющего большинства (94%) беременных отмечалось улучшение. Клинически оно выражалось в исчезновении выделений, гиперемии и отечности слизистой влагалища, чувства жжения и зуда. В мазках и бактериологическом посеве нити мицелия и дрожжевые клетки обнаружены не были. В мазках из влагалища лейкоцитоз составлял до 8–10 в поле зрения.
Таким образом, пимафуцин является высокоэффективным противогрибковым препаратом для лечения вагинального кандидоза при беременности, не оказывающим отрицательного влияния на состояние плода и новорожденного.
Натамицин –
Пимафуцин (торговое название)
(Yamanouchi Europe)
Литература:
1. Прилепская В.Н., Анкирская А.С., Байрамова Г.Р., Муравьева В.В. Вагинальный кандидоз. // М.: 1997.– 40 с.
2. Mardh P.A. The vaginal ecosystem. // Amer. J. Obstet. Gynecol. – 1991. – Vol. 165, № 4, Рt. 2. – P. 1163–1168.
3. Perry С., Whittinton R., McTavish D. Fluconazole. An update of its antimicrobial activity, phannacokinetic properties and therapeutic use invaginal candidiasis. // Drugs.–1995.– Vol. 49. № 6. – P. 994–1006.
4. Акопян Т.Э. Бактериальный вагиноз и вагинальный кандидоз у беременных (диагностика и лечение): Дисс… канд. мед. наук.– М.– 1996.–141 с.
5. Мирзабалаева А. К. Основные принципы лечения хронического кандидоза гениталий у женщины. // Вестник дерматологии и венерологии.–1994.– № 2.– С. 20–22.
Источник
Статья посвящена эффективности и комплаентности терапии вульвовагинального кандидоза при беременности. Показано, что терапия вульвовагинального кандидоза в период беременности лекарственными средствами с действующим веществом натамицин (Примафунгин) высокоэффективна и не имеет побочных эффектов.

Вульвовагинальный кандидоз (ВВК) – заболевание слизистой влагалища, обусловленное грибковой инфекцией, нередко распространяющееся на слизистую наружных половых органов [1–4].
Около 75% женщин в возрасте до 25 лет имели не менее одного эпизода ВВК в анамнезе, у 40–50% женщин случаются повторные эпизоды заболевания и у 5% женщин – рецидивирующая форма (4 и более эпизода за один год) [4, 5]. При этом у 20–50% женщин в составе нормальной микрофлоры влагалища определяются грибы рода Candida без проявления клинических симптомов [5]. В США ежегодно регистрируется 13 млн случаев вульвовагинальной инфекции, из них большинство вызвано Candida albicans. При этом 5% женщин планеты страдают рецидивирующим ВВК, для которого характерны 3 или более эпизодов обострения инфекции в течение года [6]. В Австрии при пятилетнем клинико-микробиологическом обследовании женщин с вульвовагинальными жалобами в 10 463 образцах дрожжеподобные грибы C. albicans выявлены в 87,9% и C. non-albicans – в 12,1% случаев [7].
Это заболевание встречается у 30–40% беременных, перед родами этот показатель может достигать 45–50%. Столь высокая частота ВВК при беременности обусловлена изменением гормонального баланса, так как повышение уровня эстрогенов и прогестерона увеличивает адгезивные свойства эпителиоцитов влагалища. Кроме этого, гиперэстрогенемия способствует повышенной пролиферации клеток влагалищного эпителия и увеличению содержания в них гликогена – питательной среды для грибов.
А.Н. Стрижаков и соавт. [5] показали, что частота нарушений микробиоценоза родовых путей во время беременности составляет в среднем 40–65%. Предпринятое О.Р. Асцатуровой и А.П. Никоновым скрининговое обследование беременных в III триместре на наличие вульвовагинальной инфекции, включающее 306 женщин, выявило заболевание у 47,1% из них. Среди разных форм преобладали ВВК и бактериальный вагиноз (22,2% и 27,0% соответственно) [8].
Е.И. Боровкова при изучении колонизационной резистентности влагалища у беременных с высоким риском внутриутробной инфекции показала, что в когорте женщин с угрозой раннего прерывания беременности имеет место снижение облигатной микрофлоры и отсутствие бифидобактерий, при этом у каждой пятой из них высеваются грибы рода Candida. Выявлена прямая корреляционная связь между степенью выраженности дисбактериоза влагалища и осложненным течением беременности [9].
Различают острый и хронический ВВК. Острая форма протекает не более 2-х месяцев, хроническая форма делится на рецидивирующий и персистирующий ВВК. Рецидивирующий ВВК рассматривается как особый вариант хронической формы заболевания, для которого характерны 4 и более эпизода в течение года, подтвержденные данными лабораторной диагностики. Примерно у половины женщин с рецидивирующим ВВК симптомы заболевания появляются в интервале от нескольких дней до 3-х месяцев после успешного излечения острой формы [10]. Наиболее тяжелый вариант хронической формы – персистирующий ВВК, при котором симптомы заболевания сохраняются постоянно с той или иной степенью выраженности, незначительно уменьшаясь после каждого курса терапии [11].
В зависимости от состояния вагинального микробиоценоза выделяют две формы кандидозной инфекции влагалища: истинный кандидоз, когда грибы выступают как моновозбудитель (высокая концентрация грибов сочетается с высокой концентрацией лактобактерий), и сочетание ВВК и бактериального вагиноза, когда грибы участвуют в микробных ассоциациях (грибы вегетируют при подавляющем преобладании облигатных анаэробов [12]. Кандидоносительство не является патологией ввиду наличия грибов у здоровых женщин, однако при микробиологическом исследовании в отделяемом влагалища у них обнаруживаются дрожжеподобные грибы в небольшом количестве (<104 КОЕ/мл), как правило, при отсутствии псевдомицелия [13].
Развитие кандидоза начинается с адгезии грибов к поверхности слизистой оболочки и ее колонизации, затем они проникают в эпителий и, преодолевая эпителиальный барьер слизистой, попадают в соединительную ткань собственной пластинки, преодолевая тканевые и клеточные защитные механизмы, проникают в сосуды и, распространяясь по всему организму, поражают различные органы и системы. При ВВК инфекционный процесс чаще затрагивает поверхностные слои эпителия влагалища [14].
Во время беременности возможно развитие восходящей инфекции с антенатальным инфицированием плода и новорожденного и развитие внутриутробной инфекции. Поражение плода и новорожденного чаще происходит интранатально при его прохождении через инфицированные родовые пути матери с развитием постнатального кандидоза у новорожденных. Доказаны случаи заражения трансплацентарным и восходящим путем, что ведет к врожденному кандидозу у ребенка. Инфицирование плода и новорожденного происходит при наличии у матери ВВК (особенно в III триместре беременности) и сопутствующих экстрагенитальных заболеваний [15].
Диагностика
Диагностика ВВК основывается на тщательном сборе анамнеза. При этом следует учитывать такие предрасполагающие факторы, как эндокринные заболевания (гиперкортицизм, сахарный диабет, ожирение, гипотиреоз и гипопаратиреоз), тяжелые соматические заболевания (лимфома, лейкемия, ВИЧ-инфекция и др.), осложненная беременность. Развитию кандидоза способствует применение антибиотиков широкого спектра действия, глюкокортикоидов, цитостатиков, гормональной контрацепции. Кроме того, экзогенные факторы – повышенная температура и избыточная влажность, вызывающая мацерацию кожи и слизистых оболочек, микротравмы, повреждение химическими веществами и др. – также могут быть причиной кандидоза. Воздействие одновременно нескольких предрасполагающих факторов существенно увеличивает риск развития заболевания.
Беременные предъявляют жалобы на обильные или умеренные творожистые выделения из половых путей, зуд, жжение, раздражение в области наружных половых органов, усиление зуда во время сна или после водных процедур и полового акта, неприятный запах, усиливающийся после половых контактов.
При осмотре выявляют гиперемию, отек, обильные или умеренные творожистые выделения из половых путей, высыпания в виде везикул на коже и слизистых оболочках вульвы и влагалища. При хронической форме ВВК на коже и слизистых оболочках вульвы и влагалища могут преобладать вторичные проявления в виде инфильтрации, лихенизации и атрофии тканей.
Лечение
Цель лечения ВВК – элиминация дрожжеподобных грибов рода Candida. Лечение проводится амбулаторно.
Для назначения рационального лечения необходимо учитывать клиническую форму кандидоза, его распространенность и предрасполагающие факторы (общие и местные). При любом сроке беременности предпочтительно назначать местную терапию.
Залогом выздоровления пациентки без риска хронизации процесса, развития резистентности и рецидивов является строгое следование врачебным назначениям без перерывов в лечении. К проблеме обязательного соблюдения режима местной терапии в гинекологии уделяют повышенное внимание в связи с высоким риском хронизации процесса с переходом в резистентную форму. Понятие «комплаенс» означает степень, с которой поведение больного согласуется с медицинскими требованиями. Нарушения режима лечения, отклонение от предписанных рекомендаций (снижение числа или дозы принимаемых препаратов, изменение времени приема препарата и т.д.) обозначется как нонкомплаенс (рис. 1).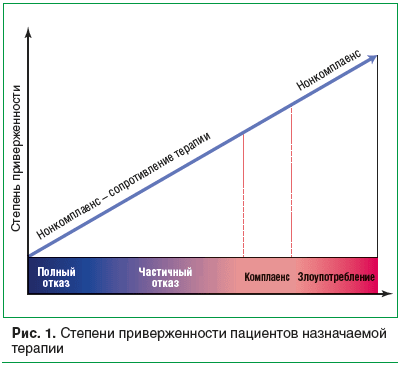
Причинами нонкомплаенса могут служить дискомфорт, вызванный нежелательными эффектами лечения, высокая стоимость, сложность приема или введения препарата, многократность приема в течение суток, побочные действия и отсутствие результата.
Побочные эффекты лекарственных препаратов, по мнению ряда исследователей, являются одной из самых значимых причин, приводящих к отказу от терапии. Однако в этом случае важны не столько количество и спектр нежелательных явлений, сколько их субъективная непереносимость: некоторые побочные эффекты столь тягостны и труднопереносимы, что больные, сознавая необходимость лечения, тем не менее отказываются от него [16].
Часто пациентки отказываются от эффективной лекарственной формы «суппозитории вагинальные» из-за неудобства применения. Некоторые формы суппозиториев после расплавления в организме женщины имеют свойство вытекать и доставляют неудобство пациентке. Для преодоления этого обстоятельства немецкая фармацевтическая компания Gattefosse создала уникальную основу из полусинтетических глицеридов для вагинальных суппозиториев – Суппоцир АМ. Суппозитории, включающие в состав Суппоцир АМ, после вагинального введения быстро расплавляются под влиянием температуры тела с образованием объемной пенистой массы, которая равномерно распределяется по слизистой оболочке с проникновением в труднодоступные складки влагалища и обеспечивает высокие биоадгезивные и мукоадгезивные свойства действующего вещества.
В последнее время в период беременности широко и эффективно применяется комплексный противогрибковый препарат Примафунгин® с широким спектром действия. Выявлена высокая эффективность Примафунгина при эрадикации C. albicans и C. non-albicans. Одним из основных показаний к применению препарата являются грибковые инфекции влагалища и вульвы – ВВК. Препарат выпускается в виде суппозиториев цилиндрично-конусной формы, содержащих 100 мг действующего вещества натамицин. Связываясь со стеролами клеточной мембраны гриба, натамицин нарушает ее проницаемость, что приводит к потере важнейших клеточных компонентов и лизису клетки. Активен в отношении большинства дрожжеподобных грибов (особенно C. albicans), дерматомицетов (Trichophyton, Microsporum, Epidermophyton), дрожжей (Torulopsis и Rhodotorula), других грибов (Aspergillus, Penicillium, Fusarium, Cephalosporium), а также в отношении некоторых простейших (трихомонад). Не влияет на грамположительные и грамотрицательные бактерии. Выраженное фунгицидное действие препарата препятствует развитию резистентности.
Суппозиторий вводится во влагалище 1 р./сут. Для удобства процедуру рекомендуется выполнять перед сном, лучше в положении лежа на боку. Предпочтительная продолжительность курса лечения составляет 6 дней. При использовании препарата не рекомендуется разрезать суппозиторий, так как активное вещество может полностью потерять лечебные свойства.
Контроль эффективности лечения проводится по окончании курса. Инфекция считается излеченной, если у пациентки нет клинических проявлений. Лечение полового партнера проводится только в том случае, если у него имеется кандидозный баланит или баланопостит, в остальных случаях необходимости лечения полового партнера нет.
В акушерском отделении ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России было проведено проспективное рандомизированное слепое исследование, включившее 60 беременных в возрасте от 18 до 37 лет (по 30 человек в каждой группе), страдающих ВВК. Пациенткам первой группы был назначен препарат Примафунгин® («Авексима», РФ), пациенткам второй группы – препарат Пимафуцин® (Temmler Italia S.r.L., Италия) по схеме 1 суппозиторий на ночь в течение 6 дней. Цель исследования – сравнительный анализ клинической эффективности и переносимости вагинальных суппозиториев при лечении ВВК у беременных женщин. Критерием включения в исследование были клинические и лабораторные признаки острой кандидозной инфекции на любом сроке беременности. Критерии исключения из исследования: хламидиоз,
микоплазменная инфекция, трихомониаз, гонорея, сифилис, генитальный герпес, хроническая кандидозная инфекция.
Эффективность лечения оценивалась:
по наличию субъективных жалоб: до лечения, на 3-й и 7-й день лечения;
при гинекологическом осмотре: до лечения, на 7-й день и через месяц после окончания лечения;
по результатам микроскопии мазка: до лечения, на 7-й день и через месяц после окончания лечения.
Клинические исследования были одобрены этическим комитетом НМИЦ АГП им. В.И. Кулакова.
На основании проведенных исследований сделаны следующие выводы.
Лекарственные средства, тестируемые в ходе исследования, продемонстрировали высокую эффективность, подтвержденную положительной динамикой клинических признаков и результатов лабораторных исследований.
При сравнительном изучении выраженности терапевтического эффекта между исследуемыми лекарственными средствами достоверных различий не выявлено.
Оба исследуемых средства характеризуются хорошей переносимостью.
Более выраженное удобство применения отмечали пациентки в группе терапии Примафунгином.
По результатам исследования, проведенного на базе НИИ акушерства и гинекологии им. Д.О. Отта СЗО РАМН, обследовано 90 женщин с признаками ВВК. У пациенток с первичным эпизодом кандидоносительства и его минимальными клиническими проявлениями проводили 6-дневный курс вагинальной аппликации Примафунгина в качестве монотерапии. При рецидивирующем кандидозном вульвовагините с выраженными клиническими симптомами проводили 9-дневный курс лечения препаратом совместно с пероральным приемом пробиотиков
и пребиотиков.
Эффективность терапии оценивали по динамикеклинических признаков и данных бактериологического (микроскопического и культурального) исследования (рис. 2).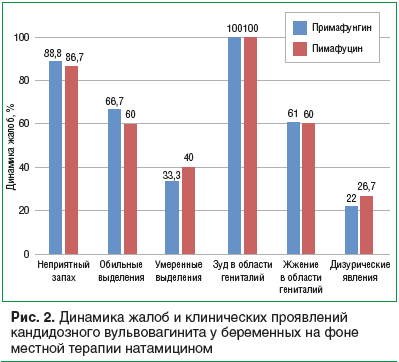
Сравнительный анализ показал сходный и достаточно быстрый клинический эффект при местном применении обоих антимикотических препаратов – Примафунгина
и Пимафуцина (рис. 3). На 5-й день лечения умеренные выделения были сходными в группе Примафунгина и в группе Пимафуцина. Однако зуд в области гениталий был выражен на 1,7% меньше в группе Примафунгина, чем в группе Пимафуцина, дизурические явления сохранялись на 4,5% чаще в группе Пимафуцина.
После окончания терапии в обеих группах клинических проявлений вагинального кандидоза не обнаружено, жалоб со стороны пациенток не поступало. При гинекологическом осмотре признаки воспаления – гиперемия и отечность слизистой влагалища – отсутствовали у всех женщин.
До лечения дрожжеподобные грибы рода Candida были обнаружены у пациенток обеих групп. При микроскопической оценке микробиоценоза влагалища были отмечены выраженная лейкоцитарная реакция и преобладание другой, нелактобациллярной флоры. Через месяц после курса терапии зафиксировано восстановление физиологического микробиоценоза влагалища в обеих группах: в отделяемом влагалища псевдомицелия, дрожжеподобных грибов не было ни у одной пациентки, у большинства преобладали лактобактерии. Клетки дрожжеподобных грибов (бластоспоры) были выявлены в единичных случаях только у беременных группы сравнения.
Кроме того, в группе, получавшей комплексную терапию, через месяц после начала лечения наблюдалось статистически значимо меньшее количество лейкоцитов во влагалище. Культуральное исследование отделяемого из влагалища у беременных с рецидивирующим вульвовагинитом через месяц после проведенной терапии показало, что в группе пациенток, получавших местную терапию Примафунгином совместно с пробиотиком и лактулозой, имел место статистически значимо более обильный рост лактобактерий при незначительном и редком росте Саndida, тогда как в группе сравнения, пациентки которой получали Пимафуцин®, рост лактобактерий был меньше, чаще сохранялся рост Candida и чаще встречались образцы с отсутствием роста влагалищной флоры [17].
Поскольку сама беременность является значимым фактором риска, то во время гестационного периода рекомендуется применять более длительные курсы антимикотической терапии, чем у небеременных пациенток [18]. Поэтому при выраженных явлениях вульвовагинита у беременных лучше рекомендовать 9-дневный курс вагинальной терапии Примафунгином. Стоимость 9-дневного курса терапии Примафунгином меньше стоимости курса терапии Пимафуцином примерно на 200 руб. при равной эффективности и большем удобстве применения.
Заключение
С целью предотвращения рецидивов заболевания показано выявление предрасполагающих факторов риска ВВК и их устранение. Необходимо провести обследование женщин на инфекции, передаваемые половым путем. После завершения курса терапии в среднем через 3 мес. у 5–25% женщин могут возникать рецидивы.
Результаты исследования и практический опыт применения вагинальных суппозиториев Примафунгин® даже у беременных с рецидивирующим ВВК и отягощенным гинекологическим анамнезом показывают его высокую эффективность в эрадикации не только C. albicans, но и C. non-albicans, без развития резистентности и без рецидивов в клинической практике. За счет высокого профиля безопасности Примафунгин® может быть рекомендован на всех сроках беременности и лактации, даже при отягощенном гинекологическом анамнезе.
Следует обратить внимание на преимущества Примафунгина – эффективность и удобство применения – в сравнении с Пимафуцином. Кроме того, стоимость курса лечения препаратом Примафунгин® ниже, чем курса лечения Пимафуцином, что также отражается на приверженности терапии. Исходя из вышеизложенного, суппозитории вагинальные Примафунгин® можно рекомендовать для широкого применения в клинической практике, включая беременных пациенток с отягощенным гинекологическим анамнезом. Терапия ВВК в период беременности необходима во избежание инфицирования плода, оптимальное лечебное действие в таких случаях окажут лекарственные средства с натамицином, не имеющие побочных эффектов.
Источник
