Статьи по вульвовагинальному кандидозу

Внедрение в клиническую микробиологию современных методов исследования позволило существенно расширить наши представления об отрицательном воздействии факторов внешней среды на микрофлору макроорганизма, что ведет к развитию разнообразных патологических процессов как воспалительного, так и невоспалительного генеза.
Речь, в частности, идет о дисбактериозе влагалища. Несмотря на появление новых методов диагностики, терапии и профилактики этого состояния, частота дисбактериоза влагалища продолжает оставаться высокой, что влияет на здоровье и психоэмоциональную сферу огромного числа женщин [1–4]. Одной из основных причин развития данного состояния является рост числа иммунодефицитных состояний, наблюдаемый на фоне ухудшения экологической обстановки, неправильного питания, частых стрессов, фармакологического бума с бесконтрольным применением лекарственных средств, в первую очередь антибиотиков [5].
Чаще всего генитальная инфекция, вызывающая дисбактериоз влагалища, обусловлена несколькими патогенными факторами — вирусами, бактериями, грибами, простейшими, которые вызывают схожие по клиническому течению, но различные по патогенезу и методам лечения заболевания [1, 6, 7].
Вульвовагинальный кандидоз является превалирующим инфекционным заболеванием, поражающим слизистую вульвы и влагалища у женщин репродуктивного возраста. В последние годы распространенность кандидоза неуклонно растет, удельный вес этого заболевания в структуре инфекционных поражений вульвы и влагалища составляет 30–45%. Вульвовагинальный кандидоз занимает второе место среди всех инфекций влагалища и является одной из наиболее распространенных причин обращения женщин к гинекологу. В США и Европе ежегодно регистрируется 13 млн случаев этого заболевания [8, 9].
Этиология
Анализ медицинской литературы последних лет свидетельствует о возросшем интересе к проблеме микозов в целом и вульвовагинального кандидоза в частности. Микозы — широко распространенная группа инфекций, которые вызываются большим числом различных видов патогенных и условно-патогенных грибов [3, 10–13].
Грибы’ (лат. Fungi или Mycota) — царство живой природы, объединяющее эукариотические организмы, сочетающие в себе некоторые признаки как растений, так и животных.
Микозы являются важной проблемой клинической медицины. Из потенциальных «болезней будущего» микозы превратились в актуальные «болезни настоящего». Возбудители микозов многочисленны, и вызываемые ими заболевания человека и животных весьма разнообразны. Количество видов микроскопических грибов (микромицетов) оценивается примерно в 100 000–200 000 видов. Ежегодно описывается приблизительно 1500 новых видов. Реальное значение в клинической практике в настоящее время имеют около 100 видов [14].
Дрожжеподобные грибы рода Candida принадлежат к семейству Cryptococcaceae. В настоящее время известно до 200 видов грибов рода Candida. Из них лишь C. albicans, С. glabrata, C. pseudotropicalis, C. tropicalis, C. krusei, C. parapsilosis, C. quillermondii и некоторые другие могут вызвать заболевания. Candida spp. — одноклеточные дрожжевые микроорганизмы размером 6–10 мкм.
Многие Candida spp. диморфны, образуют псевдомицелий или мицелий. Повсеместно некоторые Candida spp. выявляют при посевах со слизистой оболочки полости рта и ЖКТ у 30–50% здоровых людей, со слизистой оболочки гениталий — у 20–30% здоровых женщин. Поэтому важно различать заболевание (кандидоз) и колонизацию слизистых оболочек или кожи, при которой применения антимикотиков обычно не требуется.
Источник возбудителя инвазивного кандидоза обычно эндогенный, поскольку Candida spp. — естественные обитатели слизистых оболочек и кожи человека [15].
Основная роль в возникновении вагинального кандидоза принадлежит грибам рода Candida albicans, которые выделяются в 95% случаев этого заболевания. Они являются наиболее патогенными вследствие высокой адгезивной способности и выработки литических ферментов, обеспечивающих их пенетрацию в эпителиоциты влагалища [16].
Факторами риска развития вагинального кандидоза являются:
- длительный и/или бессистемный прием антибиотиков [17];
- беременность;
- использование оральных контрацептивов (особенно с высоким содержанием эстрогенов);
- применение кортикостероидов, цитостатиков, лучевой терапии;
- эндокринные заболевания (сахарный диабет, дисфункция яичников);
- развитие иммунодефицита (тяжелые инфекционные заболевания, травмы, операции).
Предрасполагающими к развитию заболевания факторами могут быть:
- ношение синтетической облегающей одежды;
- ожирение;
- несоблюдение гигиенических условий;
- жаркий климат;
- использование гигиенических средств;
- употребление йогуртов и продуктов с повышенным содержанием лактобацилл [18].
В то же время подчеркивается противоречивость полученных данных в отношении перечисленных факторов риска развития вульвовагинального кандидоза, что обусловливает необходимость проведения дополнительных исследований [19].
Особенности инфекции
В развитии кандидозной инфекции различают следующие этапы:
1. Адгезия грибов к поверхности и колонизация грибами слизистой оболочки.
2. Инвазия в эпителий, преодоление эпителиального барьера слизистой оболочки, попадание в соединительную ткань собственной пластинки, преодоление тканевых и клеточных защитных механизмов.
3. Проникновение в сосуды и гематогенная диссеминация с поражением различных органов и систем.
Значительное увеличение числа случаев вульвовагинального кандидоза обусловлено действием предрасполагающих факторов, описанных выше. При назначении антибиотиков широкого спектра действия необходимо учитывать, что они подавляют не только патогенные бактерии, но и находящиеся во влагалище лактобациллы, являющиеся физиологическими антагонистами дрожжеподобных грибов (лактобациллы подавляют прикрепление Candida к клеткам эпителия и их размножение). В результате сдвига рН в щелочную среду влагалищного содержимого процесс самоочищения влагалища нарушается. Кроме того, Candida обладают способностью использовать антибиотики в качестве источников питания. При этом создаются благоприятные условия для активного размножения Candida в половых органах женщины [20].
Принято различать 3 клинические формы вагинального кандидоза:
- кандидоносительство;
- острая форма вульвовагинального кандидоза;
- хронический (рецидивирующий) вульвовагинальный кандидоз.
Кандидоносительство характеризуется отсутствием симптомов заболевания, но в микробиологическом исследовании в отделяемом влагалища дрожжеподобные грибы рода Candida присутствуют в небольшом количестве (<104 КОЕ/мл). Бессимптомное носительство Candida отмечается у 15–20% небеременных женщин репродуктивного возраста.
Терминология острого и хронического вульвовагинального кандидоза, подразумевающая только частоту рецидивов, упрощает постановку диагноза, но в то же время выделение в классификацию осложненной и неосложненной форм заболевания подразумевает вид возбудителя, тяжесть течения заболевания, а также состояние макроорганизма, что влияет на выбор способа терапии [20].
По мнению ряда авторов, причинами рецидивирующего вульвовагинального кандидоза являются изменения в локальном и клеточном иммунитете на уровне слизистой оболочки влагалища. Меньшее значение имеет гуморальный и врожденный иммунитет. Т1- и Т2-опосредованные клеточные реакции коррелируют с резистентностью и предрасположенностью к кандидозу слизистых оболочек. Реактивность Т1-типа с продукцией ИЛ-2, ИЛN-g и ИЛ-12 (стимулирующие макрофаги и полиморфно-ядерные лимфоциты), а также IgА слизистой оболочки являются доминирующими реакциями во влагалище. Они поддерживают бессимптомную колонизацию Candida. Реактивность Т2-типа с образованием ИЛ-4-6, ИЛ-10, IgG, гистамина и простагландина Е2 преобладает в тех случаях, когда эндогенные и экзогенные факторы приводят к увеличению числа микроорганизмов C. albicans. Этот ответ «выключает» защитные реакции Т1-типа и запускает реакции гиперчувствительности немедленного типа. Candida из фазы бластоспоры переходит в фазу гифы и возникает инвазия эпителия [21].
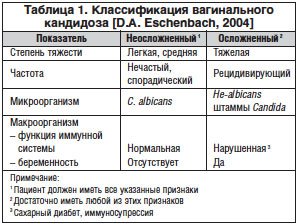
В настоящее время наиболее современная классификация вагинального кандидоза предложена D. A. Eschenbach (табл. 1) [22].
Одной из основных особенностей течения вульвовагинального кандидоза является его частое сочетание с условно-патогенной бактериальной микрофлорой, обладающей высокой ферментативной и литической активностью, что создает благоприятные условия для внедрения грибов в ткани [23].
Клиническими проявлениями вульвовагинального кандидоза являются: интенсивно выраженное раздражение и зуд во влагалища; типичные белые творожистые выделения и жжение в области наружных половых органов при мочеиспускании и болезненность при половом акте.
При хроническом рецидивирующем заболевании часто наблюдают обострение перед началом менструации [24].
Диагностика острого вульвовагинального кандидоза не представляет сложностей — это микроскопия патологического материала (соскобы со слизистых оболочек пораженных участков) и обнаружение в нативных или окрашенных по Граму препаратах дрожжевых почкующихся клеток и/или псевдомицелия и мицелия Candida spp. Во всех случаях необходимо исключить инфекции, передаваемые половым путем. Можно использовать рН-исследование. Если при цитологическом методе исследования Candida spp. не обнаружены (чувствительность метода составляет 65–70%), при наличии характерных клинических проявлений следует выполнить культуральное исследование (посев материала на специализированные среды) с целью обнаружения колоний Candida spp. В случае острого кандидоза указанных диагностических мероприятий вполне достаточно для постановки этиологического диагноза. При хроническом рецидивирующем вульвовагинальном кандидозе необходимы видовая идентификация возбудителя (при этой форме заболевания частота обнаружения грибов Candida, не относящихся к виду С. albicans, составляет до 20–25%) и определение чувствительности выделенной культуры грибов к антимикотическим препаратам [25–28].
Также можно использовать молекулярно-биологические методы исследования (полимеразная цепная реакция) — выявление ДНК определенного вида дрожжеподобных грибов, серологические реакции — реакция агглютинации (РА), реакция связывания комплемента (РСК), реакция преципитации, реакция пассивной гемагглютинации. Из комплекса серологических исследований наиболее существенное значение имеет РСК с дрожжевыми антигенами (1:10, 1:16). Диагностическим титром РА при кандидозах считается разведение сыворотки более чем 1:100 и иммуноферментный анализ — определение IgE-антител против C. albicans во влагалищных смывах. Наиболее высоким является титр IgE-антител к серотипу, А, который составляет 83% всех штаммов C. аlbicans [29].
Около 20–25% женщин с отрицательным результатом бактериологического исследования имеют положительные результаты посева на Candida уже через 30 дней после лечения. Это означает, что незначительное число микроорганизмов остается персистировать во влагалище, причем этого количества недостаточно для возникновения симптомного вагинита, но достаточно для того, чтобы при воздействии перечисленных триггерных факторов, стимулирующих избыточный рост грибов, привести к рецидиву заболевания [30].
Установлена прямая связь между сроком гестации и частотой возникновения вагинального кандидоза, для которого во время беременности характерны бессимптомное течение и частые рецидивы. Если грибы рода Candida обнаруживаются во влагалище 10–17% небеременных женщин, то вагинальный кандидоз у беременных встречается, по различным данным, в 30–40% случаев, достигая перед родами 44,4% [31]. Такие высокие показатели обусловлены изменениями гормонального баланса во время беременности [8].
Лечение
Современная фармакология предоставляет большой выбор препаратов антимикотического действия, но вопрос эффективности лечения на сегодняшний день остается до конца не решенными и не теряет своей актуальности. Требуется доработка старых и разработка новых схем лечения вульвовагинального кандидоза.
Терапия зависит от клинической формы заболевания. Основной целью назначения препаратов, обладающих адекватным спектром действия, является одновременное воздействие непосредственно на возбудителя и возможные системные резервуары дрожжеподобных грибов для эрадикации возбудителя и исключения возможных рецидивов [20].
Улучшению терапии вульвовагинального кандидоза способствуют сексуальное воздержание, объяснение врачом природы инфекции и способов лечения, понимание пациенткой, что исчезновению симптомов заболевания должна сопутствовать микробиологическая санация [32].
Для лечения вульвовагинального кандидоза в настоящее время используют следующие основные антимикотические препараты:
- полиенового ряда (натамицин, нистатин, леворин, амфотерицин В);
- имидазолового ряда (клотримазол, кетоконазол, омоконазол, миконазол, бифоназол и др.);
- триазолового ряда (флуконазол, итраконазол);
- прочие препараты (гризеофульвин, флуцитозин, хлорнитрофенол, деквалиния хлорид, препараты йода и др.).
Различают следующие пути введения противогрибковых средств:
- системный (пероральный, внутривенный и др.);
- местный (вагинальные суппозитории, таблетки и глобули, кремы, растворы) [33].

Впервые зарегистрированный в России сертаконазол (рис. 1) в виде вагинальных суппозиториев с длительным высвобождением препарата, содержащих 300 мг активного вещества, произведен Laboratoires Théramex (Монако) и маркетируется на российском рынке по лицензии фирмы Ferrer Internacionale A.S. (Испания) венгерским фармацевтическим заводом EGIS под торговым названием Залаин (Zalain). Залаин является противогрибковым средством — производным бензотиофена и имидазола — для местного использования.
Залаин вызывает лизис клеток грибов. Также механизм действия данного препарата связан с конкурентным антагонизмом с другим компонентом оболочки клеток — триптофаном. В терапевтических дозах препарат обладает фунгицидным и фунгистатическим действием. При интравагинальном введении высокие уровни Залаина сохраняются во влагалище продолжительное время и значительно превышают и минимальные ингибирующие, и фунгицидные концентрации против C. albicans, C. glabrata и прочих грибов, которые не относятся к роду Candida. Системное всасывание отсутствует при интравагинальном использовании. Залаин в неизмененном виде не обнаруживается ни в моче, ни в плазме крови.
В состав Залаина введен принципиально новый компонент — бензотиофен, который провоцирует разрыв плазматической мембраны клетки гриба, что и приводит к ее гибели, т. е. обеспечивается фунгицидное действие препарата. Бензотиофен обладает высокой липофильностью, чем усиливает проникновение препарата в кожу и ее придатки. Благодаря такому двойному механизму действия риск развития рецидивов является минимальным. Побочных эффектов и аллергических реакций при применении Залаина не отмечено ни у одной женщины.
Проведенные исследования показали, что Залаин — производное имидазола и бензотиофена, является эффективным и безопасным средством для лечения острого вульвовагинального кандидоза. Кроме выраженного антимикотического эффекта препарат обладает широким спектром действия (в т. ч. влияет и на неспецифическую флору: Streptococcus spp., Staphylococcus spp., Proteus spp., Bacteroides spp., E. сoli). Высокая клиническая эффективность Залаина (97,8%), короткий курс лечения, удобство применения, низкая частота побочных эффектов, незначимое системное воздействие, широкий спектр действия позволяют считать этот препарат перспективным в лечении острого вульвовагинального кандидоза, в т. ч. в сочетании с неспецифическим вагинитом, у небеременных и некормящих женщин [33].
При исследовании штаммов грибов, выделенных из влагалищного содержимого, были проведены тесты на чувствительность к различным азолам, нистатину, амфотерицину B и флуцитозину. Оказалось, что чувствительность к Залаину превосходила таковую к другим антимикотикам, свидетельствуя о большей активности Залаина [35].
Учитывая, что беременность является основным предрасполагающим фактором для развития вульвовагинального кандидоза, особую проблему представляет его лечение при данном состоянии [36].
К препаратам, применяемым у беременных, предъявляют особые требования. Наряду с высокой эффективностью и минимальной способностью индуцировать развитие резистентности у возбудителей, они должны характеризоваться низкой эмбриотоксичностью и хорошей переносимостью для матери. Некоторые противогрибковые препараты противопоказаны при беременности в связи с наличием у них тератогенного эффекта. С целью снижения риска развития нежелательных системных эффектов у матери и плода наиболее безопасным в период беременности является интравагинальный путь введения антимикотиков. Кроме того, при таком способе введения быстрее наступают редукция клинической симптоматики и выздоровление [12].
В связи с этим проведено исследование, в котором было выявлено, что Залаин высокоэффективен при однократном режиме лечения у беременных женщин. При этом его переносимость и удобство в применении позволяют считать данный препарат одним из перспективных в антифунгальной терапии острого вульвовагинального кандидоза у женщин во время беременности [37].
В заключение можно сказать, что Залаин можно использовать для лечения как острой формы вульвовагинального кандидоза, так и рецидивирующей, а также у беременных женщин.
Источник
Лечение кандидозного вульвовагинита
Препараты для местного применения обеспечивают эффективное лечение вульвовагинального кандидоза. Применяемые местно азоловые препараты более эффективны, чем нистатин. Лечение азолами приводит к исчезновению симптомов и микробиологическому излечению в 80-90% случаев после завершения терапии.
Рекомендованные схемы лечения кандидозного вульвовагинита
Следующие интравагинальные формы препаратов рекомендуются для лечения вульвовагинального кандидоза:
Бутоконазол 2% крем, 5 г интравагинально в течение 3 дней**
или Клотримазол 1% крем, 5 г интравагинально в течение 7-14 дней**
или Клотримазол 100 мг вагинальная таблетка в течение 7 дней*
или Клотримазол 100 мг вагинальная таблетка, по 2 таблетки в течение 3 дней*
или Клотримазол 500 мг 1 вагинальная таблетка однократно*
или Миконазол 2% крем, 5 г интравагинально в течение 7 дней**
или Миконазол 200 мг вагинальные свечи, по 1 свече в течение 3 дней**
или Миконазол 100 мг вагинальные свечи, по 1 свече в течение 7 дней**
* Эти кремы и свечи имеют масляную основу и могут повреждать латексные презервативы и диафрагмы. Для подробной информации см. аннотацию к презервативам.
** Препараты отпускаются без рецепта (ОТС).
или Нистатин 100 000 ЕД, вагинальная таблетка, 1 таблетка в течение 14 дней
или Тиоконазол 6,5% мазь, 5 г интравагинально однократно**
или Терконазол 0,4% крем, 5 г интравагинально в течение 7 дней*
или Терконазол 0,8% крем, 5 г интравагинально в течение 3 дней*
или Терконазол 80 мг свечи, по 1 свече течение 3 дней*.
Пероральный препарат:
Флюконазол 150 мг – пероральная таблетка, одна таблетка однократно.
Интравагинальные формы бутоконазола, клотримазола, миконазола и тиоконазола отпускаются без рецепта, и женщина с вульвовагинальным кандидозом может выбрать одну из этих форм. Продолжительность лечения этими препаратами может составлять 1, 3 или 7 дней. Самолечение препаратами, которые отпускаются без рецепта, рекомендуется только в тех случаях, если у женщины раньше был диагностирован вульвовагинальный кандидоз или наблюдаются такие симптомы при рецидивах. Любой женщине, у которой симптомы персистируют после лечения средствами, отпускаемыми без рецептов, или рецидивы симптомов наблюдаются в течение 2 месяцев, следует обращаться за медицинской помощью.
Новая классификация вульвовагинального кандидоза может облегчить выбор противогрибковых препаратов, а также продолжительность лечения. Неосложненные вульвовагинальные кандидозы (от слабовыражен-ных до умеренных, спорадических, нерецидивирующих заболеваний), вызванные чувствительными штаммами С. albicans) хорошо лечатся препаратами азола, даже при коротком (
Напротив, осложненные вульвовагинальные кандидозы (тяжелые местные или рецидивирующие вульвовагинальные кандидозы у пациентки, имеющей соматические заболевания, например, неконтролируемый диабет или инфекцию, вызванную менее чувствительными грибами, например, С. glabrata), требуют более продолжительного (10-14 дней) лечения с применением либо местных, либо пероральных препаратов азола. Дополнительные исследования, подтверждающие правильность этого подхода продолжаются.
[8], [9], [10], [11], [12], [13], [14]
Альтернативные схемы лечения кандидозного вульвовагинита
В ряде испытаний показано, что некоторые пероральные азоловые препараты, такие как кетоконазол и итраконазол, могут быть так же эффективны, как и препараты для местного применения. Простота использования пероральных препаратов является их преимуществом по сравнению с препаратами местного действия. Однако необходимо иметь в виду возможное проявление токсичности при использовании системных препаратов, особенно кетоконазола.
Последующее наблюдение
Пациенты должны быть проинструктированы о необходимости повторного визита только в том случае, если симптомы не исчезают или рецидивируют.
[15], [16], [17], [18], [19]
Ведение половых партнеров при кандидозном вульвовагините
Вульвовагинальный кандидоз не передается половым путем; лечение половых партнеров не требуется, но может быть рекомендовано для пациенток с рецидивирующей инфекцией. У небольшого числа половых партнеров-мужчин может наблюдаться баланит, характеризующийся эритематозными участками на головке полового члена в сочетании с зудом или воспалением; таких партнеров следует пролечивать с использованием местных противогрибковых препаратов до разрешения симптомов.
Особые замечания
Аллергия и непереносимость рекомендованных препаратов
Местные средства обычно не вызывают системных побочных эффектов, хотя возможно возникновение жжения или воспаление. Пероральные средства иногда вызывают тошноту, боли в животе и головные боли. Терапия с использованием пероральных азолов иногда приводит к повышению уровней печеночных ферментов. Частота возникновения гепатотоксичности, связанной с терапией кетоконазолом, колеблется на уровне от 1:10 000 до 1:15 000. Могут наблюдаться реакции, связанные с одновременным назначением таких препаратов, как астемизол, антагонисты кальциевых каналов, цизаприд, кумариноподобные агенты, циклоспорин А, пероральные препараты, снижающие содержание сахара в крови, фенитоин, такролим, терфенадин, теофиллин, тиметрексат и рифампин.
[20], [21], [22], [23], [24], [25], [26]
Беременность
ВВК часто наблюдается у беременных женщин. Для лечения можно использовать только препараты азола для местного применения. У беременных наиболее эффективными препаратами являются: клотримазол, миконазол, бутоконазол и терконазол. Во время беременности большинство экспертов рекомендует 7-дневный курс терапии.
ВИЧ-инфекция
Проводимые в настоящее время проспективные контролируемые исследования подтверждают возрастание количества вульвовагинальных кандидозов у ВИЧ-инфицированных женщин. Нет подтвержденных данных о различной реакции ВИЧ-серопозитивных женщин с вульвовагинальными кандидозамина соответствующую противогрибковую терапию. Поэтому, женщин с ВИЧ-инфекцией и острым кандидозом следует лечить так же, как и женщин без ВИЧ-инфекции.
Рецидивирующий вульвовагинальный кандидоз
Рецидивирующим вульвовагинальным кандидозом (РВВК), (четыре и более эпизодов вульвовагинальных кандидозов в год), страдает менее 5% женщин. Патогенез рецидивирующего вульвовагинального кандидоза изучен плохо. К факторам риска относятся: диабет, иммуносупрессия, лечение антибиотиками широкого спектра действия, лечение кортикостероидами и ВИЧ-инфекция, хотя у большинства женщин с рецидивирующим кандидозом связь с этими факторами не очевидна. В клинических испытаниях по ведению пациенток с рецидивирующим вульвовагинальным кандидозом применяли непрерывную терапию между эпизодами.
Лечение рецидивирующего вульвовагинального кандидоза
Оптимальная схема лечения рецидивирующего вульвовагинального кандидоза не установлена. Однако рекомендуется применять первоначально интенсивную схему в течение 10-14 дней, а затем продолжить поддерживающее лечение, по крайней мере, в течение 6 месяцев. Кетоконазол, 100 мг перорапьно 1 раз в день на протяжении
Несмотря на то, что пациентки с рецидивирующим вульвовагинальным кандидозом должны быть обследованы на наличие предрасполагающих факторов риска, рутинное выполнение тестов на ВИЧ-инфекцию у женщин с рецидивирующим вульвовагинальным кандидозом, не имеющих факторов риска в отношении ВИЧ-инфекции, не рекомендуется.
Последующее наблюдение
Пациентки, получающие лечение по поводу рецидивирующего вульвовагинального кандидоза должны проходить регулярное обследование для определения эффективности лечения и выявления побочных эффектов.
[27], [28], [29], [30], [31], [32], [33], [34]
Ведение половых партнеров
Лечение половых партнеров местными средствами может быть рекомендовано в том случае, если у них есть симптомы баланита или дерматита на коже полового члена. Однако, рутинное лечение половых партнеров обычно не рекомендуется.
ВИЧ-инфекция
Имеется мало данных, касающихся оптимального ведения рецидивирующего вульвовагинального кандидоза у ВИЧ-инфицированных женщин. Пока эта информация недоступна, ведение таких женщин должно осуществляться так же, как и женщин без ВИЧ-инфекции.
Источник
