Современные подходы в лечении неспецифического язвенного колита
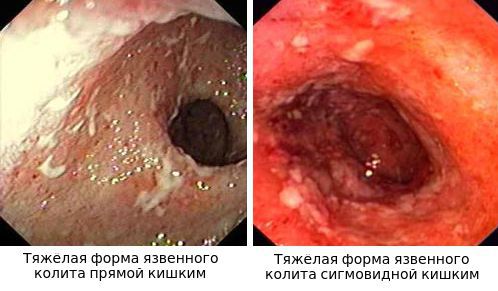
Неспецифический язвенный колит (или просто язвенный колит) — хроническое воспаление толстой кишки аутоиммунного характера. Данное заболевание относится к группе воспалительных заболеваний толстого кишечника.
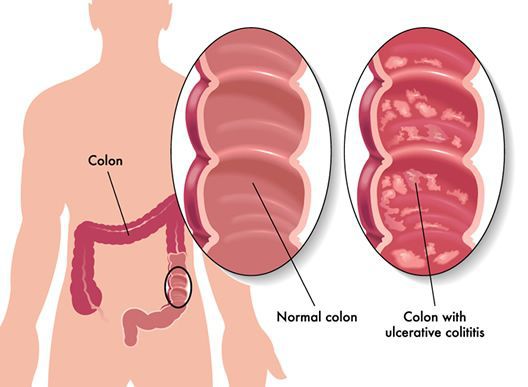
Эпидемиология
Заболевание преобладает в развитых странах Европы и Северной Америки. Язвенный колит встречается в 20-260 случаев на 100 000 человек. С каждым годом число заболевших увеличивается.[2]
Чаще всего болеют лица в возрасте от 21 до 42 лет, а также пациенты после 54 лет. Самые опасные периоды в развитии язвенного колита — это первый год болезни (из-за быстрого развития воспаления при фульминантном течении появляются осложнения, опасные для жизни) и десятый год (за этот период развиваются злокачественные новообразования).
Факторы риска до сих пор до конца не изучены. Существует следующая закономерность:
- Взаимосвязь курения и язвенного колита. По статистическим данным курящие люди реже болеют язвенным колитом.
- Аппендэктомия (удаление аппендицита) в анамнезе снижает заболеваемость язвенным колитом.
- Снижение количества пищевых волокон способствует появлению болезни.
- Лица, чаще болеющие детскими инфекциями, имеют склонность к появлению данного заболевания.
Этиология
Происхождение язвенного колита на сегодняшний день неизвестно. Существуют следующие теории развития заболевания:
- Язвенный колит возникает под действием определённых экзогенных (внешних) факторов, которые не известны. Предположительной причиной является инфекция.
- Заболевание имеет аутоиммунный характер. Существует наследственная предрасположенность к развитию болезни. Под воздействием определённых факторов запускаются иммунные реакции, вырабатываются антитела, направленные на клетки толстого кишечника.
- Язвенный колит развивается вследствие реакции организма на определённые продукты питания, при этом воспаляется кишечная стенка.
Первые признаки заболевания: кровь и слизь в стуле, диарея, боли в животе, повышение температуры тела.
Основными симптомами неспецифического язвенного колита кишечника являются:
- кишечные кровотечения;
- диарея;
- запор;
- боль в животе;
- тенезмы (ощущение постоянных режущих, тянущих, жгучих болей в толстой кишке — позывов к дефекации, однако при этом выделение кала не происходит);
- лихорадка;
- снижение массы тела;
- тошнота, рвота;
- слабость;
- внекишечные симптомы (артрит, узловатая эритема, увеит и другие).
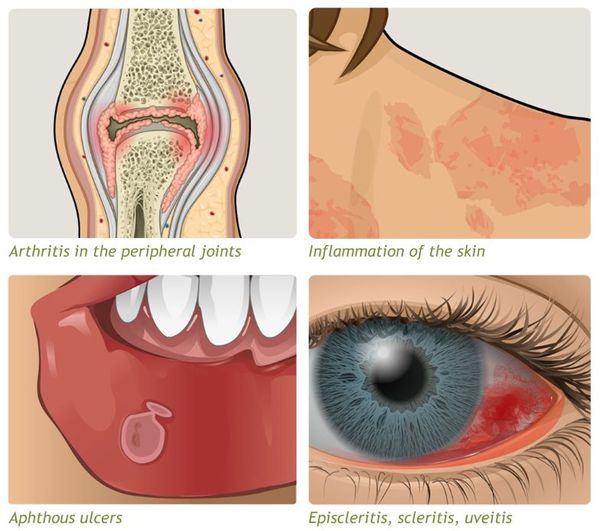
Заболевание хроническое — симптомы возникают только при обострении, при ремиссии их может не быть.
Характер преобладающей симптоматики зависит от тяжести заболевания и вовлечённого в воспалительный процесс отдела толстого кишечника. Например, при тотальном поражении наблюдается частый жидкий стул с большим количеством крови в кале, боли в животе спастического характера. При тяжёлом течении присоединяются симптомы общей интоксикации (лихорадка, тошнота, рвота, слабость).
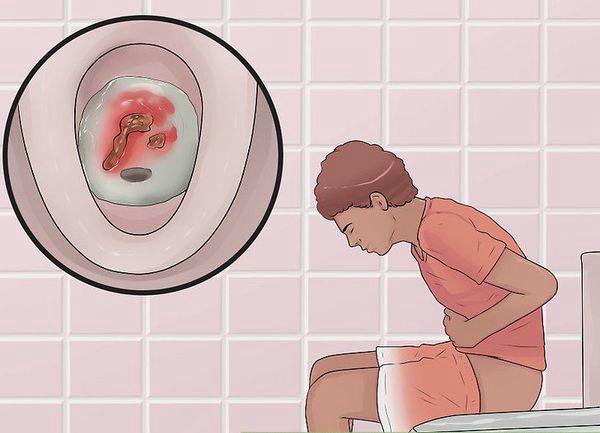
При поражении дистальных отделов толстого кишечника (проктит) чаще возникает запор, ложные позывы на дефекацию, тенезмы, в кале обнаруживаются следы алой крови, слизи или гноя. Для оценки тяжести язвенного колита предложены критерии Truelove и Witts.
При язвенном колите происходит каскад воспалительных реакций. В результате воздействия триггерного (инициирующего) фактора стимулируются Т- и В-лимфоциты, что, в свою очередь, приводит к образованию иммуноглобулинов М и G. Дефицит Т-супрессоров усиливает аутоиммунный ответ. Образование иммуноглобулинов М и G приводит к появлению иммунных комплексов и активации сиcтемы комплемента, который обладает цитотоксическим действием. В очаг воспаления проникают нейтрофилы и фагоциты, при этом высвобождаются медиаторы воспаления.
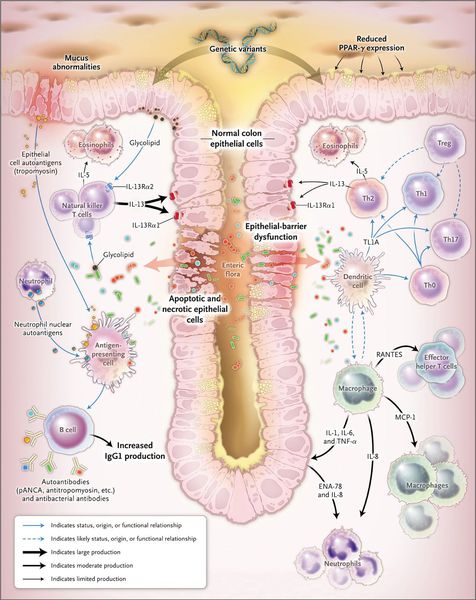
Одним из механизмов патогенеза язвенного колита является нарушение барьерной функции слизистой оболочки толстой кишки и регенераторной функции.
Реакция организма на стресс с патологическим нейрогуморальным ответом приводит к активизации аутоиммунного процесса. Часто больные язвенным колитом имеют эмоциональную нестабильность.
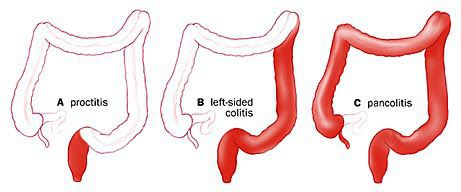
По распространённости процесса различают:
- проктит (с вовлечением прямой кишки);
- левосторонний колит (поражение прямой сигмовидной и нисходящей ободочной кишки);
- тотальный колит (поражение всех отделов толстого кишечника).
По степени тяжести течения:[3]
- лёгкое течение;
- среднетяжёлое течение;
- тяжёлое течение.
По характеру течения:
- острое течение (менее 6 месяцев от начала болезни);
- фульминантное (быстро развивающееся);
- постепенное;
- хронический язвенный колит непрерывного течения (периоды ремиссии (ослабления симптомов) менее 6 месяцев при правильном лечении);
- хронический язвенный колит рецидивирующего течения (периоды ремиссии более 6 месяцев): редко рецидивирующее (один раз в год или меньше) или часто рецидивирующее (более 2 раз в год).
Язвенный колит — это хроническое заболевание, при котором бывают периоды, когда возникает обострение и периоды, когда симптомы затухают или не выявляются — стадия ремиссии. Язвенный колит может обостряться без явной причины, однако чаще это происходит под воздействием стресса, неправильного питания и приёме некоторых лекарств.
Местные осложнения
К местным осложнениям относятся:
- перфорация;
- токсическая дилатация (расширение) толстого кишечника;
- обильное кишечное кровотечение;
- колоректальный рак.
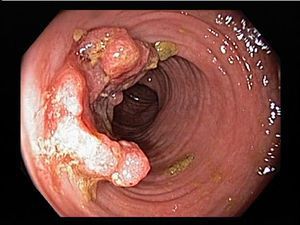
Системные осложнения
Проявляются внекишечными симптомами, причина которых до сих пор не изучена. Чаще поражаются ротовая полость, кожа, суставы.
К системным осложнениям относятся:
- узловатая эритема (поражение кожи и подкожной клетчатки);
- гангренозная пиодермия (поражение кожи крупными болезненными язвами);
- эписклерит (поражение эписклеральной ткани глаза);
- артропатия (поражение суставов);
- анкилозирующий спондилит (воспаление суставов позвоночника);
- поражения печени (повышение трансаминаз крови, гепатомегалия);
- первичный склерозирующий холангит (сужение просвета желчных протоков в результате воспаления).
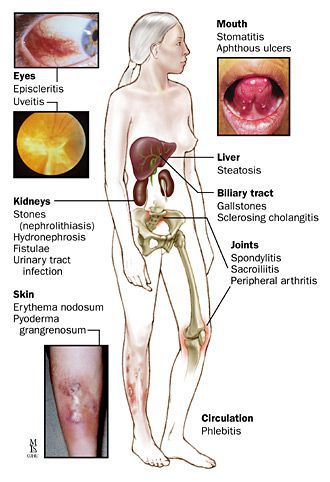
При диагностике в первую очередь оценивается клиника заболевания, анамнез, производится осмотр с обязательным пальцевым исследованием прямой кишки.
Наиболее важными в диагностике язвенного колита являются эндоскопические методы исследования: ректороманоскопия, колоноскопия с биопсией. Так же для уточнения диагноза применяются ирригоскопия, МСКТ-колоноскопия.
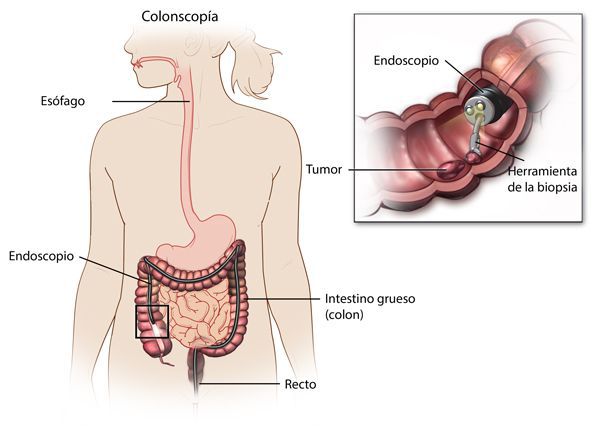
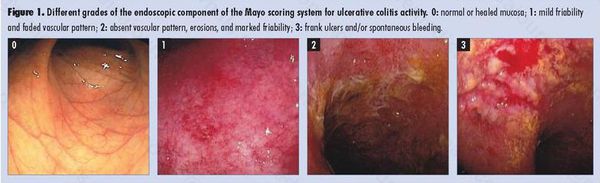
По эндоскопической картине можно определить степень воспаления толстого кишечника. Существуют четыре степени воспаления кишечника:
- При I степени наблюдается отёчность слизистой оболочки, гиперемия, сглаженность или отсутствие сосудистого рисунка, определяются точечные кровоизлияния, слизистая ранима, контактно кровоточит.
- При II степени добавляется зернистость, могут присутствовать эрозии, фиброзный налёт на стенках кишки.
- При III степени эрозии сливаются между собой, образуются язвы, в просвете кишки гной и кровь.
- При IV степени, помимо вышесказанного, появляются псевдополипы, состоящие из грануляционной ткани.

Язвы не проникают глубже подслизистого слоя.
При рентгенологическом исследовании определяется:
- отсутствие гаустр (мешкообразных выпячиваний стенки толстой кишки);
- сглаженность контуров;
- изъязвления, отёк, зубчатость, двойной контур;
- утолщение слизистой и подслизистой оболочек;
- преимущественно продольные и грубые поперечные складки;
- воспалительные полипы.
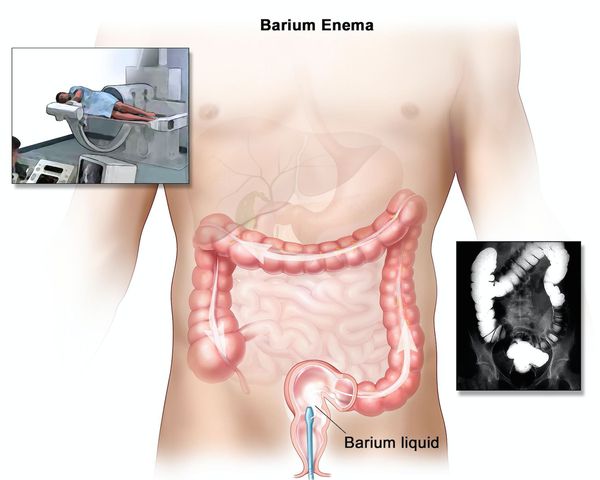
Ирригоскопия помогает не только в диагносте язвенного колита, но и в выявлении серьёзных осложнений, таких как токсическая дилатация (чрезмерное расширение просвета толстой кишки).
Дифференциальный диагноз:
- Для подтверждения диагноза «Инфекционный колит» используют бактериологическое исследование.
- Диагноз «Болезнью Крона» ставится на основании эндоскопической картины и гистологического исследования биоптата слизистой.
- Ишемический колит.
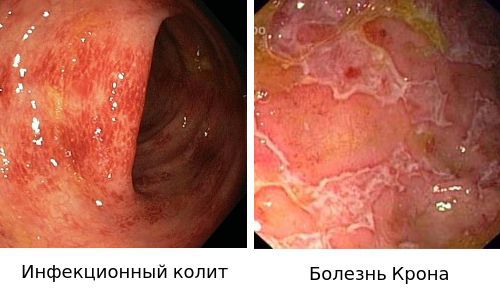
Тактика зависит от локализации поражения и тяжести течения. При дистальных формах заболевания течение обычно лёгкое, поэтому больные могут лечиться в амбулаторных условиях. Тотальное или левостороннее поражение чаще имеет тяжёлое течение, поэтому требует госпитализации и лечения в условиях стационара.
Диета
Назначаются диеты № 4, 4Б, 4В по Певзнеру. Цель диеты — уменьшить воспаление, бродильные и гнилостные процессы в кишечнике, нормализовать функции кишечника и других органов пищеварения. Блюда жидкие, полужидкие, протёртые, сваренные в воде или на пару. Исключены очень горячие и холодные блюда.
Разрешённые при язвенном колите продукты:
- сухари, супы слизистой консистенции, сваренные на обезжиренном мясном, рыбном бульоне или овощном отваре, с хорошо проваренными крупами, лапшой или вермишелью, допускается добавление фрикаделек;
- нежирное мясо и рыба;
- тщательно проваренные каши;
- фруктовые пюре;
- свежий протёртый творог;
- сахар в маленьких дозах;
- желе и кисели из черники, кизила, черемухи, айвы, груш;
- крепкий черный чай, можно с лимоном, отвар из шиповника, черной смородины, черники и черемухи;
- паровой омлет, яйца, сваренные вкрутую; сливочное масло.
Запрещенные при язвенном колите продукты:
- сдоба и кондитерские изделия;
- чёрный хлеб;
- мясные и рыбные жирные бульоны;
- колбасы, солёная и копчёная рыба, консервы;
- алкоголь;
- кофе;
- молоко;
- газированные сладкие напитки;
- свежие овощи и фрукты;
- перловая и пшеничная каши, бобовые.
Консервативная терапия
К консервативной терапии относятся:
- аминосалицилаты, препараты 5-аминосалициловой кислоты (5-АСК, месалазин);
- кортикостероиды;
- иммунодепрессанты;
- билогическая терапия.
Аминосалицилаты являются препаратами первой линии и применяются в первую очередь. Для купирования атаки язвенного колита обычно требуется 3-6 недель терапии по 1-2 г/кг в сутки. После этого проводится противорецидивное лечение сульфасалазином (3 г/сут) или месалазином (2 г/сут).
При дистальном поражении (проктит) отдаётся предпочтение формам препарата в виде свечей. При левостороннем поражении — препаратам в форме пены для ректального применения. При тотальном поражении используют таблетированные формы препаратов.
При лечении данными препаратами ремиссия достигается в 74-81 % случаев.
Наиболее выраженным и эффективным противовоспалительным средством являются глюкокортикоиды.
Основными показаниями для лечения глюкокортикоидами являются:
- острое течение тяжёлой и среднетяжёлой степени;
- тяжёлое или среднетяжёлое левостороннее и тотальное поражение при наличии III степени воспаления по данным эндоскопического исследования;
- неэффективность или недостаточная эффективность лечения аминосалицилатами при хроническом течении заболевания.
При остром тяжёлом течении назначают внутривенное введение глюкокортикоидов (преднизолона не менее 120 мг/сут) 4-6 раз в день. Обязательно проводится коррекция водно-электролитного баланса, переливание компонентов крови, гемосорбция. Через неделю после внутривенного введения переходят на приём преднизолона внутрь. За это время проводится гастроскопия для исключения язвенной болезни желудка и двенадцатиперстной кишки.
При среднетяжёлой форме можно ограничиться пероральным приёмом преднизолона. Обычно преднизолон назначается в дозе 1,5-2 мг/кг массы тела в сутки. Максимальная доза 100 мг (у лиц пожилого возраста 60 мг).
Если отсутствуют побочные эффекты, то приём продолжают ещё 10-14 дней, затем снижают дозу на 10 мг каждые 10 дней. С 30-40 мг переходят на однократный приём преднизолона. С 30 мг дозу снижают по 5 мг в неделю. Обычно курс гормональной терапии составляет от 8 до 12 недель. Параллельно с гормонотерапией применяют аминосалицилаты до полной отмены гормонов.
При проктите применяются глюкокортикоиды ректально в микроклизмах. Обычно для этого используют гидрокортизон, применяют после дефекации 2 раза в день.
Побочные эффекты гормонотерапии:
- отёки;
- артериальная гипертензия;
- остеопороз;
- различные вегетативные расстройства;
- может способствовать развитию язвы желудка, а, как следствие, может возникнуть желудочно-кишечное кровотечение.
Современным глюкокортикоидом является буденофальк (содержащий будесонид). Суточная доза составляет 3 мг будесонида (1 капсула) 4-6 раз в сутки.
При лечении глюкокортикоидами может возникнуть гормональная зависимость или даже гормонорезистентность, которая формируется у 20-35 % больных тяжёлым язвенным колитом. Гормональная зависимость — это ответ организма на лечение глюкокортикоидами, при котором возобновляется воспалительный процесс после снижения дозировки.
При отсутствии эффекта от гормональной терапии назначают препараты, обладающие иммуносупрессивным действием, а также биологическую терапию. Основными из них являются 6-меркаптопурин и азатиоприн — это препараты первой линии. Они помогают уменьшить дозу гормонов и отменить их в 62-71 % случаев. Лечение обычно начинают вместе с гормонотерапией. Максимальная суточная доза — 150 мг. Незначительное количество побочных эффектов, по сравнению с глюкокортикоидами, позволяет применять препарат на протяжении многих лет.
Также существует аналогичный препарат — метотрексат, который применяется при непереносимости азатиоприна или для ускорения лечебного эффекта. Внутрь или внутримышечно по 30 мг в неделю. Эффект наступает через 2-4 недели
Если отсутствует эффект от азатиоприна и 6-меркаптопурина, применяют препараты второй линии — это инфликсимаб и циклоспорин А.
При отсутствии эффекта от второго введения инфликсимаба и 7-дневного курса циклоспорина А показано хирургическое лечение.
Противорецидивное лечение
После купирования острых воспалительных процессов, назначают противорецидивную терапию аминосалицилатами на срок до 6 месяцев. В случае успешного лечения и отсутствии клинических и эндоскопических признаков заболевания, терапию отменяют.
В случае нестабильного эффекта от противорецидивного лечения терапию продлевают дополнительно сроком на 6 месяцев.
При неэффективности монотерапии аминосалицилатами добовляют к лечению иммуносупрессоры (азатиоприн или 6-меркаптопурин) и гормоны.
Пациентам с язвенным колитом, получающих консервативную терапию, необходимо постоянное наблюдение врача, регулярное эндоскопическое исследование с биопсией.
Хирургическое лечение
По статистике хирургическое лечение показано больным в 11-22 % случаев. Единственным способом радикального хирургического лечения язвенного колита является колпроктэктомия, то есть удаление всей толстой кишки. Основными показаниями к хирургическому лечению являются:
- отсутствие эффекта от консервативного лечения;
- развитие осложнений язвенного колита (кровотечение, перфорация, рак, токсическая дилатация толстого кишечника).
Послеоперационные осложнения
Возникают у ослабленных пациентов на фоне тяжёлого течения заболевания:
- эвентрация (выпадение кишечника через дефект в брюшной стенке );
- несостоятельность швов кишечных стом;
- серозный перитонит (воспаление брюшины);
- полисерозит;
- абсцессы брюшной полости;
- пневмония.
Особенности лечения в зависимости от формы и течения
Левосторонний колит или проктит низкой активности: свечи и пена салофальк.
Колит умеренной активности или распространённый: салофальк в таблетках, глюкокортикоиды.
Тяжёлое течение: салофальк в таблетках, глюкокортикоиды, инфузионная терапия, препараты железа, переливание плазмы и эритроцитарной массы, колпроктэктомия (удаление всей толстой кишки с формированием постоянной илеостомы — отверстия в брюшной полости, к которому прикрепляют калоприёмник).
Фульминантный колит: лечение такое же как и при тяжёлом течении.
При несвоевременном хирургическом лечении в послеоперационном периоде присоединяются другие осложнения в 59-81 % случаев, а летальность составляет от 11 до 49 %. При хирургическом лечении до возникновения тяжёлых кишечных осложнений (перфорация, токсическая дилатация и т. д.) эти цифры снижаются до 8-12 % и 0,5-1,5 % соответственно.
Таким образом, правильная диагностика, рациональная консервативная терапия и своевременное хирургическое лечение помогают добиться хороших результатов. В таком случае прогноз благоприятный. Но, в связи с длительным периодом нетрудоспособности, многие пациенты нуждаются в медико-социальной экспертизе и оформлении инвалидности.
Источник
НЯК — некротизирующее рецидивирующее воспаление слизистой оболочки толстой и прямой кишки с их эрозивно-язвенным поражением и частым вовлечением в процесс ряда других органов (суставов, печени, кожи, глаз). Чаще встречается проктит, нежели тотальный колит, и в зависимости от выраженности и распространенности неспецифического некротизирующе- го воспаления выделяют легкую (в основном, проктит), средней тяжести (в основном проктосигмоидит) и тяжелую (в основном тотальный колит) формы; возможно острое течение болезни.
Эпидемиология. НЯК — весьма распространенная болезнь, в частности, в ряде стран Западной Европы и США. Болеют люди всех возрастных групп, но чаще молодые (30-40-летние).
Среди некоторых национальностей НЯК встречается особенно часто.
Так, среди евреев, проживающих в США, НЯК встречается в 4-5 раз чаще, чем среди представителей других национальностей.
Этиология неизвестна. Предполагаемая генетическая предрасположенность заболевания описана у монозиготных близнецов. С позиций клинициста больше всего импонирует предположение о вирусной природе НЯК, но доказательных подтверждений этой гипотезы пока не получено.
Патогенез. НЯК является результатом действия факторов среды, которые у людей с генетической предрасположенностью вызывают срыв регуляторных механизмов, сдерживающих иммунные реакции на кишечные бактерии. Вероятно, повреждающий агент (вирус, токсин, микроб) стимулирует иммунный ответ, сопровождающийся формированием аутоантител против кишечного эпителия.
Малая величина конкордантности по НЯК у монозиготных близнецов (6—14%), по сравнению с близнецовой конкордантностью при болезни Крона (44—50%) является самым сильным свидетельством того, что для патогенеза НЯК факторы местной среды более важны, чем генетические факторы.
Из всех факторов среды больше всего удивляет курение, которое препятствует развитию НЯК (а при болезни Крона оказывает вредоносный эффект).
У лиц, ранее куривших помногу, а затем бросивших, а также у всех бросивших курить, у некурящих и у курящих относительный риск развития язвенного колита составил соответственно 4,4, 2,5, 1,0 и 0,6, По-видимому, ингредиентом, вносящим наибольший вклад в эти закономерности, является никотин, но механизм остается неясным.
Было показано, что курение влияет на клеточный и гуморальный иммунитет, а также повышает образование слизи в толстой кишке; в то же время курение и никотин тормозят моторику толстой кишки.
Давнее представление о НЯК как об аутоиммунном заболевании в последнее время получило новое развитие благодаря сведениям, что комменсальная микрофлора и продукты ее жизнедеятельности служат в качестве аутоантигенов, и что язвенный колит развивается за счет потери толерантности к веществам нормальной кишечной флоры, которые обычно безвредны.
К наиболее воспроизводимым доказательствам неэпителиального аутоиммунитета при язвенном колите относятся: высокая частота (около 70%) обнаружения pANCA при язвенном колите и ещё более высокая частота распространения pANCA среди больных со слерозируюшим холангитом, с рефрактерным левосторонним язвенным колитом, а также развитие хронического воспаления сумки-калосборника после наложения тонкокишечно-сумочного анастомоза.
Не столь доказательно мнение о том, что pANCA является маркером генетической подверженности язвенному колиту.
Морфологические изменения. При НЯК вся слизистая оболочка выглядит изъязвленной, гиперемированной, обычно геморрагической («кровавые слезы»). При эндоскопии обнаруживается легкая контактная ранимость слизистой оболочки. В просвете кишки могут быть кровь и гной. Воспалительные реакции имеют диффузный характер, не оставляя здоровых интактных участков.
Патологические изменения никогда не сопровождаются утолщением стенок и сужением просвета кишки.
Классификация
НЯК обычно подразделяется клиницистами на острые (молниеносные) и хронические формы.
Последние могут быть рецидивирующими и непрерывно рецидивирующими.
По локализации процесса различают дистальные формы (проктиты и проктосигмоидиты); левосторонние, когда процесс захватывает вышележащие отделы толстой кишки, и тотальные формы, при которых поражена вся толстая кишка.
Последние отличаются наиболее тяжелым течением.
Кроме того, выделяется впервые выявленная хроническая форма НЯК (первично-хроническая форма), сопровождающаяся обострением каждые 2—4 мес.
Клиника. Главные проявления НЯК: кровянистая диарея и абдоминальные боли, часто сопровождающиеся лихорадкой и похуданием в более тяжелых случаях.
По тяжести течения НЯК выделяют легкие, средней тяжести и тяжелые формы.
При легком течении частота стула не более 4 раза в сут, он либо оформленный, либо кашицеобразный, с примесью крови, слизи.
Общее состояние таких больных не страдает. Отсутствуют лихорадка, потеря массы тела, нет анемии и поражения других органов и систем.
При эндоскопии обнаруживается контактная кровоточивость слизистой оболочки, нередко выраженный ее отек и гиперемия.
При средней степени тяжести стул до 8 раз в сут, не оформлен, со значительной примесью слизи, крови и гноя. Отмечаются боли в животе, чаще в области левой ее половины.
Отмечается фебрильная (до 38 °С) лихорадка, потеря массы тела до 10 кг за последние 1,5—2 мес, умеренная анемия (до 100 г/л), увеличенная СОЭ (до 30мм/ч).
При эндоскопии выявляются поверхностные язвы, псевдополипоз, выраженная контактная кровоточивость слизистой оболочки.
При тяжелом течении стул более 10 раз в сутки, может выделяться алая кровь или сгустки крови без кала, иногда выделяется кровянисто-тканевый детрит, слизь и гной в большом количестве.
Имеет место выраженная интоксикация, высокая лихорадка (38,5-39°С), потеря более 10 кг массы тела менее чем за месяц, обезвоживание, судороги.
При обследовании: анемия (содержание гемоглобина ниже 100 г/л), лейкоцитоз более (10-12)х10*9л, СОЭ – более 40-50 мм/ч, резкая гипопротеинемия, гипер-у-глобулинемия, изменение спектра белковых фракций.
При эндоскопии — еще более выраженные изменения слизистой оболочки, в просвете кишки много крови и гноя, число язв увеличивается.
При изолированных проктитах довольно часто встречаются запоры, а главной жалобой могут быть мучительные тенезмы.
Иногда кишечные симптомы бывают на заднем плане, и превалируют общие симптомы: повышение температуры тела, похудание и какой-либо из внекишечных симптомов.
Различают 2 группы осложнений: местные и общие.
Общие (системные) проявления НЯК в значительной мере отражают состояние иммунологической реактивности организма.
У лиц пожилого возраста системные проявления в 2 раза реже, а местные в 2 раза чаще, чем у больных в возрасте 20—40 лет.
К местным осложнениям относят кровотечения, токсическую дилатацию толстой кишки, перфорацию, полипоз, опухоль, стриктуры, свищи. Физикальные находки обычно неспецифичны: вздутие или напряжение при пальпации одного из отделов толстой кишки.
В легких случаях никаких объективных находок может вообще не быть. Внекишечные проявления включают артрит, изменения кожи, увеличение печени.
Лихорадка, тахикардия, постуральная гипотензия обычно сопровождают более тяжелые случаи.
Диагностика.
Обязательные лабораторные исследования.
Общий анализ крови (при отклонении от нормы исследования повторять 1 раз в 10 дней).
Однократно: калий, натрий крови; кальций крови, резус-фактор, копрограмма, кал на скрытую кровь, гистологическое исследование биоптата, цитологическое исследование биоптата, посев кала на бактериальную флору, общий анализ мочи.
Двукратно (в случае наличия патологических изменений при первом исследовании): холестерин крови, общий билирубин и фракции, общий белок и фракции, АсАТ, АлАТ, ЩФ, ГГТП, сывороточное железо.
Дополнительные лабораторные исследования: коагулограмма, гематокритное число, ретикулоциты, сывороточные иммуноглобулины, исследования на ВИЧ, кровь на маркеры гепатитов В и С.
Обязательные инструментальные исследования. Однократно: ректороманоскопия с биопсией слизистой оболочки прямой кишки.
Дополнительные инструментальные исследования.
Проводятся в зависимости от тяжести течения основной болезни, ее осложнений и сопутствующих заболеваний.
Однократно: УЗИ брюшной полости и малого таза, эндоскопическая ретроградная холангиопанкреатография, рентгенография брюшной полости. Обязательные консультации специалистов: хирурга, гинеколога.
Диагностические критерии:
1) клинические данные (понос толстокишечного типа);
2) данные ректоскопии и колоноскопии (при легких формах болезни слизистая оболочка кишки гиперемирована, отечна, гранулирована, легко ранима; сеть кровеносных сосудов исчезает; при колите средней тяжести присоединяется кровоточивость, появляются участки, покрытые гнойным экссудатом; в тяжелых случаях колита — язвы, псевдополипы, стриктуры; в биоптате толстой кишки отмечается обильная клеточная инфильтрация собственного слоя слизистой оболочки и уменьшение числа крипт);
3) рентгенологическая диагностика — уменьшение гаустрации толстой кишки, ниши и дефекты наполнения по контуру кишки, укорочение кишки, сужение просвета; этот метод исследования может вызвать обострение процесса;
4) повторные отрицательные бактериологические анализы в отношении дизентерии. Течение хроническое, рецидивирующее.
Лечение. Диета аналогична таковой при болезни Крона (см. выше).
Цель терапии при НЯК состоит в подавлении воспаления, купировании симптомов болезни, индукции ремиссии и предотвращении рецидивов.
Основу лекарственной терапии НЯК составляют препараты 5-аминосалициловой кислоты — сульфасалазин, месалазин (5-АСК), кортикостероиды, иммунодепрессанты.
Многочисленные клинические наблюдения показали что, сульфасалазин при его высокой эффективности нередко дает побочные реакции (20—40%), которые обусловлены входящим в его структуру сульфапиридином — носителем 5-аминосалициловой кислоты.
В толстой кишке сульфасалазин расщепляется бактериальными азоредуктазами с высвобождением месалазина (5-АСК), оказывающим местное противовоспалительное действие.
Месалазин подавляет выброс лейкотриена В4, блокируя липооксигеназный и циклооксигеназный пути метаболизма арахидоновой кислоты, подавляют синтез активных медиаторов воспаления, особенно лейкотриена В4, простагландинов, других лейкотриенов.
В настоящее время синтезированы различные формы 5-АСК без сульфапиридина с различными механизмами освобождения действующего вещества в кишечнике: салофальк, пентаса, мезакол, салозинал и другие таблетки месалазина.
Таблетированные препараты отличаются составом оболочки, их энтеросолюбильным покрытием, а также скоростью ее растворения в зависимости от рН пищеварительного тракта.
Эти свойства достигаются созданием для месалазина инертной капсулы, обеспечивающей замедленное освобождение активно действующего вещества в зависимости от рН среды и времени прошедшего с момента приема препарата и транзита его по кишечнику.
Таблетки салофалька с покрытием из эудрагита L начинают освобождать месалазин (25—30%) в терминальном отделе подвздошной кишки при рН > 6,0 и в толстой кишке (70—75%). Освобождение месалазина происходит медленно.
Пентаса состоит из микрогранул месалазина диаметром 0,7—1 мм, покрытых полупроницаемой этилцеллюлозной оболочкой, разлагаются в желудке на микрогранулы, покрытые микрокристаллической целлюлозой.
Эта структура таблетки способствует медленному равномерному поступлению микрогранул, начиная с двенадцатиперстной кишки по всему кишечнику — высвобождается 50% в тонкой кишке, 50% в толстой и не зависит от рН среды (от 1,5 до 7,5).
Таким образом, по сравнению с другими препаратами, содержащими месалазин, пентаса обладает более длительным действием активного вещества с постоянной концентрацией препарата в разных отделах пищеварительного тракта, поэтому пентаса более эффективна при БК тонкой кишки, что следует учитывать в клинической практике.
При терапии пентасой выраженность микробного обсеменения тонкой кишки, диарея, а также изменения рН химуса не влияют на концентрацию препарата в ЖКТ, степень абсорбции и скорость высвобождения месалазина.
Важно обеспечить достаточную концентрацию месалазана в местах воспаления, который проявляет свою активность при местном контакте со слизистой оболочкой кишечника пропорционально адекватной концентрации его в просвете кишечника.
Салофальк, пентасу, мезакол, тидокол, салозинал и другие препараты 5-АСК назначают в дозе 3—4 г/сут до достижения клинико-эндоскопической ремиссии.
В активную фазу БК необходимы более высокие дозы месалазина — 4,8 г пентаса, салофальк, что практически эквивалентно по эффективности глюкокортикостероидам.
Высокие дозы рекомендуется использовать не более 8-10 нед.
После стихания атаки обязательным условием для поддержания ремиссии считается длительный прием (1-2 года) 1,5—2 г/сут препарата — противорецидивная терапия.
Ректальные формы месалазина (салофальк, пентаса и др., суппозитории — 1 г) более эффективны по сравнению с клизмами с гидрокортизоном при лечении больных ЯК в форме проктита, обеспечивая более длительное воздействие активного вещества на воспаленную слизистую оболочку.
При левостороннем колите возможна комбинация таблеток месалазина со свечами и клизмами.
При отсутствии эффекта от применения 5-АСК, при тяжелых формах НЯК, а также при наличии внекишечных осложнений показано назначение ГКС. Кортикостероиды блокируют фосфолипазу А2, препятствуя образованию всех ее метаболитов, подавляют активность многочисленных цитокинов.
Препаратом выбора является преднизолон.
Средняя доза 40—60 мг (1 мг на 1 кг массы тела в сут), высокие дозы 70—100мг/сут или метипред.
После купирования основных симптомов тяжелой атаки дозу снижают постепенно, по 10 мг каждую неделю. При дозе 30—40 мг в схему лечения включают пентасу, салофальк — 3 г/сут.
Мощный лечебный эффект от применения стероидов нередко вызывает серьезные побочные эффекты — гликемию, остопороз, повышение АД и др.
Для ограничения системной активности преднизолона применяют местнодействующие гормоны — будесонид (буденофальк), который имеет высокое сродство к глюкокортикоидным рецепторам и минимальное системное действие, так как достигает общего кровотока лишь в количестве 15%.
Оптимальная терапевтическая доза будесонида (буденофалька) 9 мг/сут.
В случаях стероидорезистентности и стероидозависимости используют азатиоприн и 6-мер-каптопурин (6-МП) в виде монотерапии или в сочетании с кортикостероидами.
Азатиоприн и его активный метаболит действуют на лимфоциты и моноциты, оказывая иммуносупрессивный эффект на синтез медиаторов воспаления. Доза азатиоприна 2 мг/кг/сут, улучшение отмечается не ранее чем через 3—4 нед, продолжительность лечения 4—6 мес.
Обладает побочными реакциями: тошнота, рвота, диарея, лейкопения и др.
Прогресс в изучении патогенеза НЯК способствует созданию и внедрению нового препарата ифликсимаб, воздействующего на иммунную систему и воспалительный процесс.
Инфликсимаб блокирует фактора некроза опухоли – альфа, ингибирует гранулематозное воспаление и может быть использован при лечении обострения НЯК.
Необходимость хирургического лечения возникает при осложнениях (свищи, стенозы, перфорации).
Прогноз — серьезный.
В течение 24 лет летальность составляет 39%.
Тяжелая форма болезни уже во время первого приступа дает 30% летальности.
Возникновение рака при НЯК зависит от распространенности и длительности колита.
Особенно высокий риск (30—40%) заболеть раком в случаях тотального поражения кишки с длительностью анамнеза больше 10 лет.
Источник
