Современная диагностика и лечение неспецифического язвенного колита
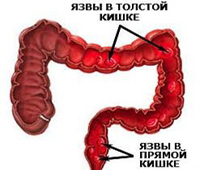
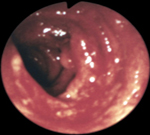
Неспецифический язвенный колит – это диффузное язвенно-воспалительное поражение слизистой оболочки толстого кишечника, сопровождающееся развитием тяжелых местных и системных осложнений. Клиника заболевания характеризуется схваткообразными болями в животе, диареей с примесью крови, кишечным кровотечением, внекишечными проявлениями. Язвенный колит диагностируется по результатам колоноскопии, ирригоскопии, КТ, эндоскопической биопсии. Лечение может быть консервативным (диета, физиотерапия, медикаменты) и хирургическим (резекция пораженного участка толстой кишки).
Общие сведения
Неспецифический язвенный колит (НЯК) – разновидность хронического воспалительного заболевания толстого кишечника неясной этиологии. Характеризуется склонностью к изъязвлению слизистой. Патология протекает циклически, обострения сменяются ремиссиями. Наиболее характерные клинические признаки – диарея с прожилками крови, боль в животе спастического характера. Длительно существующий неспецифический язвенный колит повышает риск возникновения злокачественных образований в толстом кишечнике.
Заболеваемость составляет порядка 50-80 случаев на 100 тысяч населения. При этом ежегодно выявляется 3-15 новых случаев заболевания на каждых 100 тыс. жителей. К развитию данной патологии женщины более склонны, чем мужчины, у них НЯК встречается на 30% чаще. Для неспецифического язвенного колита характерно первичное выявление в двух возрастных группах: у молодых людей (15-25 лет) и лиц старшего возраста (55-65 лет). Но помимо этого, заболевание может возникнуть и в любом другом возрасте. В отличии от болезни Крона, при язвенном колите страдает слизистая оболочка только толстой ободочной и прямой кишки.

Неспецифический язвенный колит
Причины
В настоящее время этиология неспецифического язвенного колита неизвестна. По предположениям исследователей в сфере современной проктологии, в патогенезе данного заболевания могут играть роль иммунные и генетически обусловленные факторы. Одна из теорий возникновения неспецифического язвенного колита предполагает, что причиной могут служить вирусы или бактерии, активизирующие иммунную систему, либо аутоиммунные нарушения (сенсибилизация иммунитета против собственных клеток).
Кроме того, отмечено, что неспецифический язвенный колит чаще встречается у людей, близкие родственники которых страдают этим заболеванием. В настоящее время также выявлены гены, которые вероятно могут отвечать за наследственную предрасположенность к язвенному колиту.
Классификация
Неспецифический язвенный колит различают по локализации и распространенности процесса. Левосторонний колит характеризуется поражением нисходящей ободочной и сигмовидной кишки, проктит проявляется воспалением в прямой кишке, при тотальном колите поражен весь толстый кишечник.
Симптомы НЯК
Как правило, течение неспецифического язвенного колита волнообразное, периоды ремиссии сменяются обострениями. В момент обострения язвенный колит проявляется различной симптоматикой в зависимости от локализации воспалительного процесса в кишечнике и интенсивности патологического процесса. При преимущественном поражении прямой кишки (язвенном проктите) могут отмечаться кровотечения из заднего прохода, болезненные тенезмы, боли в низу живота.  Иногда кровотечения являются единственным клиническим проявлением проктита.
Иногда кровотечения являются единственным клиническим проявлением проктита.
При левостороннем язвенном колите, когда поражена нисходящая ободочная кишка, обычно возникает диарея, каловые массы содержат кровь. Боли в животе могут быть довольно выраженные, схваткообразные, преимущественно в левой стороне и (при сигмоидите) в левой подвздошной области. Снижение аппетита, продолжительная диарея и нарушение пищеварения часто приводят к снижению массы тела.
Тотальный колит проявляется интенсивными болями в животе, постоянной обильной диареей, выраженным кровотечением. Тотальный язвенный колит является опасным для жизни состоянием, поскольку грозит развитием обезвоживания, коллапсами вследствие значительного падения артериального давления, геморрагическим и ортостатическим шоком.
Особенно опасна молниеносная (фульминантная) форма неспецифического язвенного колита, которая чревата развитием тяжелых осложнений вплоть до разрыва стенки толстой кишки. Одним из распространенных осложнений при таком течении заболевания является токсическое увеличение толстой кишки (мегаколон). Предполагается, что возникновение этого состояния связано с блокадой рецепторов гладкой мускулатуры кишечника избытком оксида азота, что вызывает тотальное расслабление мышечного слоя толстого кишечника.
В 10-20% случаев у больных неспецифическим язвенным колитом отмечаются внекишечные проявления: дерматологические патологии (гангренозная пиодермия, узловатая эритема), стоматиты, воспалительные заболевания глаз (ирит, иридоциклит, увеит, склерит и эписклерит), заболевания суставов (артриты, сакроилеит, спондилит), поражения желчевыводящей системы (склерозирующий холангит), остеомаляция (размягчение костей) и остеопороз, васкулиты (воспаления сосудов), миозиты и гломерулонефрит.
Осложнения
Довольно распространенным и серьезным осложнением неспецифического язвенного колита является токсический мегаколон – расширение толстой кишки в результате паралича мускулатуры стенки кишечника на пораженном участке. При токсическом мегаколоне отмечают интенсивные боли и вздутие в животе, повышение температуры тела, слабость.
Кроме того, неспецифический язвенный колит может осложняться массированным кишечным кровотечением, разрывом кишечника, сужением просвета толстой кишки, обезвоживанием в результате большой потери жидкости с диареей и раком толстого кишечника.
Диагностика
Основным диагностическим методом, выявляющим неспецифический язвенный колит, является колоноскопия, позволяющая детально исследовать просвет толстого кишечника и его внутренние стенки. Ирригоскопия и рентгенологическое исследование с барием позволяет обнаружить язвенные дефекты стенок, изменения размеров кишечника (мегаколон), нарушение перистальтики, сужение просвета. Эффективным методом визуализации кишечника является компьютерная томография.
Кроме того, производят копрограмму, тест на скрытую кровь, бактериологический посев. Анализ крови при язвенном колите показывает картину неспецифического воспаления. Биохимические показатели могут сигнализировать о наличии сопутствующих патологий, расстройств пищеварения, функциональных нарушений в работе органов и систем. Во время проведения колоноскопии обычно производят биопсию измененного участка стенки толстой кишки для гистологического исследования.
Лечение НЯК
 Поскольку причины, вызывающие неспецифический язвенный колит, до конца не выяснены, задачи терапии данного заболевания – это снижение интенсивности воспалительного процесса, стихание клинической симптоматики и профилактика обострений и осложнений. При своевременном правильном лечении и строгом следовании рекомендациям врача-проктолога, возможно добиться стойкой ремиссии и улучшения качества жизни пациента.
Поскольку причины, вызывающие неспецифический язвенный колит, до конца не выяснены, задачи терапии данного заболевания – это снижение интенсивности воспалительного процесса, стихание клинической симптоматики и профилактика обострений и осложнений. При своевременном правильном лечении и строгом следовании рекомендациям врача-проктолога, возможно добиться стойкой ремиссии и улучшения качества жизни пациента.
Лечение язвенного колита производят терапевтическими и хирургическими методами в зависимости от течения заболевания и состояния больного. Одним из немаловажных элементов симптоматической терапии неспецифического язвенного колита является диетическое питание.
При тяжелом течении заболевания в разгар клинических проявлений проктолог может порекомендовать полный отказ от приема пищи, ограничившись употреблением воды. Чаще всего больные при обострении теряют аппетит и переносят запрет довольно легко. В случае необходимости назначается парентеральное питание. Иногда больных переводят на парентеральное питание с целью более быстрого облегчения состояния при тяжело протекающем колите. Прием пищи возобновляют сразу после того, как аппетит восстанавливается.
Рекомендации по диете при язвенном колите направлены на прекращение диареи и снижение раздражение компонентами пищи слизистой оболочки кишечника. Из пищевого рациона удаляются продукты, содержащие пищевые волокна, клетчатку, острые, кислые блюда, алкогольные напитки, грубая пища. Кроме того, пациентам, страдающим хроническими воспалениями кишечника, рекомендовано повышение содержания в рационе белка (из расчета 1,5-2 грамма на килограмм тела в сутки).
Медикаментозная терапия неспецифического язвенного колита включает противовоспалительные средства, иммунодепрессанты (азатиоприн, метотрексат, циклоспорин, меркаптопурин) и антицитокины (инфликсимаб). Помимо этого, назначаются симптоматические средства: противодиарейные, обезболивающие, препараты железа при имеющих место признаках анемии.
В качестве противовоспалительных препаратов при данной патологии применяют нестероидные противовоспалительные средства – производные 5-аминосалициловой кислоты (сульфасалазин, месалазин) и кортикостероидные гормональные препараты. Кортикостероидные препараты применяют в период выраженного обострения в случае тяжелого и среднетяжелого течения (либо при неэффективности 5-аминосалицилатов) и не назначают более чем на несколько месяцев.
Детям кортикостероидные гормоны назначают с особой осторожностью. Противовоспалительная гормонотерапия может вызвать ряд тяжелых побочных эффектов: артериальную гипертензию, глюкоземию, остеопороз и др. Из физиотерапевтических методов лечения при язвенном колите может применяться диадинамотерапия, СМТ, интерференцтерапия и др.
Показаниями к хирургическому лечению является неэффективность диеты и консервативной терапии, развитие осложнений (массированного кровотечения, перфорации толстой кишки, при подозрение на возникновение злокачественного новообразования и т. д.). Резекция толстого кишечника с последующим созданием илеоректального анастомоза (соединения свободного конца подвздошной кишки с анальным каналом) является наиболее распространенной хирургической методикой лечения неспецифического язвенного колита. В некоторых случаях удалению подвергается ограниченный в пределах здоровых тканей участок пораженного кишечника (сегментарная резекция).
Прогноз и профилактика
Профилактики неспецифического язвенного колита на данный момент нет, поскольку причины, вызывающие это заболевание, до конца не ясны. Профилактическими мерами возникновения рецидивов обострения является соблюдение предписаний врача по образу жизни (рекомендации по питанию, аналогичные таковым при болезни Крона, снижение количества стрессовых ситуаций и физического перенапряжения, психотерапия) и регулярное диспансерное наблюдение. Неплохой эффект в плане стабилизации состояния дает санаторно-курортное лечение.
При нетяжелом течении без осложнения прогноз благоприятный. Порядка 80% пациентов, принимающих 5-ацетилсалицилаты в качестве поддерживающие терапии, не отмечают рецидивов и осложнений заболевания на протяжении года. У больных обычно происходят рецидивы 1 раз в пять лет, в 4% обострения отсутствуют в течение 15-ти лет. К хирургическому лечению прибегают в 20% случаев. Вероятность развития злокачественной опухоли у больных НЯК колеблется в пределах 3-10% случаев.
Источник
НЯК — некротизирующее рецидивирующее воспаление слизистой оболочки толстой и прямой кишки с их эрозивно-язвенным поражением и частым вовлечением в процесс ряда других органов (суставов, печени, кожи, глаз). Чаще встречается проктит, нежели тотальный колит, и в зависимости от выраженности и распространенности неспецифического некротизирующе- го воспаления выделяют легкую (в основном, проктит), средней тяжести (в основном проктосигмоидит) и тяжелую (в основном тотальный колит) формы; возможно острое течение болезни.
Эпидемиология. НЯК — весьма распространенная болезнь, в частности, в ряде стран Западной Европы и США. Болеют люди всех возрастных групп, но чаще молодые (30-40-летние).
Среди некоторых национальностей НЯК встречается особенно часто.
Так, среди евреев, проживающих в США, НЯК встречается в 4-5 раз чаще, чем среди представителей других национальностей.
Этиология неизвестна. Предполагаемая генетическая предрасположенность заболевания описана у монозиготных близнецов. С позиций клинициста больше всего импонирует предположение о вирусной природе НЯК, но доказательных подтверждений этой гипотезы пока не получено.
Патогенез. НЯК является результатом действия факторов среды, которые у людей с генетической предрасположенностью вызывают срыв регуляторных механизмов, сдерживающих иммунные реакции на кишечные бактерии. Вероятно, повреждающий агент (вирус, токсин, микроб) стимулирует иммунный ответ, сопровождающийся формированием аутоантител против кишечного эпителия.
Малая величина конкордантности по НЯК у монозиготных близнецов (6—14%), по сравнению с близнецовой конкордантностью при болезни Крона (44—50%) является самым сильным свидетельством того, что для патогенеза НЯК факторы местной среды более важны, чем генетические факторы.
Из всех факторов среды больше всего удивляет курение, которое препятствует развитию НЯК (а при болезни Крона оказывает вредоносный эффект).
У лиц, ранее куривших помногу, а затем бросивших, а также у всех бросивших курить, у некурящих и у курящих относительный риск развития язвенного колита составил соответственно 4,4, 2,5, 1,0 и 0,6, По-видимому, ингредиентом, вносящим наибольший вклад в эти закономерности, является никотин, но механизм остается неясным.
Было показано, что курение влияет на клеточный и гуморальный иммунитет, а также повышает образование слизи в толстой кишке; в то же время курение и никотин тормозят моторику толстой кишки.
Давнее представление о НЯК как об аутоиммунном заболевании в последнее время получило новое развитие благодаря сведениям, что комменсальная микрофлора и продукты ее жизнедеятельности служат в качестве аутоантигенов, и что язвенный колит развивается за счет потери толерантности к веществам нормальной кишечной флоры, которые обычно безвредны.
К наиболее воспроизводимым доказательствам неэпителиального аутоиммунитета при язвенном колите относятся: высокая частота (около 70%) обнаружения pANCA при язвенном колите и ещё более высокая частота распространения pANCA среди больных со слерозируюшим холангитом, с рефрактерным левосторонним язвенным колитом, а также развитие хронического воспаления сумки-калосборника после наложения тонкокишечно-сумочного анастомоза.
Не столь доказательно мнение о том, что pANCA является маркером генетической подверженности язвенному колиту.
Морфологические изменения. При НЯК вся слизистая оболочка выглядит изъязвленной, гиперемированной, обычно геморрагической («кровавые слезы»). При эндоскопии обнаруживается легкая контактная ранимость слизистой оболочки. В просвете кишки могут быть кровь и гной. Воспалительные реакции имеют диффузный характер, не оставляя здоровых интактных участков.
Патологические изменения никогда не сопровождаются утолщением стенок и сужением просвета кишки.
Классификация
НЯК обычно подразделяется клиницистами на острые (молниеносные) и хронические формы.
Последние могут быть рецидивирующими и непрерывно рецидивирующими.
По локализации процесса различают дистальные формы (проктиты и проктосигмоидиты); левосторонние, когда процесс захватывает вышележащие отделы толстой кишки, и тотальные формы, при которых поражена вся толстая кишка.
Последние отличаются наиболее тяжелым течением.
Кроме того, выделяется впервые выявленная хроническая форма НЯК (первично-хроническая форма), сопровождающаяся обострением каждые 2—4 мес.
Клиника. Главные проявления НЯК: кровянистая диарея и абдоминальные боли, часто сопровождающиеся лихорадкой и похуданием в более тяжелых случаях.
По тяжести течения НЯК выделяют легкие, средней тяжести и тяжелые формы.
При легком течении частота стула не более 4 раза в сут, он либо оформленный, либо кашицеобразный, с примесью крови, слизи.
Общее состояние таких больных не страдает. Отсутствуют лихорадка, потеря массы тела, нет анемии и поражения других органов и систем.
При эндоскопии обнаруживается контактная кровоточивость слизистой оболочки, нередко выраженный ее отек и гиперемия.
При средней степени тяжести стул до 8 раз в сут, не оформлен, со значительной примесью слизи, крови и гноя. Отмечаются боли в животе, чаще в области левой ее половины.
Отмечается фебрильная (до 38 °С) лихорадка, потеря массы тела до 10 кг за последние 1,5—2 мес, умеренная анемия (до 100 г/л), увеличенная СОЭ (до 30мм/ч).
При эндоскопии выявляются поверхностные язвы, псевдополипоз, выраженная контактная кровоточивость слизистой оболочки.
При тяжелом течении стул более 10 раз в сутки, может выделяться алая кровь или сгустки крови без кала, иногда выделяется кровянисто-тканевый детрит, слизь и гной в большом количестве.
Имеет место выраженная интоксикация, высокая лихорадка (38,5-39°С), потеря более 10 кг массы тела менее чем за месяц, обезвоживание, судороги.
При обследовании: анемия (содержание гемоглобина ниже 100 г/л), лейкоцитоз более (10-12)х10*9л, СОЭ – более 40-50 мм/ч, резкая гипопротеинемия, гипер-у-глобулинемия, изменение спектра белковых фракций.
При эндоскопии — еще более выраженные изменения слизистой оболочки, в просвете кишки много крови и гноя, число язв увеличивается.
При изолированных проктитах довольно часто встречаются запоры, а главной жалобой могут быть мучительные тенезмы.
Иногда кишечные симптомы бывают на заднем плане, и превалируют общие симптомы: повышение температуры тела, похудание и какой-либо из внекишечных симптомов.
Различают 2 группы осложнений: местные и общие.
Общие (системные) проявления НЯК в значительной мере отражают состояние иммунологической реактивности организма.
У лиц пожилого возраста системные проявления в 2 раза реже, а местные в 2 раза чаще, чем у больных в возрасте 20—40 лет.
К местным осложнениям относят кровотечения, токсическую дилатацию толстой кишки, перфорацию, полипоз, опухоль, стриктуры, свищи. Физикальные находки обычно неспецифичны: вздутие или напряжение при пальпации одного из отделов толстой кишки.
В легких случаях никаких объективных находок может вообще не быть. Внекишечные проявления включают артрит, изменения кожи, увеличение печени.
Лихорадка, тахикардия, постуральная гипотензия обычно сопровождают более тяжелые случаи.
Диагностика.
Обязательные лабораторные исследования.
Общий анализ крови (при отклонении от нормы исследования повторять 1 раз в 10 дней).
Однократно: калий, натрий крови; кальций крови, резус-фактор, копрограмма, кал на скрытую кровь, гистологическое исследование биоптата, цитологическое исследование биоптата, посев кала на бактериальную флору, общий анализ мочи.
Двукратно (в случае наличия патологических изменений при первом исследовании): холестерин крови, общий билирубин и фракции, общий белок и фракции, АсАТ, АлАТ, ЩФ, ГГТП, сывороточное железо.
Дополнительные лабораторные исследования: коагулограмма, гематокритное число, ретикулоциты, сывороточные иммуноглобулины, исследования на ВИЧ, кровь на маркеры гепатитов В и С.
Обязательные инструментальные исследования. Однократно: ректороманоскопия с биопсией слизистой оболочки прямой кишки.
Дополнительные инструментальные исследования.
Проводятся в зависимости от тяжести течения основной болезни, ее осложнений и сопутствующих заболеваний.
Однократно: УЗИ брюшной полости и малого таза, эндоскопическая ретроградная холангиопанкреатография, рентгенография брюшной полости. Обязательные консультации специалистов: хирурга, гинеколога.
Диагностические критерии:
1) клинические данные (понос толстокишечного типа);
2) данные ректоскопии и колоноскопии (при легких формах болезни слизистая оболочка кишки гиперемирована, отечна, гранулирована, легко ранима; сеть кровеносных сосудов исчезает; при колите средней тяжести присоединяется кровоточивость, появляются участки, покрытые гнойным экссудатом; в тяжелых случаях колита — язвы, псевдополипы, стриктуры; в биоптате толстой кишки отмечается обильная клеточная инфильтрация собственного слоя слизистой оболочки и уменьшение числа крипт);
3) рентгенологическая диагностика — уменьшение гаустрации толстой кишки, ниши и дефекты наполнения по контуру кишки, укорочение кишки, сужение просвета; этот метод исследования может вызвать обострение процесса;
4) повторные отрицательные бактериологические анализы в отношении дизентерии. Течение хроническое, рецидивирующее.
Лечение. Диета аналогична таковой при болезни Крона (см. выше).
Цель терапии при НЯК состоит в подавлении воспаления, купировании симптомов болезни, индукции ремиссии и предотвращении рецидивов.
Основу лекарственной терапии НЯК составляют препараты 5-аминосалициловой кислоты — сульфасалазин, месалазин (5-АСК), кортикостероиды, иммунодепрессанты.
Многочисленные клинические наблюдения показали что, сульфасалазин при его высокой эффективности нередко дает побочные реакции (20—40%), которые обусловлены входящим в его структуру сульфапиридином — носителем 5-аминосалициловой кислоты.
В толстой кишке сульфасалазин расщепляется бактериальными азоредуктазами с высвобождением месалазина (5-АСК), оказывающим местное противовоспалительное действие.
Месалазин подавляет выброс лейкотриена В4, блокируя липооксигеназный и циклооксигеназный пути метаболизма арахидоновой кислоты, подавляют синтез активных медиаторов воспаления, особенно лейкотриена В4, простагландинов, других лейкотриенов.
В настоящее время синтезированы различные формы 5-АСК без сульфапиридина с различными механизмами освобождения действующего вещества в кишечнике: салофальк, пентаса, мезакол, салозинал и другие таблетки месалазина.
Таблетированные препараты отличаются составом оболочки, их энтеросолюбильным покрытием, а также скоростью ее растворения в зависимости от рН пищеварительного тракта.
Эти свойства достигаются созданием для месалазина инертной капсулы, обеспечивающей замедленное освобождение активно действующего вещества в зависимости от рН среды и времени прошедшего с момента приема препарата и транзита его по кишечнику.
Таблетки салофалька с покрытием из эудрагита L начинают освобождать месалазин (25—30%) в терминальном отделе подвздошной кишки при рН > 6,0 и в толстой кишке (70—75%). Освобождение месалазина происходит медленно.
Пентаса состоит из микрогранул месалазина диаметром 0,7—1 мм, покрытых полупроницаемой этилцеллюлозной оболочкой, разлагаются в желудке на микрогранулы, покрытые микрокристаллической целлюлозой.
Эта структура таблетки способствует медленному равномерному поступлению микрогранул, начиная с двенадцатиперстной кишки по всему кишечнику — высвобождается 50% в тонкой кишке, 50% в толстой и не зависит от рН среды (от 1,5 до 7,5).
Таким образом, по сравнению с другими препаратами, содержащими месалазин, пентаса обладает более длительным действием активного вещества с постоянной концентрацией препарата в разных отделах пищеварительного тракта, поэтому пентаса более эффективна при БК тонкой кишки, что следует учитывать в клинической практике.
При терапии пентасой выраженность микробного обсеменения тонкой кишки, диарея, а также изменения рН химуса не влияют на концентрацию препарата в ЖКТ, степень абсорбции и скорость высвобождения месалазина.
Важно обеспечить достаточную концентрацию месалазана в местах воспаления, который проявляет свою активность при местном контакте со слизистой оболочкой кишечника пропорционально адекватной концентрации его в просвете кишечника.
Салофальк, пентасу, мезакол, тидокол, салозинал и другие препараты 5-АСК назначают в дозе 3—4 г/сут до достижения клинико-эндоскопической ремиссии.
В активную фазу БК необходимы более высокие дозы месалазина — 4,8 г пентаса, салофальк, что практически эквивалентно по эффективности глюкокортикостероидам.
Высокие дозы рекомендуется использовать не более 8-10 нед.
После стихания атаки обязательным условием для поддержания ремиссии считается длительный прием (1-2 года) 1,5—2 г/сут препарата — противорецидивная терапия.
Ректальные формы месалазина (салофальк, пентаса и др., суппозитории — 1 г) более эффективны по сравнению с клизмами с гидрокортизоном при лечении больных ЯК в форме проктита, обеспечивая более длительное воздействие активного вещества на воспаленную слизистую оболочку.
При левостороннем колите возможна комбинация таблеток месалазина со свечами и клизмами.
При отсутствии эффекта от применения 5-АСК, при тяжелых формах НЯК, а также при наличии внекишечных осложнений показано назначение ГКС. Кортикостероиды блокируют фосфолипазу А2, препятствуя образованию всех ее метаболитов, подавляют активность многочисленных цитокинов.
Препаратом выбора является преднизолон.
Средняя доза 40—60 мг (1 мг на 1 кг массы тела в сут), высокие дозы 70—100мг/сут или метипред.
После купирования основных симптомов тяжелой атаки дозу снижают постепенно, по 10 мг каждую неделю. При дозе 30—40 мг в схему лечения включают пентасу, салофальк — 3 г/сут.
Мощный лечебный эффект от применения стероидов нередко вызывает серьезные побочные эффекты — гликемию, остопороз, повышение АД и др.
Для ограничения системной активности преднизолона применяют местнодействующие гормоны — будесонид (буденофальк), который имеет высокое сродство к глюкокортикоидным рецепторам и минимальное системное действие, так как достигает общего кровотока лишь в количестве 15%.
Оптимальная терапевтическая доза будесонида (буденофалька) 9 мг/сут.
В случаях стероидорезистентности и стероидозависимости используют азатиоприн и 6-мер-каптопурин (6-МП) в виде монотерапии или в сочетании с кортикостероидами.
Азатиоприн и его активный метаболит действуют на лимфоциты и моноциты, оказывая иммуносупрессивный эффект на синтез медиаторов воспаления. Доза азатиоприна 2 мг/кг/сут, улучшение отмечается не ранее чем через 3—4 нед, продолжительность лечения 4—6 мес.
Обладает побочными реакциями: тошнота, рвота, диарея, лейкопения и др.
Прогресс в изучении патогенеза НЯК способствует созданию и внедрению нового препарата ифликсимаб, воздействующего на иммунную систему и воспалительный процесс.
Инфликсимаб блокирует фактора некроза опухоли – альфа, ингибирует гранулематозное воспаление и может быть использован при лечении обострения НЯК.
Необходимость хирургического лечения возникает при осложнениях (свищи, стенозы, перфорации).
Прогноз — серьезный.
В течение 24 лет летальность составляет 39%.
Тяжелая форма болезни уже во время первого приступа дает 30% летальности.
Возникновение рака при НЯК зависит от распространенности и длительности колита.
Особенно высокий риск (30—40%) заболеть раком в случаях тотального поражения кишки с длительностью анамнеза больше 10 лет.
Источник
