Синдром эндогенной интоксикации на фоне лямблиоза и кандидоза

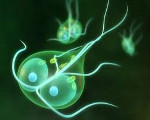
Лямблиоз – протозойная инвазия, вызываемая кишечной лямблией и протекающая с признаками функционального расстройства пищеварения. Ведущим в клинике лямблиоза выступает гастроинтестинальный синдром (тошнота, боли в животе, неустойчивый стул, метеоризм); также могут развиваться интоксикационный, аллергический, астено-невротический, гепатолиенальный синдромы. Для лабораторного подтверждения лямблиоза проводится микроскопическое исследование кала и дуоденального содержимого, ИФА, ПЦР, анализ биопсийного материала. С целью специфической терапии при лямблиозе назначаются антипротозойные препараты (метронидазол, тинидазол, орнидазол и др.); дополнительно – желчегонные препараты, ферменты, энтеросорбенты.
Общие сведения
Лямблиоз – кишечная инфекция, вызываемая патогенными простейшими – лямблиями, обитающими в просвете тонкой кишки. Возбудителя инфекции впервые описал русский врач Д.Ф. Лямбль в 1859 г., именем которого был назван и сам паразит, и вызываемое им заболевание – лямблиоз. Однако в западных странах принято считать, что первенство открытия возбудителя протозойной инфекции принадлежит французскому исследователю А.Жиарду, отчего в международной нозологической классификации принято другое название заболевания – жиардиаз или гиардиаз (giardiasis). Лямблиоз распространен повсеместно: инвазированность лямблиями взрослого населения развитых стран составляет 3-5%, развивающихся стран – 10-15%; детей в организованных коллективах – 30-40%. Лямблиоз у детей и взрослых изучается в рамках педиатрии, гастроэнтерологии, паразитологии.

Лямблиоз
Причины лямблиоза
С точки зрения морфологии, лямблии (Lamblia intestinalis, Giardia intestinalis или Giardia lamblia) представляют собой микроскопических одноклеточных паразитов, относящихся к типу простейших, классу жгутиковых. В кишечнике лямблии могут паразитировать в вегетативной (в виде трофозоитов) и споровой (в виде цист) форме. Трофозоиты имеют грушевидную форму, длину 18-21 мкм и ширину 5-15 мкм, оболочку и присасывательный диск. Питание лямблий осуществляется осмотическим путем, за счет всасывания продуктов пристеночного пищеварения всей поверхностью тела. Благодаря имеющимся четырем парам жгутиков трофозоиты способны совершать круговые или колебательные движения. Размножаются лямблии путем деления; каждые 10-12 часов паразиты способны удваиваться. Местом обитания вегетативных форм лямблий служат верхние отделы тонкой кишки. Цисты лямблий неподвижны; имеют овальную форму, двухконтурную капсулу; длину 8-14 мкм, ширину – 5-8 мкм. В форме цист лямблии существуют в толстой кишке и вне организма, во внешней среде, где могут длительно сохранять свою жизнеспособность.
Источником распространения возбудителей лямблиоза служит инвазированный человек, выделяющий зрелые цисты лямблий с фекалиями в окружающую среду. Не исключается эпидемиологическая роль животных, являющихся носителями лямблий (собак, кошек, морских свинок, кроликов и др.). Механическими переносчиками возбудителей могут являться мухи, тараканы и другие насекомые. Заражение лямблиозом происходит по фекально-оральному механизму; водным, пищевым, контактно-бытовым путями. Ведущими факторами передачи инфекции выступают некипяченая вода, продукты питания, руки, предметы общего пользования, почва, загрязненные цистами лямблий. Инвазированности населения лямблиозом способствует фекальное загрязнение окружающей среды, плохое состояние водоснабжения, скученность людей, низкий уровень санитарно-гигиенических навыков населения. Предрасполагающими моментами выступают возраст до 10 лет, гипотрофия и дистрофия, врожденные аномалии желчевыводящих путей, заболевания ЖКТ со снижением кислотности и ферментативной активности, перенесенная резекция желудка, белковое голодание и др. Всплеск заболеваемости лямблиозом регистрируется в весенне-летний сезон.
Патогенез
Попадая в пищеварительный тракт, цисты лямблий достигают 12-перстной кишки, где превращаются в вегетативные формы. Здесь, а также в проксимальном отделе тощей кишки лямблии прикрепляются к ворсинкам эпителия, вызывая механическое повреждение энтероцитов, раздражение нервных окончаний стенки тонкой кишки, нарушение процесса всасывания. Следствием этих процессов служит развитие воспаления ЖКТ (дуоденита, энтерита), синдрома мальабсорбции, вторичной ферментопатии, дисбактериоза, синдром хронической эндогенной интоксикации. Лямблиоз может способствовать хронизации гельминтозов и других кишечных инфекций (сальмонеллеза, дизентерии, иерсиниоза). Доказано, что в процессе жизнедеятельности лямблии выделяют токсин, обладающий тропностью к нервной ткани, что объясняет угнетающее действие на нервную систему. Вследствие сенсибилизации организма протозойными антигенами при лямблиозе могут развиваться различные аллергические проявления, особенно свойственные детям с лимфатико-гипопластическим диатезом.
Классификация
Лямблиоз может протекать в виде бессимптомного лямблионосительства (25%), субклинической (50%) и манифестной формы (25%). В зависимости от ведущих клинических проявлений манифестного лямблиоза различают:
- кишечную форму, включающую функциональное расстройство кишечника, дуоденит, дуодено-гастральный рефлюкс, гастроэнтерит, энтерит;
- билиарно-панкреатическую форму, протекающую с явлениями дискинезии желчевыводящих путей, холангита, холецистита, реактивного панкреатита;
- внекишечную форму, сопровождающуюся астено-невротическим синдромом, нейроциркуляторной дистонией, токсико-аллергическими проявлениями;
- смешанную фому.
Клинически выраженный лямблиоз может иметь острое и хроническое течение.
Симптомы лямблиоза
Симптоматика манифестной формы лямблиоза складывается из гастроинтестинального, интоксикационного, аллерго-дерматологического, астено-невротического, гепатолиенального синдромов. В типичных случаях период инкубации составляет 1-3 недели. Основные клинические проявления лямблиоза связаны с нарушением функционирования желудочно-кишечного тракта, поскольку местом паразитирования лямблий служит кишечник. В острой стадии преобладают жалобы на умеренные боли в околопупочной области и правом подреберье, тошноту, отрыжку, плохой аппетит, чувство тяжести в желудке, вздутие живота. Стул становится учащенным до 3-5 раз в сутки, жидким, пенистым, водянистым, а позднее – жирным; нередко поносы сменяются запорами. Острая фаза лямблиоза длится 5-7 дней; затем может наступить самопроизвольное излечение либо переход инфекции в подострое хроническое течение. При хроническом лямблиозе отмечаются похудание, астенизация, кратковременные обострения кишечных проявлений в виде гастродуоденита, еюнита, дискинезии 12-перстной кишки.
Синдром интоксикации при лямблиозе напрямую зависит от массивности инвазии, длительности и тяжести течения заболевания. Он может проявляться периферическим лимфаденитом, увеличением аденоидов, субфебрилитетом. Признаками угнетения ЦНС при лямблиозе служат раздражительность, быстрая утомляемость, снижение работоспособности, эмоциональная лабильность, бруксизм. У детей возможно появление тиков, гиперкинезов, гипотонических кризов и обморочных состояний. Дерматоаллергические проявления включают сухость и шелушение кожи, фолликулярный кератоз, крапивницу с кожным зудом, атопический дерматит и т. д. Пациенты с лямблиозом часто страдают упорным течением блефарита и конъюнктивита, хейлита; астматическим бронхитом и бронхиальной астмой.
Диагностика лямблиоза
Клиническое распознавание лямблиоза затруднено в виду большого разнообразия и неспецифичности симптоматики. Клинические проявления лямблиоза часто объясняются другими причинами, а больные лечатся у гастроэнтеролога, невролога, аллерголога, пульмонолога, дерматолога по поводу отдельных синдромов.
При объективном обследовании пациентов с лямблиозом выявляется бледность кожных покровов, обложенность языка, вздутие живота, увеличение печени, болезненность в мезогастрии. С помощью УЗИ гепатобилиарной системы и холецистографии выявляются дискинезии желчевыводящих путей с признаками холестаза. Изменения в гемограмме представлены эозинофилией, моноцитозом. В биохимическом анализе крови обнаруживается гипогаммаглобулинемия, гипоальбуминемия, повышение уровня щелочной фосфатазы. Исследование кала на дисбактериоз выявляет изменение микрофлоры кишечника: снижение количества лакто- и бифидобактерий, появление патогенных микроорганизмов (стафилококков и стрептококков, грибов Candida и др.).
Диагноз лямблиоза в обязательном порядке должен быть подтвержден данными паразитологического обследования, а именно обнаружением цист лямблий в кале или вегетативных форм в дуоденальном содержимом. С этой целью проводится микроскопическое исследование свежевыделенных фекалий и мазков (нативных и окрашенных), дуоденальное зондирование с последующим исследованием полученного секрета. Учитывая циклический характер выделения трофозоитов и цист с испражнениями, целесообразно проведение повторных исследований кала (3-5 раз в течение месяца). Для подтверждения лямблиоза также используется определение антигенов лямблий в фекалиях (ПЦР) или специфических антител в сыворотке крови (ИФА), исследование биопсийного материала, полученного при эндоскопии.
Лечение лямблиоза
Терапия лямблиоза проводится поэтапно и состоит из подготовительного периода (устранение холестаза, эндотоксикоза, механическое удаление лямблий), собственно антипаразитарного лечения (ликвидация трофозоитов и цист лямблий) и восстановительного периода (восстановление микрофлоры кишечника, укрепление иммунитета и пр.).
Подготовительный этап включает в себя рациональную диетотерапию, направленную на создание неблагоприятных условий для размножения лямблий в организме. Такая диета предполагает употребление каш, отрубей, овощей и фруктов, растительного масла; ограничение углеводов, главным образом, сахаров. Полезно проведение разгрузочных дней; тюбажей с минеральной водой, ксилитом, сорбитом; прием желчегонных и антигистаминных препаратов.
Медикаментозный этап лечения лямблиоза проводится специальными антипротозойными препаратами (метронидазол, тинидазол, орнидазол, ниморазол, албендазол, фуразолидон и др.) и обычно состоит из 2-х курсов. На заключительном, восстановительном этапе назначаются поливитаминные препараты, энтеросорбенты, бактерийные и ферментативные препараты, растительные адаптогены, иммуностимуляторы, фитотерапия.
Прогноз и профилактика
Эффективность терапии лямблиоза составляет 92-95%, однако в дальнейшем могут возникать рецидивы паразитарной инфекции или реинфицирование. Для полного освобождения от паразитов нередко требуется настойчивое повторное лечение. Диспансерное наблюдение пациентов проводится в течение 3-6 месяцев с 2-3-х кратным паразитологическим обследованием. Для предупреждения лямблиоза следует осуществлять охрану водоемов и почвы от загрязнения паразитами, контроль за качеством питьевой воды, санитарно-гигиеническое просвещение населения. С целью разрыва цепи передачи лямблиоза важно своевременное выявление бессимптомных носителей и больных лиц путем проведения копрологического обследования детей и персонала детских учреждений.
Источник
Синдром эндогенной интоксикации. Клиника синдрома эндогенной интоксикации.
В настоящее время одной из наиболее сложных проблем интенсивной терапии является синдром эндогенной интоксикации (СЭИ), сопровождающий значительное количество патологических состояний (шок, перитонит, панкреатит и др.), которые по мере своего развития могут приводить к летальному исходу.
Прогрессирование эндотоксикоза обусловлено накоплением в крови различных по происхождению, химической структуре и биологическому воздействию веществ, именуемых эндотоксинами. Эндотоксины способствуют развитию острой почечно-печеночной недостаточности, сердечно-сосудистой недостаточности, острого респираторного дистресс-синдрома, приводя в конечном итоге к появлению крайне тяжелого состояния – синдрома мультиорганной дисфункции.
Эндогенная интоксикация – клинический синдром, возникающий при различных по этиологии патологических состояниях, обусловленных накоплением в тканях и биологических жидкостях организма продуктов нарушенного обмена веществ, метаболитов, деструктивных клеточных и тканевых структур, разрушенных белковых молекул, pi сопровождающийся функциональными и морфологическими поражениями органов и систем организма.
Выделяют три основных звена, которые определяют тяжесть состояния больных и выраженность клинической симптоматики: токсемия, нарушение микроциркуляции, угнетение функций собственных детоксицирующих и защитных систем организма.
Основным звеном патогенеза синдрома эндогенной интоксикации является токсемия. К сожалению, четкая дифференциация токсических веществ эндогенного происхождения практически невозможна. Однако в каждом конкретном случае можно выделить “первичные” и “вторичные” эндотоксины. Так, при ожогах, синдроме длительного раздавливания, облитерирующих сосудистых заболеваниях “первичными” являются продукты белковой деградации, “вторичными” – продукты естественного метаболизма, накопление которых в организме является следствием угнетения функций естественной детоксикации и экскреции.
Эндотоксемия, нарушая тонус периферических сосудов, реологию крови, кинетические и механические свойства форменных элементов крови, приводит к тканевой гипоксии, которая является одним из важных звеньев патогенеза СЭИ, течение которого усугубляется снижением функции органов естественной детоксикации и экскреции. Токсины блокируют места связывания молекул альбумина, что ведет к снижению эффективности проводимого медикаментозного лечения, поскольку этот белок является транспортным агентом для многих фармакологических препаратов.
Клиника синдрома эндогенной интоксикации.
Сопоставление экспериментальных и клинических исследований позволило выявить следующие стадии развития синдрома эндогенной интоксикации.
I стадия синдрома эндогенной интоксикации. Реактивно-токсическая возникает в ответ на формирование первичного деструктивного очага или травматического повреждения. Лабораторными признаками этой стадии являются повышение в крови уровней молекул средней массы (МСМ), продуктов перекисного окисления липидов (ДК и МДА), возрастание ЛИИ.
II стадия синдрома эндогенной интоксикации – стадия выраженной токсемии развивается после прорыва гастогематического барьера, когда в циркулирующую кровь попадают эндотоксины, образовавшиеся в первичном очаге интоксикации, с последующим распространением и накоплением в организме. В зависимости от состояния организма, его резистентности и исходного уровня детоксицирующих и иммунных систем выделяют компенсированную и декомпенсированную стадии выраженной токсемии.
III стадия синдрома эндогенной интоксикации – мультиорганной дисфункции (СМОД) наблюдается при дальнейшем прогрессировашш патологического процесса как следствие тяжелого повреждения эндотоксинами различных органов и систем с развитием их функциональной декомпенсацш!. Клинически эта стадия Проявляется нарушением сознания, гипоксией, выраженной сердечной Недостаточностью, олигурией, паралитической непроходимостью кишечника. В крови определяется высокая концентрация креатинина, мочевины, билирубина.
– Также рекомендуем “Маркеры эндогенной интоксикации. Диагностика эндогеннной интоксикации.”
Оглавление темы “Синдром эндогенной интоксикации и сепсис.”:
1. Синдром эндогенной интоксикации. Клиника синдрома эндогенной интоксикации.
2. Маркеры эндогенной интоксикации. Диагностика эндогеннной интоксикации.
3. Лечение эндогенной интоксикации. Интенсивная терапия эндогеннной интоксикации.
4. Гемосорбция. Механизмы действия гемосорбции. Плазмоферез. Фильтрационный плазмоферез.
5. Энтеросорбция. Форсированный диурез. Перитонеальный диализ.
6. Непрямая электрохимическая детоксикация. Ультрафиолетовое облучение крови.
7. Сепсис и септический шок.
8. Мониторинг жизненно важных функций при сепсисе. Поддержание адекватного газообмена при сепсисе.
9. Инфузионная терапия при сепсисе.
10. Инотропная поддержка при сепсисе.
Источник
Синдром эндогенной интоксикации (эндотоксемия) – это накопление в крови и тканях организма эндотоксинов.
Эндотоксины – это вещества, которые оказывают отравляющее воздействие на организм. Они, в свою очередь, могут быть продуктами жизнедеятельности самого организма, либо могут попадать в него извне.
Синдром эндогенной интоксикации является одной из острейших проблем в интенсивной терапии, так как сопутствует большому количеству патологических состояний, среди которых: шок, панкреатит, перитонит и пр. Выраженный синдром эндогенной интоксикации способен приводить к гибели человека.
Содержание:
- Классификация эндотоксинов
- Симптомы синдрома эндогенной интоксикации
- Степени эндогенной интоксикации
- Диагностика синдрома эндогенной интоксикации
- Лечение синдрома эндогенной интоксикации
Причины синдрома эндогенной интоксикации

Причины синдрома эндогенной интоксикации могут быть самыми разнообразными. Тем не менее, этот процесс всегда развивается при поступлении эндотоксинов из мест их образования в кровоток. По крови эндотоксины распространяются в органы и системы органов, а также во все ткани организма. Когда количество агрессивных компонентов и эндотоксинов превышает естественные возможности организма в их биотрансформации, наступает синдром эндогенной интоксикации.
Различают следующие причины синдрома эндогенной интоксикации:
Болезни, протекающие с гнойно-воспалительной реакцией в организме. Сюда можно отнести холецистит, острую пневмонию, перитонит, панкреатит и пр.
Тяжелые и сложные травмы: краш-синдром.
Некоторые хронические болезни в стадии обострения, например, сахарный диабет, тиреотоксический зоб.
Отравления организма.
Первичные механизмы возникновения синдрома эндогенной интоксикации следующие:
Резорбционный механизм. При этом происходит рассасывание токсических веществ (некротических масс, воспалительного экссудата) из ограниченного очага инфекции по всему организму. Этот процесс может быть запущен при кишечной непроходимости, при абсцессах, при флегмоне мягких тканей и пр.
Обменный механизм развития синдрома эндогенной интоксикации. Он обуславливается чрезмерной выработкой токсических веществ. Этот механизм развития характерен для пневмонии, острого панкреатита, разлитого перитонита.
Ретенционный механизм. По такому типу синдром эндогенной интоксикации развивается в том случае, если страдает непосредственно сам процесс выведения токсинов из организма, то есть нарушается работа органов детоксикации.
Реперфузионный механизм. Проникновение эндотоксинов в кровь происходит из тканей, которые продолжительное время находились в состоянии ишемии, при этом антиоксидантный барьер организма утратил состоятельность. Это может происходить при шоковых состояниях, при проведении оперативного вмешательства с использованием АИК и пр.
Механизм вторичной токсической агрессии, при которой ткани отвечают токсической реакцией на воздействие эндотоксинов.
Инфекционный механизм, при котором в качестве эндотоксинов выступают патогенные микроорганизмы из очагов инвазивной инфекции.
Классификация эндотоксинов
Эндотоксины – это те вещества, которые приводят к формированию эндотоксемии и к синдрому эндогенной интоксикации.
Выделяют следующие эндотоксины, в зависимости от механизма их образования:
Ферменты, которые после активации тем или иным патологическим процессом, начинают повреждать ткани. Это могут быть протеолитические и лизосомные ферменты, а также продукты активации калликреин-кининовой системы.
Продукты естественной жизнедеятельности организма могут выступать в качестве эндотоксинов при условии накопления их в высоких концентрациях. Сюда можно отнести мочевину, билирубин и пр.
Все биологически активные вещества, которые имеются в организме человека. Это могут быть медиаторы воспаления, цитокины, простагландины и пр.
Агрессоры, которые возникают при распаде чужеродных антигенов и иммунных комплексов.
Токсины, выделяемые микробами или иными патологическими агентами.
Среднемолекулярные вещества (вирусы, аллергены, холестерин и пр.).
Продукты, которые возникают при перекисном окислении липидов.
Продукты, которые появляются в результате распада клеток при повреждении их мембран деструктивными процессами. Это могут быть белки, миоглобин, липазы, фенол и пр.
Высокие концентрации компонентов регуляторных систем.
Эндотоксины способны оказывать на организм прямое и опосредованное воздействие, они способны повлиять на микроциркуляцию, на процессы синтеза и метаболизма в тканях.
Симптомы синдрома эндогенной интоксикации

Одним из ведущих симптомов эндотоксемии является угнетение сознания. Возможна его полная потеря, либо частичное снижение. Параллельно у больного возникают выраженные головные боли, появляется мышечная слабость, характерна миалгия.
По мере прогрессирования интоксикации организма, присоединяется тошнота и рвота. Так как организм больного теряет жидкость, слизистые оболочки становятся сухими.
Развивается тахикардия или брадикардия. Температура тела может и повышаться, и, напротив, понижаться.
Так как эндогенная интоксикация часто возникает на фоне шокового состояния, то на первый план выходят симптомы эндотоксического шока. В крови при тяжелых состояниях человека однозначно будут присутствовать те или иные эндотоксины бактериальной природы, даже на фоне отсутствия бактериемии. Это не зависит от того, что спровоцировало синдром эндогенной интоксикации: травма, ожог, ишемия тканей и др. Важна лишь степень тяжести состояния человека.
Степени эндогенной интоксикации
Врачи различают три степени тяжести синдрома эндогенной интоксикации, для каждой из которых имеются свои критерии:
Первая степень эндотоксикацииРеакция организма возникает в ответ на формирование очага деструкции, либо на полученную травму:
|
Вторая степень эндотоксикацииДля второй степени эндогенной интоксикации характерно попадание в кровь эндотоксинов, которые поступают в нее из источника интоксикации. С током крови они распространяются по организму и накапливаются во всех тканях:
|
Третья степень эндотоксикацииЭта степень эндотоксикации характеризуется нарушением работы всех органов. Патологический процесс прогрессирует вплоть до развития функциональной мультиорганной дисфункции:
|
Диагностика синдрома эндогенной интоксикации

Диагностика синдрома эндогенной интоксикации выстраивается на основе оценки степени тяжести состояния человека по характерным симптомам (оттенок кожных покровов, частота дыхания и сердцебиения и пр.). Кроме того, необходимо проведение анализов крови.
Полученные результаты обрабатываются, и по ним будет наблюдаться изменение таких показателей как:
Значительное увеличение количества лейкоцитов в венозной крови.
Превышение лейкоцитарного и ядерного индекса интоксикации. Хотя иногда эти показатели могут быть заниженными, что свидетельствует о несостоятельности системы кроветворения и о детоксикации организма.
Увеличение индекса интоксикации. Если он превышает отметку в 45, то это однозначно указывает на неминуемый летальный исход.
Необходима оценка концентрации общего белка в плазме крови.
Увеличение уровня билирубина.
Увеличение уровня креатинина и мочевины.
Увеличение концентрации молочной кислоты.
Увеличение коэффициента клеток неспецифической защиты относительно клеток специфической защиты. О тяжелом состоянии больного говорит коэффициент, превышающий 2,0.
Наиболее чувствительным признаком эндотоксикации является увеличение уровня молекулы средней массы.
Лечение синдрома эндогенной интоксикации

Лечение синдрома эндогенной интоксикации предполагает удаление токсических компонентов из организма и из крови с первоначальным снижением их концентрации. Активную детоксикацию назначают при установлении 2 или 3 степени тяжести патологического синдрома.
Биологическая интоксикация всегда базируется на следующих механизмах:
Биологическая трансформация эндотоксических компонентов в печени. Для запуска данного механизма выполняют гемоксигенацию, химическое окисление крови (непрямое), ее фотомодификацию. Возможно проведение перфузии через клеточные взвеси или ксеноорганы.
Связывание и разведение эндотоксических компонентов. С этой целью возможно выполнение сорбционных мероприятий, направленных на выведение эндотоксических компонентов из крови, из плазмы, из лимфы, из ликвора.
Удаление эндотоксических компонентов. Для реализации данного механизма задействуют печень, почки, желудочно-кишечный тракт, кожу и легкие. Пациенту проводят кишечный диализ, гемодиализ, энтеросорбцию, плазмаферез, гемо- и ультрафильтрацию, замещение крови, форсируется диурез.
В период острой интоксикации общий суточный объем воды, которую вводят через капельницу, должен быть на уровне 4-5 литров. Причем 2,5-3 литра должны составлять кристаллоидные растворы, а оставшаяся часть – коллоидные и белковые препараты крови: плазму, альбумин, протеин.
Форсированный диурез считается простым и часто используемым способом лечения эндоинтоксикации, который базируется на применении естественного процесса удаления токсинов из организма.
Прогноз при синдроме эндогенной интоксикации напрямую зависит от тяжести состояния больного и от первопричины, приведшей к развитию патологии.

Автор статьи: Алексеева Мария Юрьевна | Терапевт
Образование:
С 2010 по 2016 гг. практикующий врач терапевтического стационара центральной медико-санитарной части №21, город электросталь. С 2016 года работает в диагностическом центре №3.
Наши авторы
Источник


