Псевдомембранозный колит этиология патогенез клиника лечение
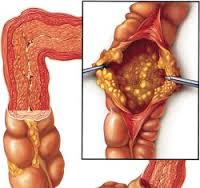
Доказано, что Clostridium difficile может обнаруживаться в стуле здоровых людей. Одновременноо, имеются убедительные данные, указывающие на то, что эти микроорганизмы не способны к длительному существованию в неизмененной нормальной микроэкосистеме кишечника.
Для осуществления патогенных свойств этого микроорганизма необходимы условия, способствующие его избыточному росту, которые возникают в результате применения антибиотиков, то есть проведения антибиотикотерапии.
К основным антибактериальным препаратам, связанным с развитием псевдомембранозного колита, относят цефалоспорины (особенно 2 и 3 поколений), ампициллин, амоксциллин и клиндамицин. Менее причинно-значимыми антибиотиками являются макролиды (эритромицин, кларитромицин, азитромицин) и другие пенициллины. Однако следует учитывать, что практически любой антибактериальный препарат может привести к возникновению псевдомембранозного колита.
Длительное применение антибиотиков или же одновременное применение 2-х и более антибактериальных препаратов ещё более повышает риск развития псевдомембраного колита.
Заболевание развивается при развитии резистентности Clostridium difficile к антибиотикам, подавляющим жизнедеятельность прочей кишечной микрофлоры. Таким образом, возникновение псевдомембранозного колита является результатом развития своеобразного “клостридиального” дисбактериоза у больных под влиянием различных предрасполагающих факторов.
Патогенные штаммы C. difficile продуцируют токсин А и токсин В. Токсин А – мощный энтеротоксин с цитотоксической активностью, вызывающий нарушение барьерной функции слизистой кишечника за счет повреждения эпителиоцитов и активацию секреции жидкости в просвет кишечника. Токсин B – цитотоксин, в 1000 раз более мощный цитотоксин, чем токсин А, его цитотоксический эффект обусловлен нарушением полимеризации внутриклеточных филаментов актина).
Токсины C.difficile воздействует на слизистую оболочку кишечника, вызывая в ней глубокие изменения, вплоть до перфорации. Некоторые антибиотики, особенно линкомицин, клиндамицин, ампициллин индуцируют продукцию цитотоксина, повышая его уровень в 16-128 раз без прироста биомассы микроорганизма; несколько меньше, но также повышается продукция энтеротоксина.
У C.difficile описаны плазмиды, которые участвуют в переносе устойчивости к антибиотикам.
Выявляемые в толстой кишке морфологические изменения слизистой обусловлены действием только токсинов, поскольку сами клостридии не обладают инвазивными свойствами и, как правило, в подслизистый слой не проникают. Протяженность и глубина морфологических изменений, выявляемых в толстой кишке, обусловливают тяжесть течения инфекционного процесса.
- Предрасполагающие факторы развития псевдомембраного колита
Помимо антибиотикотерапии (основного предрасполагающего фактора) кдругим предрасполагающим факторам развития псевдомембраного колита относят:
- Возраст старше 60 лет.
- Нахождение в стационаре (особенно в одной палате с инфекционным больным или в реанимационном отделении).
- Операции на органах брюшной полости.
- Применения цитостатических препаратов (особенно метотрексата).
- Гемолитико-уремический синдром.
- Злокачественные заболевания.
- Ишемия кишечника.
- Почечная недостаточность.
- Некротический энтероколит.
- Болезнь Гиршпрунга.
- Хронические воспалительные заболевания кишечника.
- Различные желудочно-кишечные нехирургические манипуляции (например, установка назогастрального зонда).
Источник
Введение
Врачи достаточно часто сталкиваются с диареей развивающейся у пациентов, на фоне или после применения антибиотиков. В России как больные, так и ряд врачей склонны связывать ее появление с «дисбактериозом». Зарубежные специалисты в этом случае говорят об «антибиотик-ассоциированной диарее». Clostridium difficile является возбудителем наиболее тяжелых форм данного осложнения, вплоть до развития фульминантного колита и токсической дилатации толстой кишки. По данным канадских исследователей уровень заболеваемости связанной с инфекцией данным возбудителем составляет от 30,8 до 40,3 случая на 100 тыс. больных (в больницах с более 200 коек) [1]. У 10 % пациентов получающих антибиотики развивается диарея, но только в 1 % случаев возникает псевдомембранозный колит.
Этиология и патогенез
Clostridium difficile это спорообразующий, анаэробный микроорганизм впервые описанный в 1935 году [7]. Однако роль токсинов Clostridium difficile в развитии псевдомембранозного колита была установлена только к 1978 году [6]. Микроорганизм далеко не всегда вызывает развитие заболевания (т.к. существуют штаммы, не продуцирующие токсины), а его тяжесть может варьировать от легкой диареи, без признаков колита, до угрожающих жизни состояний.
Патогенез заболевания включает следующие этапы
- нарушение нормальной микрофлоры толстой кишки (в норме стул содержит более 500 различных бактерий в концентрации 10 в 12 степени в одном грамме);
- колонизация толстой кишки продуцирующими токсин штаммами Clostridium difficile;
- выработка токсинов (А и В);
- воспаление и повреждение слизистой оболочки толстой кишки (до некроза эпителия и образования мембран в тяжелых случаях).
Чаще всего к развитию заболевания приводит применение клиндамицина, линкамицина, цефалоспоринов и защищенных пенициллинов [3]. Кроме недавнего (обычно не позднее 2 месяцев) применения антибиотиков риск развития инфекции повышен у лиц старше 60 лет, стационарных больных, пациентов с ослабленным иммунитетом, почечной недостаточностью, онкологическими заболеваниями и у лиц получающих антисекреторную терапию.
Клиника
К типичным симптомам данной патологии относятся диарея (стул водянистый, небольшого объема, от 4 до 20 раз в сутки, без примесей крови), схваткообразная боль в животе, а также слабость, анорексия и тошнота. Не специфическими, хотя и весьма характерными для инфекции Clostridium difficile признаками являются лейкоцитоз (до 15х109/л, а иногда и выше), гипоальбуминемия и лейкоциты в кале.
При заболевании легкой степени развивается водянистая диарея, не сопровождающаяся системными симптомами и явлениями колита при эндоскопическом обследовании.
При средней степени тяжести кроме диареи беспокоят сваткообразные боли в животе, вздутие живота, наблюдается умеренная дегидратация, тахикардия до 100 ударов в минуту, умеренный лейкоцитоз с нейтрофильным сдвигом, умеренное снижение артериального давления. При эндоскопии можно часто наблюдать характерную для псевдомембранозного колита картину.
При тяжелом течении на первое место выходят системные проявления – спутанное сознание, лихорадка, тахикардия больше 100 ударов в минуту, падение давления ниже 100 мм рт. ст., вентиляционные нарушения, высокий лейкоцитоз (до лейкемойдной реакции), развиваться токсическая делатация толстой кишки, ее перфорация, перитонит. У пациентов с таким вариантом заболевания диарея можем отсутствовать, в результате токсической дилатации толстой кишки [10].
При рентгенологическом исследовании или компьютерной томографии визуализируются «отпечатки большого пальца» свидетельствующие об отеке слизистой толстой кишки и/или дилатация толстой кишки. По данным Dallal et. al., [4] из 39 пациентов с колитом, он носил правосторонний характер у 11, левосторонний у 9 и тотальный у 19. Эндоскопическая картина может варьировать от нормы до диффузного или очагового колита с или без образования псевдомембран. Исследование не должно выполняться при подозрении на токсическую дилатацию в связи с риском перфорации толстой кишки.
Стандартом диагностики является определение токсинов Clostridium difficile в кале. Желательно проводить определение как токсина А, так и В т.к 1-2 % штаммов Clostridium difficile продуцируют только токсин В [9]. Методика, основанная на действии цитотоксина в культуре ткани обладает высокой чувствительностью (94-100 %) и специфичностью (99 %) [10,11]. Несмотря на то, что она позволяет выявить токсин в количестве 10 pg и рассматривается в качестве «золотого стандарта» диагностики, ее проводят в немногих лабораториях, а время до получения результата занимает 24-48 часов [3].
Существует иммуноферментный метод определения токсина А и/или В в стуле. Результат исследования становиться известным в течение нескольких часов, но его чувствительность (65-85 %) и специфичность (95-100 %) ниже [2, 16]. Данный тест требует присутствия большего количества токсина для получения положительного результата (100-1000 pg) [3]. Несмотря на это, данную методику рассматривают как диагностический тест выбора у лиц с частотой стула более 6 раз в день [8]. У 5-20 % больных необходимо не однократное исследование стула для выявления токсина [14].
Получение культуры Clostridium difficile в анаэробных условиях для диагностики используется редко, во первых потому, что это занимает несколько дней, а во вторых не позволяет различить патогенные и не патогенные штаммы. Получение культуры с оценкой ее токсигенности позволяет избежать этой проблемы, но методика весьма трудоемка и занимает несколько суток.
Другие диагностические тесты включают реакцию латексной аглютенации (на клостридиальный белок глутамат дегидрогеназу, но она имеет относительно низкую чувствительность и специфичность) и определение токсинов путем полимеразной цепной реакции (находиться в процессе стандартизации).
Лечение
Одним из важнейших этапов лечения является отмена антибиотика вызвавшего заболевание (если это возможно). При легкой степени инфекции этого бывает достаточно для выздоровления [5]. При необходимости продолжения антибиотикотерапии лучше использовать препараты реже вызывающие развитие клостридиальной инфекции: аминогликозиды, сульфаниламиды, макролиды, тетрациклин и фторхинолоны.
В случае более тяжелого течения данной патологии необходимо назначение препаратов направленных на подавления Clostridium difficile. В качестве лечения выбора рассматривается Метронидазол 250 мг 4 раза в сутки или 500 мг 3 раза [15]. Ванкомицин (125 мг 4 раза в сутки) применяется при непереносимости метронидазола или его неэффективности [13]. Эффективность обеих препаратов сходна [17,18]. В обоих случаях длительность терапии 10-14 дней (улучшение состояние должно наступить в течение 72 часов). Если пациент продолжает лечение другими антибиотиками то метронидазол (ванкомицин) должен применяться весь период лечения и неделю после его прекращения [13]. Ванкомицин практически не всасывается и, следовательно, дает меньше побочных эффектов, но значительно дороже метронидазола.
Антиперистальтические агенты категорически противопоказаны. В качестве адсорбента рекомендуется холестирамин [12], но т.к. в России он отсутствует, мы с успехом вместо него используем смекту (в стандартных дозах). У пациентов с тяжелым колитом, которые не могут принимать препараты перорально, применяется метронидазол внутривенно, он выделяется в желчь и достигает достаточно высокой концентрации в просвете ЖКТ, но не ванкомицин т.к. при парентеральном введении последний в просвет ЖКТ практически не экскретируется. Впрочем, можно вводить ванкомицин (парентеральная форма) через назогастральный зонд или непосредственно в толстую кишку [13]. Не следует забывать о полноценной регидратации (пероральной или инфузионной) и коррекции электролитных нарушений.
В 10-20 % случаев при прекращении лечения возникает рецидив заболевания [19]. Он проявляется повторным возникновением симптомов через 3-21 день после прекращения применения метронидазола или ванкомицина. В таких случаях показана повторная терапия метронидазолом или ванкомицином, разумным является добавления лактобактерий и пробиотиков (хотя их эффективность не доказана).
У 0.4 %- 3,6 % пациентов требуется хирургическое лечение [13]. Наиболее частыми показаниями к операции является перитонит и токсическая дилатация толстой кишки с высоким риском перфорации. Операцией выбора является субтотальная колэктомия, но уровень летальности при ее выполнении достигает 57 % [4].
В заключение приведем схему лечения применяемую нами:
- Отмена антибиотиков (если возможно) или замена их на относительно безопасные (аминогликозиды, макролиды, фторхинолоны).
- Отмена всех антиперистальтических агентов и опиойдных анальгетиков.
- Смекта (стандартная дозировка).
- Линекс или хилак-форте (стандартная дозировка).
- Метронидазол 250 мг 4 раза в день (при системных проявлениях, частоте стула более 4 в сутки или необходимости продолжать антибиотикотерапию).
- Ванкомицин 125 мг 4 раза в сутки (при непереносимости, неэффективности метронидазола или при тяжелой инфекции).
- Метронидазол внутривенно (ванкомицин через назогастральный зонд) при невозможности самостоятельного приема препаратов.
- Коррекция водно-электролитных нарушений.
Литература
- Alfa M. J., Dul T., Beda G. Sulrvey of incidence of Clostridiulm difficile infection in Canadian hospitals and diagnostic approaches// J. Clin. Microbiol. 1998. V. 36. P. 2076-2080.
- Barbut F., Kajzer C., Planas N., Petit J.C. Comparison of three enzyme immunoassays, a cytotoxicity assay, and toxigenic culture for diagnosis of Clostridium difficile-associated diarrhea. J Clin Microbiol 1993;31:963-7.
- Bartlett J. G. ANTIBIOTIC-ASSOCIATED DIARRHEA N Engl J Med, Vol. 346, No 56: 334-339.
- Dallal M.R. Fulminant Clostridium difficile: An Underappreciated and Increasing Cause of Death and Complications. Ann Surg. 2002 March; 235(3): 363–372.
- Fekety R. Guidelines for the diagnosis and management of Clostridium
difficile-associated diarrhea and colitis. Am J Gastroenterol 1997;92:739-50. - George R.H., Symonds J.M., Dimock F., et al. Identification of Clostridium difficile as a cause of pseudomembranous colitis. BMJ 1978;1:695.
- Hall I.C., O’Toole E. Intestinal flora in newborn infants with a description of a new pathogenic anaerobe, Bacillus difficilis. Am J Dis Child 1935; 49:390-402.
- Jacobs J., Rudensky B., Dresner J., et al. Comparison of four laboratory tests for diagnosis of Clostridium difficile–associated diarrhea. Eur J Clin Microbiol Infect Dis 1996;15: 561-6.
- Johnson S., Kent S.A., O’Leary K.J., et al. Fatal pseudomembranous colitis associated with a variant Clostridium difficile strain not detected by toxin A immunoassay. Ann Intern Med 2001;135:434-8
- Kelly C.P., Pothoulakis C., LaMont J.T. Clostridium difficile colitis. N Engl J Med 1994;330:257-62
- Kelly CP, LaMont JT. Clostridium difficile infection. Annu Rev /Med 1998;49:375-90.
- Kreutzer E.W., Milligan F.D. Treatment of antibiotic-associated pseudomembranous colitis with cholestyramine resin. Johns Hopkins Med J 1978;143:67-72.
- Malnick S., Zimhony O. Treatment of Clostridium difficile–Associated Diarrhea. Ann Pharmacother 2002;36:1767-75.
- Manabe Y.C., Vinetz J.M., Moore R.D., Merz C., Carache P., Bartlett J.G. Clostridium difficile colitis: an efficient clinical approach to diagnosis. Ann Intern Med 1995;123:835- 40.
- Mylonakis E., Ryan E.T., Calderwood S.B. Clostridium difficile–associated diarrhea. A review. Arch Intern Med 2001;161:525-33.
- Staneck J.L., Weckbach L.S., Allen S.D., et al. Multicenter evaluation of four methods for Clostridium difficile detection: immunoCard C. difficile, cytotoxin assay, culture, and latex agglutination. J Clin Microbiol 1996;34:2718-21.
- Teasley D.G., Gerding D.N., Olson M.M., et al. Prospective randomised trial of metronidazole versus vancomycin for Clostridium-difficile-associated diarrhoea and colitis. Lancet 1983;2:1043-1046.
- Wenisch C., Parschalk B., Hasenhundl M., Hirschl A.M., Graninger W. Comparison of vancomycin, teicoplanin, metronidazole, and fusidic acid for the treatment of Clostridium difficile-associated diarrhea. Clin Infect Dis 1996;22:813-8.
- Young G., McDonald M. Antibiotic-associated colitis: why do patients relapse? Gastroenterology 1986;90:1098-1099.
Источник
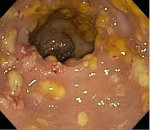
Псевдомембранозный колит – это острое воспаление толстого кишечника, вызываемое условно патогенными клостридиями и возникающее на фоне приема антибиотиков или (реже) других лекарственных средств. Клинические проявления могут варьировать. Обычно выявляются боли в животе и продолжительная диарея в сочетании с признаками общей интоксикации. В тяжелых случаях возможны грубые повреждения кишечной стенки, выраженные расстройства обмена и летальный исход. Заболевание диагностируется на основании симптомов, данных осмотра, анализов крови и кала, эндоскопического исследования. Лечение – отмена антибиотика, диета, этиотропная терапия, коррекция обменных нарушений.
Общие сведения
Псевдомембранозный колит – тяжелое осложнение приема антибиотиков, реже лечения препаратами других групп, в результате которого у больного развивается специфический дисбактериоз, сопровождающийся воспалением толстого кишечника с образованием характерных пленок на слизистой оболочке. Дисбактериоз и воспаление слизистой вызывают анаэробные грамположительные бактерии Clostridium difficile. В тяжелых случаях псевдомембранозный колит сопровождается выраженной интоксикацией, повреждениями стенки кишечника вплоть до перфорации, общей дегидратацией и грубыми электролитными расстройствами, нередко – в сочетании нарушениями белкового обмена. Возможен летальный исход. Лечение осуществляют специалисты в области клинической проктологии и гастроэнтерологии.

Псевдомембранозный колит
Причины
Причиной псевдомембранозного колита является нарушение нормальной кишечной микрофлоры, сопровождающееся избыточным размножением условно патогенной бактерии Clostridium difficile. В подавляющем большинстве случаев дисбактериоз, предшествующий развитию псевдомембранозного колита, возникает на фоне приема антибиотиков, однако в отдельных случаях состав микрофлоры кишечника может меняться под влиянием цитостатиков, иммуносупрессоров и слабительных средств.
Чаще всего псевдомембранозный колит вызывают такие антибиотики, как клиндамицин, амоксициллин, ампициллин, линкомицин и препараты из группы цефалоспоринов. Реже псевдомембранозный колит развивается при приеме левомицетина, эритромицина, тетрациклина и пенициллина. Из-за подавления микробов-симбионтов в кишечнике начинают размножаться Clostridium difficile. Эти бактерии в небольшом количестве содержатся в ЖКТ примерно у 3% населения.
Размножающиеся клостридии выделяют токсические вещества, оказывающие негативное влияние на слизистую оболочку кишечника и вызывающие развитие псевдомембранозного колита. Некоторые антибиотики усиливают повреждающее действие токсинов, что еще больше усугубляет возникшие нарушения. Стенка кишечника теряет свои барьерные свойства и начинает интенсивно секретировать жидкость в просвет кишки. Токсичные соединения всасываются в организм, вызывая развитие интоксикации. Жидкость перемещается в просвет кишечника, развивается обезвоживание, возникают электролитные расстройства.
В тяжелых случаях у больных псевдомембранозным колитом выявляются нарушения белкового обмена. Страдает сердечно-сосудистая система. Возможно формирование токсического мегаколона и прободение стенки кишечника с излитием кишечного содержимого в брюшную полость. Причиной летального исхода при псевдомембранозном колите может стать перитонит, обусловленный инфицированием брюшной полости микроорганизмами, содержащимися в каловых массах, или обезвоживание и нарушение функций различных органов и систем в результате интоксикации и грубых обменных расстройств.
Псевдомембранозный колит может рассматриваться, как внутрибольничная инфекция. Болезнь часто развивается при лечении в стационарных условиях, особенно – при пребывании в одной палате с пациентами, страдающими данной патологией. Факторами, увеличивающими вероятность развития псевдомембранозного колита и одновременно усугубляющими его течение, являются пожилой возраст, декомпенсированные соматические заболевания, болезни ЖКТ, бесконтрольный прием антацидов, почечная недостаточность, злокачественные опухоли, иммунные нарушения (в том числе – при СПИДе), ослабление организма после обширных хирургических вмешательств, а также состояния различного генеза, требующие проведения интенсивной терапии.
Симптомы колита
Клиническая картина псевдомембранозного колита определяется тяжестью патологии. При легких формах наблюдаются поносы и схваткообразные боли в животе на фоне ухудшения общего состояния организма. Стул обильный, водянистый, возможно – с примесями слизи. Общая интоксикация при псевдомембранозном колите проявляется в виде повышения температуры тела, слабости, разбитости, головной боли, тошноты и рвоты. Выраженность диареи и интоксикационного синдрома могут различаться. Все признаки исчезают после отмены антибиотиков.
При тяжелой форме болезни и псевдомембранозном колите средней степени тяжести клиническая симптоматика сохраняется в течение 1-2 и более недель после прекращения антибиотикотерапии. Пациенты страдают от изнуряющей диареи. Кал приобретает специфический вид «рисового отвара» желтоватой или зеленоватой окраски. В каловых массах больных псевдомембранозным колитом выявляются примеси слизи и крови. Потери значительных количеств жидкости с калом обуславливают развитие дегидратации и расстройств водно-электролитного обмена, проявляющихся слабостью, учащением пульса, снижением артериального давления, нарушением тонуса мышц и парестезиями. Возможны судороги. Отмечается уменьшение количества выделяемой мочи.
Отличительными особенностями тяжелой формы псевдомембранозного колита являются более бурное течение и появление крови в фекальных массах с первых дней заболевания. Наблюдается быстрое нарастание интоксикации, в сочетании с интенсивными схваткообразными болями в левой половине живота (преимущественно – в проекции сигмовидной кишки). Тяжелым осложнением псевдомембранозного колита может стать образование патологического расширения кишечника (мегаколона) с последующим разрывом кишки и развитием перитонита. О развитии мегаколона свидетельствует ухудшение состояние пациента с гипертермией до 39 градусов и выше в сочетании с уменьшением частоты дефекаций и увеличением объема живота.
У некоторых пациентов с псевдомембранозным колитом выявляется реактивный артрит. Иногда наблюдается экссудативная энтеропатия – невоспалительное поражение кишечника, сопровождающееся нарушениями белкового обмена и гипопротеиновыми отеками, обусловленными потерей большого количества белка через желудочно-кишечный тракт. Известны случаи стремительного развития псевдомембранозного колита с быстрым обезвоживанием, развитием гиперкалиемии и последующей остановкой сердца.
Диагностика
Диагноз устанавливается специалистом-проктологом или гастроэнтерологом с учетом анамнеза (прием антибиотиков или других препаратов, способных спровоцировать развитие заболевания), жалоб, данных физикального исследования и дополнительных диагностических процедур. В ходе внешнего осмотра больного псевдомембранозным колитом врач отмечает гипертермию, артериальную гипотонию, тахикардию, увеличение объема живота и болезненность при пальпации. В общем анализе крови определяется лейкоцитоз. При исследовании кала выявляются кровь и слизь. При бактериологическом исследовании фекальных масс обнаруживаются Clostridium difficile.
При проведении эндоскопического исследования у пациентов с псевдомембранозным колитом визуализируется слизистая оболочка, покрытая характерными желтоватыми фибринозными пленками (псевдомембранами). Обычно для подтверждения диагноза достаточно ректороманоскопии, поскольку псевдомембранозный колит чаще поражает дистальные отделы толстой кишки. В сомнительных случаях и при необходимости оценить состояние верхних отделов толстого кишечника проводят колоноскопию. При подозрении на развитие мегаколона назначают радиологические исследования (КТ, рентгенографию).
Лечение псевдомембранозного колита
Лечение данной патологии преимущественно консервативное. Больным отменяют антибиотики, назначают специальную диету, рекомендуют употреблять больше жидкости для предупреждения дегидратации. При легких формах псевдомембранозного колита этиотропные препараты обычно не требуются. При среднетяжелой и тяжелой форме болезни используют метронидазол. При наличии противопоказаний к применению данного препарата проводят терапию ванкомицином. Для восстановления нормальной микрофлоры кишечника назначают препараты бифидум и лактобактерий.
При тяжелых формах псевдомембранозного колита осуществляют инфузионную терапию для восстановления объема жидкости, устранения интоксикации, коррекции потерь белка и электролитных нарушений. При псевдомембранозном колите, осложненном токсическим мегаколоном, показано хирургическое вмешательство – сегментарная резекция пораженной части кишечника. Перфорация кишки является показанием к проведению неотложной операции – удалению пораженного отдела кишки, промыванию и дренированию брюшной полости для предупреждения развития перитонита.
Прогноз и профилактика
Прогноз при псевдомембранозном колите определяется тяжестью заболевания. Средняя вероятность гибели пациентов с данной патологией при отсутствии лечения составляет около 30%. При легких формах псевдомембранозного колита обычно наблюдается выздоровление после прекращения антибиотикотерапии. При колитах средней тяжести клиническая симптоматика сохраняется в течение нескольких недель, в последующем возможны рецидивы. Тяжелые формы псевдомембранозного колита часто завершаются гибелью пациентов. Шансы на благополучный исход при мегаколоне и перфорации кишечника еще больше снижаются, поскольку оперативные вмешательства приходится проводить в условиях резкого ослабления организма больного. Кроме того, перфорация толстой кишки часто осложняется перитонитом даже при раннем оперативном вмешательстве, что обусловлено наличием большого количества бактерий в кишечном содержимом.
Основной профилактической мерой является обоснованное назначение антибиотиков, выбранных с учетом индивидуальных противопоказаний, состояния больного и риска развития псевдомембранозного колита. Необходимо одновременное использование средств для предупреждения дисбактериоза, особенно – при продолжительной антибиотикотерапии. В группу высокого риска возникновения псевдомембранозного колита включают больных в возрасте старше 65 лет и пациентов, постоянно принимающих средства из группы антагонистов гистаминовых рецепторов. Больным из этой группы не рекомендуется назначать антибиотики, часто провоцирующие псевдомембранозный колит.
Источник
