Лечение язвенного колита стероидами
В статье рассмотрена роль системных и топических кортикостероидов в терапии язвенного колита
Язвенный колит (ЯК) представляет собой хроническое идиопатическое воспалительное заболевание с повреждением слизистой оболочки толстой кишки. При ЯК поражается только толстая кишка (за исключением ретроградного илеита), в процесс обязательно вовлекается прямая кишка, воспаление чаще всего ограничивается слизистой оболочкой (за исключением фульминантного колита) и носит диффузный характер. ЯК характеризуется периодами активного проявления симптомов заболевания, которые перемежаются периодами клинической ремиссии [1]. В 2012 г. статистический анализ показал, что в мире распространенность ЯК достигла 249 на 100 тыс. человек в Северной Америке и 505 на 100 тыс. человек в Европе; самые высокие годовые показатели заболеваемости ЯК были 19,2 на 100 тыс. человеко-лет в Северной Америке и 24,3 на 100 тыс. человеко-лет в Европе [2]. Самый высокий уровень заболеваемости, по-видимому, отмечается в возрасте 20–30 лет, хотя есть некоторые доказательства второго пика заболеваемости в более позднем возрасте [2]. Однако наличие второго пика заболеваемости признается не всеми специалистами, занимающимися воспалительными заболеваниями кишечника (ВЗК).
Эндоскопическое исследование толстой кишки у больных ЯК выявляет ряд характерных повреждений слизистой оболочки толстой кишки (СОТК): отсутствие сосудистого рисунка, гиперемию, зернистость, контактную кровоточивость, наличие эрозий и язв [1, 3]. В настоящее время заживление СОТК при ЯК рассматривается как одна из ключевых конечных точек в клинических исследованиях, а достижение заживления СОТК в клинической практике – как реальная возможность изменить течение ЯК и сохранить функции кишечника. В исследованиях последних лет показано, что заживление СО как при ЯК, так и при болезни Крона (БК) достоверно связано с большей продолжительностью клинической ремиссии заболевания, более низкой частотой рецидивов, более низким риском развития колоректального рака и более высоким качеством жизни [4, 5], а также существенно меньшей частотой кол-эктомий [6].
Существующие руководства по лечению взрослых больных ЯК в США [7], Европейском союзе [8] и Российской Федерации [9] рекомендуют в качестве первой линии терапии для индукции ремиссии у пациентов с легкой и среднетяжелой формами ЯК препараты 5-аминосалициловой кислоты (5-АСК). Такое лечение считается наиболее эффективным при комбинации системных и пероральных препаратов 5-АСК [7–9]. В случае неэффективности 5-АСК препаратами второй линии являются глюкокортикостероиды (ГКС) [7–9]. Однако ГКС I поколения, такие как преднизолон, имеют ряд побочных эффектов: повышенный риск развития инфекционных осложнений, остеопороза, синдрома Иценко – Кушинга, развитие стероидного диабета, симптоматической гипертензии и даже повышенный риск смертности по сравнению с таковым в общей популяции [7, 10–12].
В настоящее время для лечения ВЗК применяется несколько глюкокортикоидов топического действия для приема внутрь и для ректального введения: будесонид, тиксокортола пиволат, беклометазон, флютиказон [13]. В России с 2004 г. зарегистрирован и успешно применяется препарат Буденофальк (компания Dr. Falk, Германия) в форме капсул для приема внутрь. Одна капсула Буденофалька содержит 3 мг будесонида. При ряде заболеваний, например при бронхиальной астме и сезонном аллергическом рините, будесонид так же эффективен, как системные ГКС, отличаясь при этом лучшей переносимостью и меньшим влиянием на гипоталамо-гипофизарно-адреналовую систему. Это послужило основанием для применения будесонида при БК. Будесонид является первым топическим кортикостероидом, имеющим сродство к глюкокортикоидным рецепторам приблизительно в 8,5, 15 и 195 раз больше, чем у дексаметазона [14], преднизолона [15] и гидрокортизона [15] соответственно. Кроме того, будесонид почти не всасывается из кишечника, характеризуется низкой системной биодоступностью (не более 10% по сравнению с таковой преднизолона и гидрокортизона) и быстрым пресистемным метаболизмом. Последнее обеспечивает отсутствие токсичных метаболитов в крови после первого прохождения препарата через печень. Однако наиболее высокая внутрипросветная концентрация действующего вещества и, соответственно, наибольшая эффективность Буденофалька достигаются, начиная с терминального отдела подвздошной кишки и до поперечной ободочной кишки.
ЯК – это хроническое заболевание, поражающее только СОТК, сопровождающееся ее воспалением, отеком и образованием язвенных дефектов. Воспаление всегда начинается с прямой кишки, непрерывно распространяясь выше вплоть до поражения СО всех отделов толстой кишки. Таблетированный мультиматричный (ММХ) будесонид является представителем II поколения кортикостероидов, созданным для доставки активного вещества на протяжении всей толстой кишки. В фармакокинетических исследованиях среднее относительное всасывание будесонида в месте между восходящей кишкой и нисходящей/сигмовидной кишкой составило 95,9% (рис. 1) [16]. В 2-х похожих по дизайну исследованиях 3-й фазы (CORE I и II) однократный ежедневный прием будесонида ММХ 9 мг оказался эффективным и хорошо переносимым для индукции ремиссии ЯК легкой и средней степени тяжести. Частота клинической и эндоскопической ремиссии составила 17,9% (CORE I) и 17,4% (CORE II) для будесонида ММХ 9 мг по сравнению с плацебо 7,4% и 4,5% соответственно (p<0,05, будесонид ММХ 9 мг по сравнению с плацебо в обоих исследованиях), 12,1% с месалазином 2,4 г и 12,6% с будесонидом 9 мг, высвобождаемым в подвздошной кишке. По данным исследования поддерживающей терапии будесонидом в течение 12 мес., будесонид ММХ 6 мг может удлинять время до рецидива заболевания: среднее время составило 1 год для будесонида ММХ 6 мг по сравнению с 181 днем (р=0,02) для плацебо; однако необходимы дальнейшие исследования. В исследованиях CORE будесонид ММХ проявил хороший профиль безопасности; большинство нежелательных явлений (НЯ) были легкими или умеренными по своей интенсивности, серьезные НЯ были очень редкими. Более того, частота побочных реакций, возможно, связанных с глюкокортикоидами, была сравнима среди групп лечения. Долгосрочная безопасность (12 мес.) будесонида ММХ была сравнима с таковой плацебо. Эти данные подтверждают возможность включения ММХ будесонида в алгоритм лечения ЯК [17–20].
Будесонид ММХ для лечения и индукции ремиссии ЯК
Эффективность и безопасность будесонида ММХ для индукции ремиссии пациентов с легкой и умеренной активностью ЯК (индекс активности заболевания 4–10) изучались в похожих по дизайну рандомизированных исследованиях CORE I и CORE II [17–20]. В CORE I сравнивали будесонид ММХ 9 мг и 6 мг с месалазином 2,4 г и плацебо, тогда как в CORE II сравнивались те же дозы будесонида ММХ с будесонидом 9 мг, высвобождающимся в подвздошной кишке, и плацебо. В обоих исследованиях терапия проводилась 8 нед., и первичными точками были клиническая и эндоскопическая ремиссия на 8-й нед. лечения. Ремиссия определялась как индекс активности ЯК ≤ 1 со значением 0 для ректального кровотечения и частоты стула, отсутствие ранимости СО при колоноскопии, и снижение ≥ 1 эндоскопического индекса от исходного значения. В обоих исследованиях клиническая и эндоскопическая ремиссия была достигнута у значительной части пациентов, получавших будесонид ММХ 9 мг (по сравнению с плацебо). В исследовании CORE I ремиссия на 8-й нед. была достигнута у 17,9% пациентов, получавших будесонид ММХ 9 мг, у 7,4% (р=0,01) в группе плацебо и у 12,1% в группе, получавшей месалазин. В исследовании CORE II частота ремиссии к 8-й нед. составила 17,4% у пациентов, получавших будесонид ММХ 9 мг, по сравнению с 4,5% (p=0,005) и 12,6% (p=0,048) в группах, получавших плацебо и будесонид, высвобождающийся в подвздошной кишке, соответственно. Кроме этого, анализ подгруппы в исследовании CORE II показал, что при приеме будесонида ММХ 9 мг существенно большая часть пациентов с левосторонним ЯК достигла клинической и эндоскопической ремиссии, чем при приеме плацебо (17,7% по сравнению с 5,8% соответственно; p=0,03); часть пациентов с распространенным заболеванием, которые достигли клинической и эндоскопической ремиссии, также была больше при использовании будесонида ММХ 9 мг, чем при использовании плацебо (13,8% по сравнению с 0% соответственно), но это различие не было статистически значимым (p=0,10). В исследовании CORE I анализ подгрупп по тяжести заболевания показал, что у пациентов с легким течением ЯК (индекс активности ЯК 4 или 5), которые получали будесонид ММХ 9 мг или плацебо, клиническое улучшение (определялось как снижение ≥ 3 баллов индекса активности ЯК) было достигнуто у 44,4% и 25,0% пациентов соответственно; у пациентов с умеренной активностью заболевания (индекс ЯК ≥ 6 и ≤10) показатели клинического улучшения составили 39,7% и 30,1% соответственно. Более того, частота заживления СО была больше при применении будесонида MMX 9 мг, чем при применении плацебо, у пациентов с проктосигмоидитом (32,4% по сравнению с 19,5% соответственно; p=0,20) и левосторонним ЯК (40,6% по сравнению с 26,5% соответственно; p=0,22). Похожее различие в пользу будесонида ММХ 9 мг наблюдалось у пациентов с распространенным ЯК (16,1% по сравнению с 10,0% при применении плацебо), но это различие также не было статистически значимым (p=0,39). В анализе исследований CORE I и CORE II пациенты, получающие будесонид ММХ 9 мг, достигали клинической и эндоскопической ремиссии в 3 раза чаще, чем при получении плацебо [ОШ 3,3 (95% ДИ 1,7–6,4)]. Будесонид ММХ 9 мг был статистически значимо более эффективен по сравнению с плацебо у нескольких групп пациентов: мужского и женского пола ≤ 60 лет; ранее принимавших месалазин; не получавших месалазин ранее; с легким течением ЯК на исходном уровне; со средней тяжестью ЯК исходно; с проктосигмоидитом; с левосторонним ЯК; с длительностью ЯК ≥ 1 года и ≤5 лет; с длительностью ЯК > 5 лет.
Будесонид ММХ 9 мг для поддержания ремиссии ЯК
Эффективность будесонида ММХ 9 мг для поддержания ремиссии была изучена у пациентов, которые достигли клинической и эндоскопической ремиссии в исследованиях CORE I и CORE II, у пациентов в исследованиях CORE I и II, которые получали дополнительно 8 нед. лечения (будесонид ММХ 9 мг), и открытом исследовании, в котором пациенты были рандомизированы на группы, получавшие будесонид ММХ 6 мг или плацебо в течение 12 мес.; первичная точка эффективности – клиническая ремиссия, которая оценивалась через 1, 3, 6, 9 и 12 мес. Среднее время до рецидива заболевания (определялось как ректальное кровотечение, частота стула более чем 1–2 р./сут или оба этих фактора) составило 181 день в группе плацебо, но не было достигнуто в группе будесонида ММХ (p=0,02); к 12 мес. вероятность рецидива составила 59,7% и 40,9% соответственно. Однако процентное соотношение пациентов, у которых ремиссия поддерживалась в течение 12 мес., не различалось существенно между группами, что, возможно, связано со статистическими недостатками исследования.
Следовательно, польза будесонида ММХ в поддержании ремиссии в настоящее время недостаточно ясна, и необходимо проведение дальнейших исследований [21].
Побочные эффекты
В целом у молекулы будесонида более благоприятный профиль безопасности, чем у I поколения пероральных кортикостероидов, таких как преднизон или преднизолон. Например, в двойном слепом исследовании в течение 10 нед. 176 пациентов с БК, которые получали преднизолон по схеме снижения или будесонид, высвобождающийся в подвздошной кишке, в течение 10 нед., частота побочных явлений, связанных с глюкокортикоидами, была значительно ниже при применении будесонида, чем преднизолона (33% по сравнению с 55% соответственно; p=0,003). Кроме этого, подавление гипоталамо-гипофизарно-надпочечниковой системы, оцениваемое с помощью измерения средней концентрации кортизола в плазме, было существенно выше при применении преднизолона, чем будесонида, высвобождавшегося в подвздошной кишке, через 4 нед. (р<0,001) и 8 нед. (р=0,02). Благоприятный профиль НЯ будесонида ММХ у пациентов с ЯК был показан в исследованиях CORE I и II.Частота НЯ у пациентов, получающих будесонид ММХ 9 мг или 6 мг, составила 57,5% и 58,7% соответственно в исследовании CORE I, 55,5% и 62,5% соответственно – в CORE II. В обоих исследованиях большинство НЯ было легкими или умеренными по интенсивности, частота серьезных НЯ была ниже и схожей во всех группах лечения. Наиболее распространенными НЯ у пациентов, получавших будесонид ММХ, были головная боль, тошнота. В исследованиях CORE I и II частота НЯ, возможно, связанных с ГКС (акне, задержка жидкости, гиперемия, гирсутизм, инсомния, изменение настроения, «лунное» лицо, нарушение сна, образование стрий), была сравнима с таковой для будесонида ММХ 9 мг (10,2%), 6 мг (7,5 %) и плацебо (10,5%). Самыми распространенными НЯ, возможно, связанными с ГКС, при применении будесонида ММХ 9 мг по сравнению с плацебо были изменения настроения (3,5% и 4,3% соответственно) и нарушение сна (2,7% и 4,7% соответственно). В исследовании будесонида ММХ 6 мг в течение 1 года профиль безопасности был сравним с таковым плацебо [22].
Клиническое наблюдение
Больной Б., 22 года. Болен с 2013 г., диагноз «язвенный колит» поставлен при колоноскопии в ГНЦ колопроктологии и подтвержден гистологически в 2013 г. Принимал постоянно месалазин 3 г/сут. Амбулаторно проведена колоноскопия 24.11.2014 г.: язвенный колит, тотальное поражение, минимальная активность. С января 2016 г. отменил прием препаратов 5-АСК. В феврале 2016 г. отметил появление примеси крови в стуле. Возобновил прием месалазина 3 г/сут со слабоположительным эффектом, кровь в стуле сохранялась.
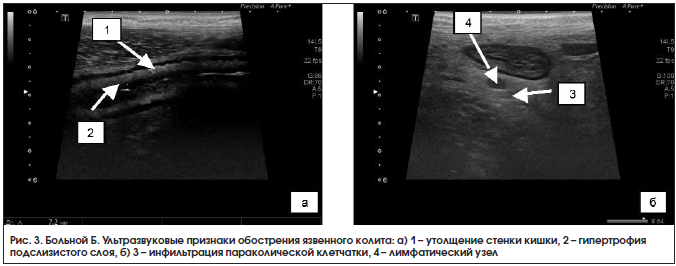
Однако с середины марта 2016 г. состояние ухудшилось, кроме примеси крови в стуле отмечались диарея до 17 р./сут, периодическое повышение температуры тела до 38° С в вечернее время. При колонофиброскопии от 15.03.2016 г. колоноскоп проведен в дистальный отдел восходящей части толстой кишки, заключение: эндоскопическая картина ЯК (тотальное поражение), тяжелая степень активности (рис. 2). При ЭГДС – хронический гастродуоденит с признаками выраженного обострения процесса, дуоденогастральный рефлюкс, недостаточность кардии, Нр+. Самостоятельно увеличил дозу месалазина до 4 г/сут, микроклизмы месалазина 2 г/сут на ночь со слабоположительным эффектом в виде урежения стула до 12 р./сут, примесь крови сохранялась.
![Рис. 1. Сцинтиграфия здорового добровольца. Будесонид MMX меченый [153Sm] в толстой кишке. Изображение получено через 7 ч после приема препарата (Brunner et al., 2006) Рис. 1. Сцинтиграфия здорового добровольца. Будесонид MMX меченый [153Sm] в толстой кишке. Изображение получено через 7 ч после приема препарата (Brunner et al., 2006)](https://www.rmj.ru/upload/medialibrary/fdc/fdce054cd022b9f2e7afc1c307ee002c.png)
18.03.2016 г. поступил на стационарное лечение в ГБУЗ МКНЦ ДЗМ. В общем анализе крови от 18.03.2016 г. отмечались лейкоцитоз (9,6 × 109) с палочкоядерным сдвигом (28%), повышение СОЭ до 26 мм/ч. В биохимическом анализе крови от 18.03.2016 г. отмечались повышение СРБ до 133,37 мг/л, латентный дефицит железа – 5,4 мкмоль/л.
При УЗИ органов брюшной полости 18.03.2016 г.: стенка левых отделов отечная, гипоэхогенная, утолщена до 7–8 мм, гаустрация сглажена, дифференциация слоев прослеживается четко не везде, в просвете – жидкость и изоэхогенное содержимое, в толще стенки – гиперэхогенные включения, что может соответствовать наличию язвенных дефектов; по ходу нисходящего отдела и сигмовидной кишки воспалительная инфильтрация параколической клетчатки с включением л/узлов размером до 11×7 мм; свободная жидкость в правой подвздошной области в небольшом количестве; заключение: эхопризнаки язвенного колита, левостороннее поражение, воспалительная инфильтрация параколической клетчатки по ходу левых отделов ободочной кишки с лимфаденопатией, небольшое количество свободной жидкости в правой подвздошной области (рис. 3). Кальпротектин кала от 19.03.2016 г. – 840 мкг/г.

Установлен диагноз: язвенный колит, тотальное поражение, хроническое рецидивирующее течение, средней степени тяжести, умеренной активности. Латентный дефицит железа.
С учетом отсутствия у больного эффекта от терапии препаратами 5-АСК и категорического отказа от проведения терапии системными ГКС больному назначены Кортимент (топические ГКС) 9 мг/сут, месалазин 5 г/сут, микроклизмы с гидрокортизоном 125 мг 2 р./сут, метронидазол 500 мг 3 р./сут в/в, гидроксид железа 100 мг/сут № 3; цефтриаксон 2,0 г/сут в/в капельно.
На фоне терапии через 10 дней у больного отмечалось улучшение состояния в виде урежения стула до 2 р./сут, без примеси слизи и крови.
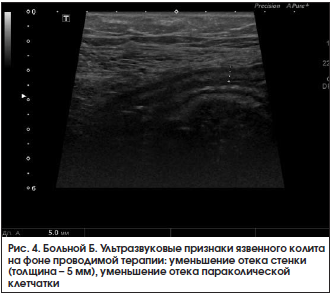
При контрольном УЗИ кишечника 28.03.2016 г.: по сравнению с предыдущим исследованием от 18.03.2016 г. отмечается положительная динамика. Тонкая кишка: петли не расширены, прослеживается ритмичная перистальтика, содержимое – средней эхогенности. Осмотрена ободочная кишка. В проекции слепой кишки, восходящего и поперечного отдела стенки не утолщены (2 мм), дифференциация слоев четкая. В проекции нисходящего отдела и сигмовидной кишки стенки толщиной 2,5–2,7 мм, слоистость стенки сохранена, более выражен подслизистый слой, в толще стенки сохраняются гиперэхогенные включения до 1,5 мм (вероятно, язвы). Клетчатка вокруг умеренно повышенной эхогенности с включением л/узлов размером до 8×3 мм. В правой подвздошной области межпетельно незначительное количество свободной жидкости. Заключение: эхопризнаки язвенного колита, левостороннее поражение, обострение. Мезентериальная лимфаденопатия (рис. 4). В общем анализе крови от 28.03.2016 г. сохраняется повышение СОЭ до 33 мм/ч. В биохимическом анализе крови от 28.03.2016 г. – нормализация уровня СРБ до 3,25 мг/л.
Заключение
Лекарственная формула будесонид ММХ доставляет лекарственное вещество в толстую кишку на всем ее протяжении [23], в то время как другие пероральные формы будесонида с контролируемым высвобождением работают только в дистальной части подвздошной кишки и в восходящей кишке – участках, которые наиболее часто поражаются воспалительным процессом при БК [24].
Будесонид ММХ является эффективным и хорошо переносится при применении с целью индукции ремиссии у пациентов с ЯК легкой и средней тяжести. Имеющиеся в настоящее время данные говорят о том, что этот препарат может быть эффективным и хорошо переноситься для поддержания длительной ремиссии (более 1 года) у пациентов с ЯК [17, 18]. Долгосрочная безопасность ММХ будесонида у пациентов с ЯК сравнима с таковой плацебо, эти данные представлены только в одном исследовании, которое длилось 12 мес. [19]. Однако в нескольких исследованиях изучали применение пероральных форм будесонида в качестве поддерживающей терапии у пациентов с БК, и это подтверждает долгосрочную (до 1 года) безопасность будесонида при поддержании ремиссии ВЗК [25–32]. Применение будесонида ММХ также может быть полезным в фармакоэкономическом плане в связи с возможным повышением приверженности терапии благодаря однократному приему препарата и снижению риска побочных явлений по сравнению с таковым при приеме традиционных пероральных кортикостероидов. Однако необходимо дальнейшее изучение этого препарата у пациентов с ВЗК.
Источник
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Я предоставляю слово Щукиной Оксане Борисовне. Мы опять в Санкт-Петербурге. Оксана Борисовна, «Оптимизация терапии язвенного колита. Калейдоскоп клинических наблюдений».
Оксана Борисовна Щукина, доценит, кандидат медицинских наук:
– Глубокоуважаемые коллеги, добрый день! Прежде всего, хотелось бы сказать, что когда мы касаемся вопросов лечения язвенного колита, мы обязательно подчеркиваем различия, касающиеся стандартных подходов для купирования тяжелой, фульминантной атаки язвенного колита и индукции ремиссии язвенного колита легкой и средней степени тяжести. Кроме того, назначая терапию, мы должны учитывать локализацию поражения – проктит это, левосторонний язвенный колит или тотальный, распространенный язвенный колит. И, наконец, наша лечебная тактика будет отличаться в зависимости от стадии заболевания – имеем мы дело с обострением язвенного колита, и тогда речь идет об индукции ремиссии, клинико-эндоскопической ремиссии с отменой стероидов, либо мы говорим об уже достигнутой ремиссии язвенного колита, и речь идет о поддержании без стероидов с эндоскопической оценкой.
Следует подчеркнуть, что язвенный колит на сегодняшний день является неизлечимым заболеванием, и поэтому терапия для пациентов пожизненной является. В отличие от болезни Крона, поражение затрагивает только толстую кишку, поэтому хирургическое излечение возможно проведением операции колпроктэктомии. Что касается лечения препаратами 5-аминосаллициловой кислоты легкой и средней тяжести язвенного колита, то у 80% пациентов больных эти препараты являются вполне эффективными. Консенсус говорит, что все препараты месалазина одинаково эффективны, в ряде случаев повышение дозы месалазина более 3-4 г приводит к более быстрому достижению ответа. Рекомендуется назначение месалазина с учетом не только эффективности, но также и учитывается способ высвобождения действующего вещества, кратность приема, что влияет на приверженность лечению, и различные системы доставки месалазина, потому что препарат работает конкретно в том сегменте толстой кишки, куда он доставлен. Поэтому говоря в целом об одинаковой эффективности месалазинов, у каждого конкретного пациента эффективность может быть индивидуальной, в зависимости от этих его свойств.
Я остановлюсь на трех случаях клинических – это будет фульминантная атака язвенного колита, тяжелая атака и язвенный колит средней степени тяжести – и на клинических примерах попытаюсь подчеркнуть особенности оптимизации терапии по индукции ремиссии и по поддержанию ремиссии у этих пациентов. Итак, пациентка 1972 года рождения, в тридцатичетырехлетнем возрасте бросает курить. В последующем, спустя примерно год после родов фульминантная атака язвенного колита – стул до 12 раз, высокая лихорадка, со снижением гемоглобина до 96, с ускоренным СОЭ до 62, С-реактивный белок при норме 5 до 136, и эндоскопический индекс тяжести равен 8 баллам, то есть максимальный. Пациентка была переведена из инфекционной больницы, где исключалась инфекция кишечная, в наш специализированный стационар. Это тяжелая атака по индексу Трулов-Виттса, поэтому была назначена терапия внутривенными стероидами, но в течение двух недель ответа на терапию не было.
Пациентка не ухудшалась, поэтому всякий раз обсуждая оперативное лечение с колопроктологами, вопрос об операции откладывался, и индукции ремиссии было решено достичь антицитокиновой терапией, то есть пациентке назначен был ремикейд в связи с отсутствием ответа на внутривенные стероиды. Подключалась также терапия иммуносупрессорами азатиоприна. Пациентка ответила на индукционный курс и в течение практически 8 месяцев получала комбинированную терапию ремикейдом и азатиоприном. Проведено было 6 инфузий. Она получала ремикейд, азатиоприн, препараты 5-аминосаллициловой кислоты, и в сентябре сохраняющаяся клиническая ремиссия, но препарат исчезает в аптечной сети, и седьмая инфузия в ноябре не была проведена. Но пациентка оставалась в ремиссии, продолжала получать азатиоприн, препараты 5-аминосаллициловой кислоты, и когда через 3 месяца, в феврале 2010 года появляется ремикейд, вопрос встал, следует ли продолжать антицитокиновую терапию пациентке, находящейся в ремиссии. По обследованию нормальный кальпротектин, нормальное самочувствие, и решено воздержаться от продолжения инфузий и продолжить их в случае ухудшения самочувствия.
Пациентка приходит через год, в январе 2012 года. У нее нормальный кальпротектин, у нее нормальная эндоскопическая картина, проводится исследование на рыхлость, ранимость (…)(05:11), тест отрицательный, что говорит о хорошем, глубоком заживлении слизистой оболочки, гистологическая ремиссия также подтверждается, и пациентка просит отменить иммуносупрессоры в связи с тем, что среди побочных эффектов ей не нравится, она настороженно относится к перечисленным там побочным эффектам иммуносупрессоров. Продолжается терапия 5-аминосаллициловой кислоты, в течение года она получает уже «Мезавант». Сначала шла 1 таблетка, но после отмены иммуносупрессоров мы переходим на 2 таблетки «Мезаванта», и через год оценивается ремиссия клиническая по кальпротектину, и на сегодняшний день пациентка пребывает в состоянии ремиссии клинической и лабораторной ремиссии.
Почему в данном случае нам удалось уйти от азатиоприна? Азатиоприн показан в следующих ситуациях, говорит Консенсус последний по язвенном колиту: рецидивы, возникающие на фоне поддерживающей терапии адекватными дозами 5-аминосаллициловой кислоты, или непереносимость этих препаратов. Пациентка у нас не получала лечение, это была фульминантная атака язвенного колита, поэтому в данном случае, несмотря на то, что индукция ремиссии была достигнута ремикейдом, мы позволили себе уйти от азатиоприна и остаться на адекватных дозах 5-аминосаллициловой кислоты. Таким образом, особенностью данного клинического наблюдения является то, что это фульминантное начало язвенного колита. У пациентки была резистентность к внутривенным стероидам, что привело к необходимости подключить «спасательную» терапию как альтернативу колэктомии ремикейдом (инфликсимабом).
Ремиссия была достигнута комбинированной схемой – это ремикейд, азатиоприн, 5-аминосаллициловая кислота. Поддерживающая терапия осуществлялась азатиоприном и 5-аминосаллициловой кислотой. Ушли от ремикейда, потому что ранее она не получала азатиоприн, это согласуется с данными Консенсуса, и очень важным фактором является то, что пациентка была полностью привержена лечению. Наконец, отмена азатиоприна стала возможна при условии опять же таки приверженности поддерживающей терапии адекватным дозам 5-аминосаллициловой кислоты, ранее пациентка не получала до фульминантные атаки. Ну, и отказ от местных форм 5-аминосаллициловой кислоты с переходом на мультиматриксную форму месалазина («Мезавант») позволил достичь очень хорошей приверженности. Клинический случай – пациент 1987 года рождения. Также бросил курить, и где-то через 7 месяцев у двадцатиоднолетнего молодого человека повышается температура, учащается стул, лабораторная активность в виде ускорения СОЭ, повышение С-реактивного белка, также достаточно тяжелый эндоскопический индекс тяжести язвенного колита. Это язвенный колит распространенный, тоже тяжелое течение, высокая активность, и назначаются внутривенные стероиды для индукции ремиссии с последующим переходом на стероиды внутрь.
Назначается также азатиоприн, почему, потому что индукция проводится с назначением внутривенного преднизолона, поэтому обязательно подключаем сразу же азатиоприн, и получает он месалазин внутрь и ректально, комбинированную схему. Очень долго получает стероиды, постепенная отмена – 6 месяцев постепенно снижаем дозу, продолжает получать азатиоприн, месалазин, и после отмены стероидов развивается лейкопения на азатиоприне, в связи с чем мы вынуждены отказаться от этого препарата. Остается он на 5-аминосаллициловой кислоте, в общем-то, полная доза – 3 г внутрь и свечка «Салофальк» 0,5 г ректально. Контроль ремиссии. Чувствует он себя хорошо, контроль ремиссии осуществляется уровнем фекального кальпротектина, и без азатиоприна он удерживает ремиссию на месалазине, на комбинированных препаратах. Естественно, местное лечение не очень нравится молодому человеку, в связи с чем в начале 2011 года он переходит на назначение мультиматриксного месалазина («Мезаванта») в дозе 2 таблетки. Он приходит на контрольный визит в марте 2012 года, через год – нормальный фекальный кальпротектин, полностью зажившая слизистая оболочка с эндоскопическим индексом тяжести 0, и проведением пробы на рыхлость и кровоточивость – также она отрицательная, глубокая гистологическая ремиссия без базального плазмоцитоза.
Пациент продолжает принимать «Мезавант» 2 таблетки однократно утром, очень удобная схема. Он полностью привержен терапии, это его вполне устраивает, на сегодняшний день находится в ремиссии. Особенности этого клинического наблюдения: тяжелая атака, внутривенно преднизолон назначается для индукции ремиссии; стероидозависимость развивается, она преодолевается назначением азатиоприна. Поддерживающая терапия азатиоприном и препаратами 5-аминосаллициловой кислоты, к сожалению, невозможна из-за развития лейкопении, то есть миелотоксичности на фоне азатиоприна, и возможность отмены азатиоприна на фоне того, что пациент полностью привержен терапии 5-аминосаллициловой кислотой. И сразу подчеркнем, что до начала болезни, до появления первых симптомов он был нелеченым пациентом 5-аминосаллициловой кислотой, поэтому мы спокойно можем уйти от азатиоприна. Ну, и отказ от местных форм 5-аминосаллициловой кислоты, назначением месалазина мультиматриксного только внутрь, да еще раз в день, это очень удобно, позволило достичь прекрасной приверженности.
И, наконец, третий случай – пациентка со средней степенью тяжести язвенного колита, двадцатидевятилетняя больная. Появился стул более слабый с примесью крови, эндоскопический индекс тяжести – 5 баллов. Назначена была стандартная терапия – это месалазин внутрь и в клизмах, с быстрым достижением ремиссии – фактически за 2 месяца пациентка чувствовала себя уже прекрасно и бросила принимать эти препараты, то есть перестала принимать. На этом фоне развивается обострение, с ускорением СОЭ, с эндоскопической активностью, и пациентке рекомендован все-таки прием индукционного курса месалазина 3 г и свечка 2 раза в день ректально месалазина для индукции ремиссии. Ремиссии она достигает достаточно быстро, но затем начинает опять же таки то принимать, то не принимать месалазин, то ставит свечку, когда появляется кровь, то перестает ее ставить. И когда она пришла в очередной раз на прием – это был январь 2011 года – с ней проведена была жесткая беседа о необходимости сохранения ремиссии, что появление крови в стуле – это только вершина айсберга, что сохраняющееся воспаление в слизистой приводит к совершенно ненужным, грозным последствиям. Назначена была стандартная индукционная вновь доза – 3 г внутрь и 0,5 г ректально, достигнута была очень быстро ремиссия, и настолько она хорошо себя чувствовала, что опять начала сомневаться в терапии. Обратилась буквально через 3 месяца, можно ли что-то сделать с ректальными формами, не нравятся ей свечки. Назначена была поддерживающая ремиссию терапия мульматриксиным месалазином («Мезавантом»), всего одна таблетка, хотя в инструкции к препарату указывается, что поддержание ремиссии обеспечено должно быть 2 таблеточками, 2,4 г в сутки.
Но учитывая, что у пациентки не было тяжелых каких-то симптомов проктита, и она очень хорошо отвечала на терапию 5-аминосаллициловой кислотой, вполне достаточно для нее одной дозы 1,2 г поддерживающей оказалось. Она пришла через почти год – нормальный кальпротектин, полностью привержена терапии, и на следующий год, вот в январе 2013 года, обращается к нам с вопросом, что ей делать, она собирается беременеть. Она вообще сомневается, есть ли у нее язвенный колит, что так она себя прекрасно чувствует, может быть, ей с этой таблеточкой, уже и прекращать ее принимать. Мы отправляем пациентку на исследование. Клиническая ремиссия подтверждается эндоскопической ремиссией, отсутствует рыхлость, ранимость при проведении теста давлением на слизистую оболочку, морфолог нам доказывает, что здесь нет базального плазмоцитоза, то есть полная глубокая гистологическая ремиссия, и пациентке предложено продолжать месалазин одну таблетку постоянно, планировать беременность.
Это вполне допустимый препарат, и даже нужно его принимать, обязательно защищать слизистую на момент беременности, родов и кормления. Контролировать фекальный кальпротектин – она это делает, данные в 2013 году, на январь 2014-го вполне нас устраивают, и рекомендовано контролировать фекальный кальпротектин каждые 4-6 месяцев. Продолжать принимать «Мезавант» одну таблетку, и если будет повышение уровня фекального кальпротектина, добавить свечи с 5-аминосаллициловой кислотой. В данном случае локализация язвенного колита была левосторонняя, но вовлечена была слепая кишка, поэтому ограничиться топическим месалазином мы не могли, нам обязательно нужно было назначать терапию и внутрь 5-аминосаллициловой кислоты. И основным фактором отсутствия стойкой ремиссии являлось отсутствие приверженности лечению. Пациентке не нравилось большое количество таблеток, не нравились ректальные формы, и отказ от ректальных форм, перевод на фактически одну таблетку в день утром, не обременяющую, так скажем, по жизни, привел к хорошей приверженности.
И два последних слайда. Мы часто сталкиваемся в нашем центре с тем, что пациентам очень неадекватно, не всегда вовремя назначаются стероиды. Что говорит об этом Консенсус? Когда назначать стероиды пациентам? Как нужно оценивать правильно ответ на терапию 5-аминосаллициловой кислотой? Стероиды назначаем в том случае, если ухудшение наступает на адекватной дозе месалазина. То есть когда назначается более 2 г в сутки, а пациент ухудшается, тогда подключаем стероиды. Следующая ситуация – когда нет улучшения в течение 10-14 дней терапии месалазином, то есть сохраняется примесь крови в стуле, обсуждаем вопрос о назначении стероидов. И, наконец, если к 4-6 неделе тоже нет полного клинического ответа, то есть сохраняется кровь в стуле. Интересное исследование, которое проводилось по «Мезаванту», по мультиматриксному месалазину. Пациенты, которые не ответили к 8-й неделе на прием «Мезаванта», достигали клинической ремиссии в 60% случаев в последующие 8 недель. То есть если они 8 последующих недель принимали максимальную дозу препарата – это 4 таблетки, 4,8 г – 60% из тех, кто не ответил к 8-й неделе, отвечали в течение последующих 8 недель. Это очень важная информация для клиницистов. То есть если пациент не ухудшается, то медленно и верно нужно пытаться дождаться этих еще 8 недель, потому что у всех заживление идет разным темпом, у всех немножко разный ответ со стороны слизистой на терапию.
Наконец, мы говорим, что левосторонний язвенный колит, в общем-то, можно лечить топически, назначая клизмы или пену, но Консенсус в этом случае говорит, что можно попытаться начать терапию в случае легкого язвенного колита, средней степени тяжести, назначая мультиматриксный месалазин, который охватывает не только восходящий, поперечно-ободочный отдел ободочной кишки, нисходящую кишку, и в прямой кишке, в общем-то, достаточно 5-аминосаллициловой кислоты. Поэтому можно начать с таблетированных форм, и только в том случае, если сохраняется симптоматика, не заживает прямая кишка, добавить топические формы. Спасибо за внимание.
Источник
