Кандидурия и кандидоз мочевыводящих путей
Медицинский эксперт статьи

х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Кандидоз мочевыводящих путей обычно возникает у больных с факторами риска, чаще в качестве внутрибольничной инфекции.
Кандидоз и колонизация мочевыводящих путей – факторы риска развития инвазивного кандидоза.
 [1], [2], [3], [4], [5], [6], [7]
[1], [2], [3], [4], [5], [6], [7]
Код по МКБ-10
B37.4 Кандидоз других урогенитальных локализаций
Причины кандидоза мочевыводящих путей
Сахарный диабет, катетеризация мочевого пузыря, мочекаменная болезнь, длительный приём антибиотиков широкого спектра действия, могут послужить причиной заболевания.
 [8], [9], [10], [11], [12]
[8], [9], [10], [11], [12]
Симптомы кандидоза мочевыводящих путей
Для кандидозного цистита характерно частое болезненное мочеиспускание. Для кандидозного пиелонефрита характерны боли в поясничной области, повышение температуры тела и боль при мочеиспускании.
 [13], [14], [15], [16], [17]
[13], [14], [15], [16], [17]
Диагностика кандидоза мочевыводящих путей
Диагностика кандидоза мочевыводящих путей основана на выявлении Candida spp. в моче и оценке состояния больного. Важно правильно понимать клиническое значение выявления Candida spp. в моче. У большинства больных возникает бессимптомная кандидурия, свидетельствующая о колонизации Candida spp. нижних отделов мочевыводящих путей, данное обстоятельство не считают показанием для применения антимикотиков (достаточно устранения или коррекции факторов риска).
Кандидурия в сочетании с клиническими или инструментальными признаками инфекции мочевыводящих путей – показание для применения противогрибковых препаратов. Кроме того, кандидоз мочевыводящих путей может быть источником, а кандидурия – проявлением инвазивного кандидоза. Именно поэтому при высоком риске развития инвазивного кандидоза (наличие факторов риска, предполагаемых клинических признаков) показано дополнительное обследование и решение вопроса о назначении противогрибковой терапии.
 [18], [19], [20], [21]
[18], [19], [20], [21]
Лечение кандидоза мочевыводящих путей
Лечение проводят больным с клиническими признаками инфекции мочевыводящих путей или с бессимптомной кандидурией и наличием факторов риска развития инвазивного кандидоза. Лечение кандидоза мочевыводящих путей состоит в применении системных антимикотиков, удалении или замене мочевых катетеров, в устранении или уменьшении выраженности других факторов риска (оптимизации применения антибактериальных препаратов, коррекции сахарного диабета и т. д.). Препарат выбора – флуконазол, в отличие от других антимикотиков он создает высокую концентрацию активного вещества в моче. При неэффективности флуконазола используют промывание мочевого пузыря раствором амфотерицина В (50-200 мкг/мл), обычно сопровождающееся временным прекращением кандидурии, однако данный метод лечения неэффективен при поражении вышележащих отделов мочевыводящих путей. При неэффективности флуконазола и возможном поражении паренхимы почек применяют каспофунгин или вориконазол.
При бессимптомной кандидурии у пациентов без факторов риска развития инвазивного кандидоза антимикотики не применяют. Устранение или уменьшение выраженности факторов риска кандидоза мочевыводящих путей (удаление или замена мочевого катетера, оптимизация применения антибактериальных препаратов, коррекция сахарного диабета и так далее) обычно приводит к устранению бессимптомной кандидурии.
Источник

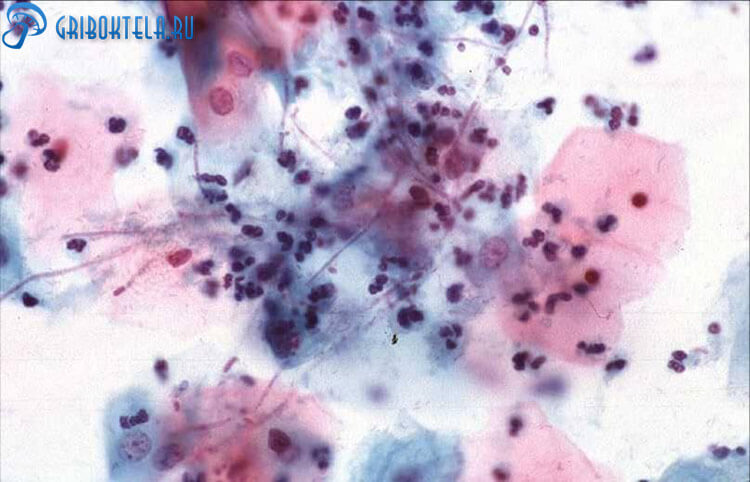
Кадидурия – болезнь, вызванная дрожжевыми грибками Candida spp., оккупирующая слизистые оболочки мочевыделительной системы человека. Кандидоз мочевыводящих путей — это наличие в моче кандидозных штаммов, подтвержденное как минимум двукратным лабораторным исследованием и сочетающееся с клиническими проявлениями.
Возбудитель и пути передачи
О проникновении грибковой флоры в мочевые пути известно уже более полувека, однако до последнего времени существуют трудности в ее распознавании, а соответственно сложности в подборе адекватного лечения.
По мнению врачей наиболее склонным к возбуждению патологического процесса является вид Кандида альбиканс. Более половины патологий дислоцирующихся в мочевом пузыре, мочеточниках, почках связывают именно с ним. Иные формы возбудителя составляют от 4 до 16%, редко одновременно сочетаясь друг с другом.
Причины заражения
Главным фактором, способствующим развитию недуга, остается понижение защитных сил организма, которое происходит из-за перенесенных инфекций, сахарного диабета, обострения хронических заболеваний (в том числе имеющихся в анамнезе грибковых поражений), оперативных вмешательств, внутрибольничной инфекции.
Характерно, что кандидурия в 75-80% случаев — проблема пациентов реанимационных отделений. Кандидурия, прежде всего, вызывается ежедневно проводимой катетеризацией. В результате манипуляции грибки беспрепятственно мигрируют по катетеру, нарушается целостность (микротравмы) слизистой уретры и кожи промежности. Отметим, что всего за пару недель после госпитализации явно обнаруживаются следы кадидурии.
Значительный фактор риска появления кандидурии – индивидуальные особенности (аномалии) строения и функционирования данных органов.
Провоцирует активное размножение молочницы длительно проводимая антибиотико и гормонотерапия, иммунодепрессанты.
Не исключается возможность инфицирования половым путем от больного кандидозом к здоровому партнеру. Частенько таким путем формируется кандидоз мочевого пузыря.
Симптоматика
Клиника во многом зависит от места расположения колоний грибка-паразита. Чаще других регистрируется молочница (кандидоз) в мочевом пузыре. Не смотря на то, что клетки Кандиды быстро захватывают обширные участки слизистой, кандидурия нередко протекает бессимптомно. Особенно это касается пациентов после пересадки органов и оперативных вмешательств, новорожденных с низкой массой и больных нейтропенией (снижение количества нейтрофилов, помогающих бороться с инфекциями).
На втором месте по частоте случаев фиксируется грибковый цистит, который мало чем отличается от бактериального. Острый диссеминированный кандидоз (ОДК) опасен тем, что кроме воспаления на слизистой мочевого пузыря и уретры образовываются грибковые скопления-папилломы, мешающие нормальной работе органов. Пытаясь справиться с кандидой, организм заболевшего быстро реагирует:
- повышается температура тела до субфебрильных значений (38°С и выше);
- появляются ноющие боли в пояснице, рези внизу живота;
- болезненное мочеиспускание;
- ложные и частые позывы;
- задержка мочи;
- снижается качество мочи (мутная моча, следы крови, кисловатый запах);
- иногда начинаются зуд и раздражение (слизистой влагалища, половых губ и кожи промежности у женщин, головки полового члена у мужчин);
- ухудшается общее самочувствие (плохой сон, раздражительность, головная боль, потеря аппетита).
Поражение непосредственно почек происходит только у тяжелобольных пациентов с подтвержденной кандидурией, и составляет всего 2 процента случаев.
Важно! Только доктор (уролог, гинеколог) точно диагностирует заболевание с учетом всех данные о течении болезни и по результатам предварительных анализов.
Диагностика

Для окончательного установления диагноза необходимо провести ряд процедур:
- визуальный осмотр, сбор анамнеза;
- многократный анализ мочи для посева на питательную среду с целью выявления разновидности штамма, чувствительности его к антигрибковым препаратам (под микроскопом);
- сдача крови на наличие антител и антигена и общий анализ крови (ОАК);
- по необходимости: ультразвуковое исследование (УЗИ), компьютерная томография (КТ), цистоскопия (эндоскопия мочевого пузыря с помощью специального катетера).
Лечение
Лечение заболевания во многом направлено на сокращение или уничтожение рисков возникновения недуга.
Поскольку ОДК в настоящее время в 50% случаев протекает со смертельным исходом, рекомендуется антимикотическая терапия. Только при бессимптомной форме кандидурии она не совсем целесообразна.
Терапевтические мероприятия предполагают комплексный подход. Кроме своевременной замены изделий медицинского назначения, соблюдения антисептики, приема противокандидозных лекарств, нужно правильное ведение сопутствующих болезней (прием инсулина, антибиотиков, гормонов и т.п.).
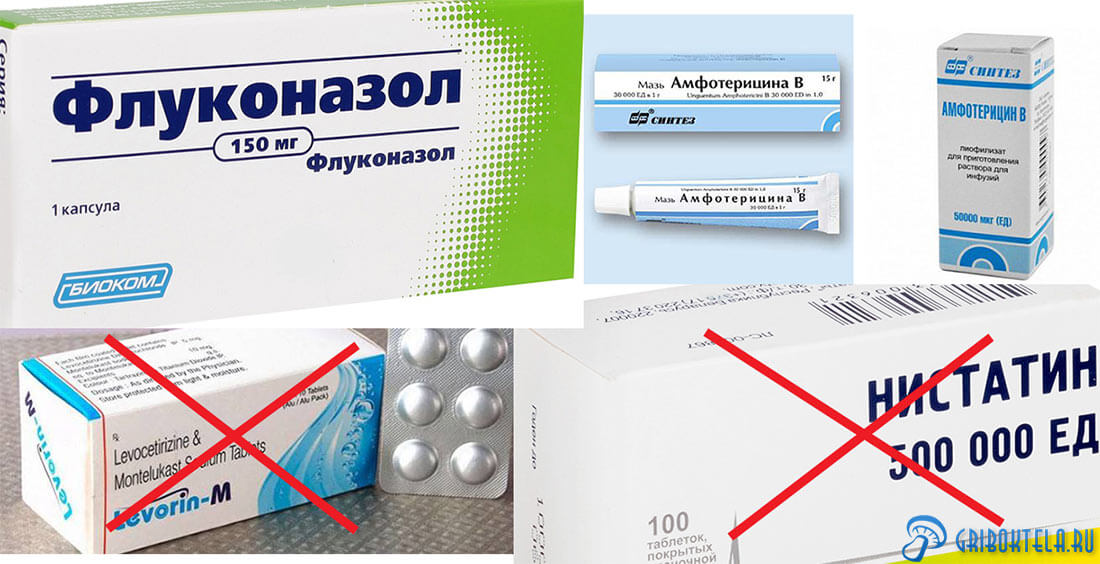
Высокую эффективность в устранении хвори показали флуконазол и амфотерицин В. Медики считают ошибочным использование нистатина и леворина, так как они очень слабо всасываются в ЖКТ и не попадают в мочу.
| Флуконазол | Амфотерицин |
| Противогрибковый препарат широкого спектра действия растворимый в воде (Дифлюкан). При пероральном приеме (через рот) способен находится в организме до 30 часов. Выпускается в капсулах, удобен и прост в применении. На 80% выводится с мочой. Безопасен при нарушениях функции почек. У детей назначается с учетом веса, дозой в 3 мг на кг в сутки, взрослым – 200 мг. В тяжелых случаях вводится внутривенно в растворе. Курс лечения варьирует от недели до двух недель, до полного исчезновения симптоматики. | Гиперактивен по отношению к большинству возбудителей заболевания. Не смотря на низкую концентрацию в моче достаточно эффективен. Однако имеет много противопоказаний и побочных эффектов. Применяется для капельниц. Прописывают при тяжелом течении и невозможности употребления флуконазола. Максимальная дозировка – 0,3-1 мг/кг/в сут. Длительность – до 7 суток. |
Рекомендации
При заболеваниях почек и мочевыводящих путей необходимо соблюдение диеты с пониженным содержанием соли и белка (стол №7). Диетологи утверждают, что нежирное мясо, птица и рыба в отварном виде, каши и молочные продукты помогают быстрее выздороветь. А вот, алкоголь, сладости, газированные напитки, острое и копченое могут навредить.
Подспорьем основному лечению становятся настои и отвары из сборов целебных трав: цветков ромашки, листьев толокнянки, брусники и клюквы, травы хвоща, горца птичьего (спорыша) для внутреннего и наружного применения.
Частые вопросы FAQ
Можно ли заболеть кандидурией, если периодически дает о себе знать молочница во влагалище?
Как подготовиться к сдаче анализа мочи?
А у мужиков такая зараза часто бывает?
Источник
Введение
Инфекции мочевыводящих путей (ИМП) относят к числу наиболее распространенных заболеваний в урологической практике. Согласно статистическим данным, ИМП являются причиной более 7 млн. обращений к врачам амбулаторной практики в США ежегодно. На долю ИМП приходится более 40% от всех нозокомиальных инфекций, и в большинстве случаев они являются катетер–ассоциированными [2,3]. Осложненные ИМП возникают у пациентов с обструктивными уропатиями, на фоне инструментальных (инвазивных) методов обследования и лечения, при наличии инородных тел (дренажей) в мочевых путях и тяжелых сопутствующих заболеваниях (сахарный диабет, нейтропения). Нозокомиальные ИМП могут вызывать не только облигатные, но и оппортунистические возбудители со сравнительно невысоким потенциалом патогенности, особенно у пациентов с иммунодефицитами. За последние десятилетия в этиологической структуре нозокомиальных ИМП отмечается возрастание роли грибковой инфекции [2]. По данным исследований, проведенных Richards M.J. с соавт. (1998), у больных блоков интенсивной терапии хирургических отделений, ИМП в 95–97% случаев возникали при наличии постоянного уретрального катетера, при этом у 31% больных в моче выявляли грибковую инфекцию.
Инфекции мочевыводящих путей (ИМП) относят к числу наиболее распространенных заболеваний в урологической практике. Согласно статистическим данным, ИМП являются причиной более 7 млн. обращений к врачам амбулаторной практики в США ежегодно. На долю ИМП приходится более 40% от всех нозокомиальных инфекций, и в большинстве случаев они являются катетер–ассоциированными [2,3]. Осложненные ИМП возникают у пациентов с обструктивными уропатиями, на фоне инструментальных (инвазивных) методов обследования и лечения, при наличии инородных тел (дренажей) в мочевых путях и тяжелых сопутствующих заболеваниях (сахарный диабет, нейтропения). Нозокомиальные ИМП могут вызывать не только облигатные, но и оппортунистические возбудители со сравнительно невысоким потенциалом патогенности, особенно у пациентов с иммунодефицитами. За последние десятилетия в этиологической структуре нозокомиальных ИМП отмечается возрастание роли грибковой инфекции [2]. По данным исследований, проведенных Richards M.J. с соавт. (1998), у больных блоков интенсивной терапии хирургических отделений, ИМП в 95–97% случаев возникали при наличии постоянного уретрального катетера, при этом у 31% больных в моче выявляли грибковую инфекцию.
Особенно отчетливо тенденция увеличения числа системных инфекций, вызванных грибковыми патогенами, прослеживается у больных, перенесших трансплантацию органов, страдающих гемобластозами, ВИЧ–инфекцией, а также нейтропенией. В значительной степени это связано с внедрением в клиническую практику антимикробных препаратов широкого спектра действия, применением аппаратов для искусственной вентиляции легких, внутривенных и уретральных катетеров у больных в отделениях интенсивной терапии [1–3]. Предрасполагающие к развитию грибковых ИМП факторы представлены в таблице 1. Необходимо отметить, что у больных с нейтропенией системные микозы встречаются чаще и являются главной причиной ухудшения общего состояния и летальных исходов в 40–60% случаев [5].
Этиологическая структура
грибковых ИМП
По данным Sobel J.D. с соавт. (1999), наиболее частыми грибковыми патогенами в моче являются грибы рода Candida. Среди видов Candida наиболее частым возбудителем инфекционных заболеваний является Candida albicans (более 50% случаев) [2,3,6]. В последнее время наблюдается тенденция увеличения частоты и других представителей рода Candida: C. glabrata, C. tropicalis, C. parapsilosis, C. krusei и др. Это связано с широким и нерациональным использованием препаратов азолов первой генерации, в основном флуконазола, широко применяющегося для лечения кандидоза различных локализаций. Среди иммунных механизмов ключевое значение в защите от грибковых патогенов рода Candida принадлежит Т–клеточному звену иммунитета [7]. Именно с этим фактом связывают широкое распространение кандидоза мочевыводящих путей у больных с нейтропенией, гемобластозами и ВИЧ–инфекцией, а также после трансплантации органов.
Также известны случаи выявления в моче Cryptococcus neoformans, разновидностей Aspergillus и возбудителей эндемичных микозов. Выявление в моче Cryptococcus neoformans и Aspergillus, чаще всего свидетельствует не об изолированном поражении мочевыводящих путей, а о диссеминированном микозе с поражением почек, и характерно для больных с выраженными нарушениями иммунитета, в основном при ВИЧ–инфекции, гемобластозах, после трансплантации органов [11,12].
Диагностика грибковых ИМП
Кандидурией называется выявление в моче Candida spp. в титре > 103 КОЕ/мл в двух последовательных образцах мочи с интервалом не менее 24 часов [2,10]. Сама по себе кандидурия не является признаком поражения мочевыводящих путей. В большинстве случаев кандидурия не сопровождается какими–либо симптомами и связана с восходящей колонизацией мочевых путей по дренажу (уретральные катетеры, цистостомические дренажи, стенты, нефростомические дренажи) или у женщин из контаминированной вульвовагинальной области. Данное состояние не требует применения системных противогрибковых препаратов. Однако в ряде случаев кандидурия может быть первым клиническим проявлением системного кандидоза с поражением почек [2,3,9].
Кандидозом мочевыводящих путей считается сочетание кандидурии с симптомами поражения мочевыводящих путей. В основном это дизурические расстройства, но также может наблюдаться и гематурия. Необходимо отметить, что такие состояния возникают достаточно редко. Цистоскопическая картина при этом будет соответствовать очаговому или распространенному кандидозному поражению в виде мягких, белесоватых, приподнятых над поверхностью участков на фоне воспалительно–измененной слизистой. Кандидоз мочевыводящих путей, а тем более системный кандидоз, нуждаются в обязательном применении противогрибковых препаратов. Поэтому при выявлении кандидурии необходима комплексная диагностика, направленная на исключение кандидоза мочевыводящих путей [2,3]. Методы диагностики кандидоза мочевыводящих путей обобщены в таблице 2.
При кандидозной инфекции верхних мочевых путей основные симптомы схожи с таковыми при бактериальном поражении. Восходящая инфекция почти всегда наблюдается при нарушениях уродинамики, наиболее часто – у пациентов с сахарным диабетом и мочекаменной болезнью [3]. Среди осложнений пиелонефрита при кандидозной инфекции наиболее важным следует считать возникновение обструкции верхних мочевых путей грибковым конгломератом (безоаром), при этом наблюдается клиническая картина почечной колики. В исходе острого и хронического пиелонефрита возможно присоединение некротического папиллита. Кандидемия редко является следствием кандидурии и, как правило, развивается вследствие обструкции мочевыводящих путей [3,9]. Резистентность к антимикробным препаратам широкого спектра действия, повышение температуры тела более 38°С, септический шок, а также острая дыхательная или почечная недостаточность являются основными клиническими проявлениями кандидемии и острого диссеминированного кандидоза [1,3]. Точная диагностика инвазивного кандидоза остается довольно сложной проблемой. Обязательной ее составляющей должно быть выявление факторов риска развития острого диссеминированного кандидоза. Целью лабораторной диагностики должно быть определение вида возбудителя и его чувствительности к антимикотическим препаратам, для этого производятся многократные посевы крови и материала из очагов поражения на специальные питательные среды.
Таким образом, у большинства больных выявление грибов Candida в моче в титре 103 КОЕ/мл является бессимптомным или малосимптомным проявлением колонизации мочевыводящих путей. С другой стороны, кандидозная инфекция мочевыводящих путей может сопровождаться наличием рентгенологически подтвержденных безоаров. У больных с обструктивной уропатией кандидурия может быть источником последующей диссеминации или маркером острой гематогенной диссеминации [3].
Терапия ИМП
Лечение бессимптомной кандидурии у катетеризированных больных без нейтропении не имеет никакой практической ценности. Известно, что С. albicans обладает хорошей чувствительностью к флуконазолу, тогда как C. krusei зачастую к нему резистентна, а у C. glabrata может определяться дозозависимый эффект при применении флуконазола [1,2]. Терапия флуконазолом быстро устраняет кандидурию примерно у 50% больных, но при этом достаточно часто возникают рецидивы, а также возможно развитие селекции резистентных штаммов грибов рода Candida. Микробиологические результаты у больных, перенесших лечение и без него, были сопоставимы. У больных с кандидурией замена дренажа приводит к устранению кандидурии лишь в 20% случаев; тем не менее удаление катетера может привести к исчезновению кандидурии почти у 40% больных [2,3,9].
Внутрипузырное введение раствора амфотерицина B долгое время было стандартом терапии при фунгурии. Однако результаты исследований Gubbins P.O. с соавт. (1999) демонстрируют, что и внутрипузырное введение амфотерицина B и пероральная терапия флуконазолом в равной степени эффективны для купирования фунгурии. Внутрипузырное введение амфотерицина B, как оказалось, действует более быстро, однако эффект системной терапии флуконазолом часто сохраняется дольше, чем после инстилляции амфотерицина B. Кроме того, пероральная терапия более удобна и экономически приемлема. Эффект от пероральной терапии флуконазолом наступает отсроченно, но сохраняется более длительно, чем после внутрипузырного введения раствора амфотерицина B. По данным Jacobs L.G. с соавт. (1996), у пожилых пациентов уровень смертности, связанной со всеми причинами, после проведенного курса лечения фунгурии был выше среди больных, получавших лечение в виде инстилляций в мочевой пузырь амфотерицина В, чем среди тех, кто получал пероральную терапию флуконазолом (41% к 22% соответственно). Таким образом, местная терапия может быть связана с более низкими показателями выживаемости. Внутрипузырное введение раствора амфотерицина B (50–200 г/мл) показано лишь в редких случаях, исключительно в качестве диагностического, локализационного теста [8].
Кандидурия может быть первым, единственным микробиологическим проявлением диссеминированного кандидоза. В случае диагностики диссеминированного кандидоза в настоящее время рекомендуется применение таких препаратов, как амфотерицин B, флуконазол, или каспофунгин [9]. Противогрибковые препараты в обязательном порядке должны применяться у больных с высоким риском диссеминированного кандидоза: с нейтропенией, у младенцев с дефицитом веса, у больных с почечными аллотрансплантатами, а также у больных после урологических операций. Курс противогрибковой терапии должен продолжаться не менее 7–14 дней. При отсутствии почечной недостаточности эффективно пероральное применение флуцитозина в дозе 25 мг/кг 4 раза в сутки, особенно у больных с кандидозом мочевыводящих путей, вызванным разновидностями кандид, отличными от Candida albicans. Однако его назначение может привести к формированию резистентности патогенных штаммов Candida. Флуконазол при этом должен применяться в дозе 200 мг/сут. в течение 7–14 дней, а амфотерицин B деоксихолат – в дозе от 0,3 до 1,0 мг/кг/сут. в течение 17 дней.
Таким образом, неадекватная терапия может способствовать формированию резистентных микроорганизмов. У больных с лихорадкой неясного генеза при наличии бессимптомной кандидурии показано проведение противогрибковой терапии в связи с возможным скрытым диссеминированным кандидозом [9].
В связи с тем, что кандидурия часто развивается на фоне мочекаменной болезни, пиелонефрита, антибиотикотерапии инфекционных заболеваний мочевыводящей системы и сопровождается явлениями дизурии, рационально проведение лечебно–профилактических мероприятий с использованием препаратов, обладающих комплексным антисептическим, литолитическим, диуретическим и противовоспалительным действием. В этом отношении перспективным представляется использование фитотерапии и растительных препаратов. К таким препаратам относится комплексное лекарственное средство Цистон (Хималайя Драг Ко).
Это комбинированный растительный препарат. Оказывает диуретическое, спазмолитическое, литолитическое, противомикробное и противовоспалительное действие. Препарат регулирует кристалло–коллоидный баланс при дисметаболической нефропатии, снижает концентрацию в моче элементов, способствующих образованию камней (щавелевая кислота, кальций, гидроксипролин). Повышает уровень элементов, которые ингибируют процесс образования камней (натрий, магний, калий). Воздействуя на муцин, препарат способствует дезинтеграции камней, приводит к их деминерализации. Препятствует аккумуляции частиц вокруг ядра камня, что предотвращает его дальнейший рост. Стимулируя диурез и расслабляя гладкую мускулатуру мочевого тракта, Цистон способствует выведению оксалатных и фосфатных солей, мочевой кислоты и мелких камней из мочевыводящих путей. Цистон оказывает бактериостатическое и бактерицидное действие, особенно в отношении Klebsiella spp., Pseudomonas aeruginosa, Escherichia coli и других грамотрицательных бактерий. Литолитический эффект препарата не зависит от рН мочи. Цистон назначается по 2 таб. 2 раза/сут. Особенно эффективно применение препарата при сопутствующих кандидурии, мочекаменной болезни, кристаллурии, циститах и пиелонефритах.
Постоянная кандидурия у иммунокопрометированных пациентов требует проведения дообследования в объеме цистоскопии, УЗИ и КТ почек. Длительное использование уретрального катетера, несмотря на проводимую противогрибковую терапию, может способствовать развитию частых рецидивов кандидозной инфекции [9].
Заключение
Несмотря на увеличение частоты выявления грибковых патогенов в моче, а также важную роль системной инфекции в структуре заболеваемости и смертности больных столь сложной категории, возможности адекватной диагностики и своевременного выбора метода лечения в большинстве стационаров явно ограничены. Широкое и нерациональное применение антимикотиков в лечении грибковых инфекции приводит к появлению и распространению резистентных штаммов. В связи с этим проблема диагностики и лечения инфекций мочевыводящих путей, проблема выбора оптимального препарата, безусловно, требует пристального внимания специалистов и продолжения поиска новых стратегий ее решения.
Литература
1. Пестова Л.А. Кандидемия и острый диссеминированный кандидоз у больных в отделениях интенсивной терапии. Автореферат диссертации на соискание ученой степени кандидата медицинских наук, Санкт–Петербург, 2004г.
2. Климко Н.Н. Кандидурия и кандидоз мочевыводящих путей: врачебная тактика. Рациональная антимикробная терапия для практического врача. Том 04/N 3/2002
3. Белобородов В.Б., Синякова Л.А. Нозокомиальная кандидурия: алгоритм диагностики и лечения. Consilium medicum Том 05/N 7/2003
4. Ostrosky–Zeichner L, Pappas PG. Invasive candidiasis in the intensive care unit. Crit Care Med. 2006 Mar;34(3):857–63
5. Eggimann P, Garbino J, Pittet D Management of Candida species infections in critically ill patients. Lancet Infect Dis. 2003 Dec;3(12):772–85
6. Krcmery S, Dubrava M, Krcmery V Jr. Fungal urinary tract infections in patients at risk. Int J Antimicrob Agents. 1999 May;11(3–4):289–91
7. Лебедева Т.Н. Иммунитет при кандидозе (обзор). Проблемы медицинской микологии. – 2004. – Т.6, №4 – С.8–16.
8. Fong I.W. The value of a single amphotericin B bladder washout in candiduria. J. Antimicrob. Chemother. 1995; 36: 1067–71.
9. Peter G. Pappas, John H. Rex, Jack D. Sobel, Scott G. Filler, William E. Dismukes, Thomas J. Walsh, John E. Edwards. Практическое руководство по лечению кандидоза. Clinical Infection Diseases – 2004 –Vol. 38–P. 161–189.
10. Richardson MD, Kokki M. Therapeutic guidelines in systemic fungal infections. London: Current Medical Literature Ltd, 1998.
Источник
