Цикл кори биологическое значение
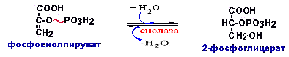
Глюконеогенез
– это образование глюкозы вновь
из неуглеводных компонентов: пирувата,
лактата,гликогенных аминокислот,
глицерина,любого соединения, которое
в процессе катаболизма может быть
превращено в пируват или один из
метаболитов цикла Кребса.
Глюконеогенез
протекает в: печени, корковом веществе
почек,слизистой кишечника.За счёт
глюконеогенеза в условиях углеводного
голодания образуется 80 г глюкозы.
Глюконеогенез–это
частично обращённый гликолиз.
Три
реакции гликолиза необратимы, поэтому
используются другие ферменты.
Пируваткиназная реакция заменяется
двумя:пируваткарбоксилазной реакцией
и фосфоенолпируваткарбоксикиназной
реакцией.

Между
этими реакциями существует челночный
механизм.ЩУК не может самостоятельно
выйти из митохондрий.ЩУК + НАДН+Н =
малат + НАД. В цитоплазме малат окисляется
цитоплазматической малатдегидрогеназой
до ЩУК

От
ФЕП до ФФК реакции все реакции идут в
обратной последовательности
гликолиза:Фосфофруктокиназная реакция
заменяется фруктозодифосфатазной
реакцией.
Биологическая
роль глюконеогенезаизбавление от
лактата (85% лактата идёт на глюконеогенез,
15% – окисляется до СО2, Н2О и энергии),
связь обменов, получение эндогенной
глюкозы.
Итоговое
уравнение глюконеогенеза
2
лактата + 6АТФ + 4Н2О + 2НАДН+Н глюкоза
+ 6АДФ + 6Фн + 2НАД
АТФ
используется в пируваткарбоксилазной,
фосфоенолпируваткарбоксикиназной,
фосфоглицераткиназной реакциях. НАДН+Н
необходим для ГАФДГ. 2Н20 участвуют в
енолазной реакции. 2Н20 – в фосфатазных
реакциях.
Регуляция
глюконеогенеза4 фермента определяют
скорость процесса. При уменьшении АТФ
и НАД тормозится глюконеогенез. Ключевые
ферменты стимулируются АТФ,ингибируются
– АДФ и АМФ. Инсулин – репрессор ферментов
глюконеогенеза.Процесс активируется:
глюкокортикоидами, жирными кислотами,
избытком лактата в крови, глюкагоном.
Цикл
Кори
осуществляет связь между
гликолизом в мышце при активной работе
и глюконеогенезом в печени. При работе
лактат поступает из мышц в кровь и
печень.
Мышца
Кровь
Печень
3)Больной 50 лет поступил в клинику с жалобами на резкие боли в области сердца, слабость. Активность каких ферментов следует определить в крови больного для исключения инфаркта миокарда?
МБ+КФК
ЛДГ
АСТ/АЛТ
Миоглобин
тропонин
Билет
23
1)Холестерин, его биологическая роль, биосинтез. Гиперхолестеринемии. Атеросклероз.
Холестерин:
циклический
ненасыщенный спирт,нерастворим
в воде,в
основе холестерина лежит кольцо
циклопентанпергидрофенантрена.
Содержится
в: коре надпочечников, мозге, нервной
ткани, мышцах, соединительной ткани,
жировой ткани.
Биороль:
синтез
желчных кислот,синтез
половых гормонов,синтез
кортикостероидов,синтез
витамина D3,входит
в состав клеточных мембран, миелиновых
оболочек,участвует
в образовании желчных камней, развитии
атеросклероза.
Пищевые
источники холестерина:
печень,
яйца,
мясо,
мозг,
икра.
Синтезируется
в:
эндоплазматическом
ретикулуме, цитозоле печени (80%),
коже,
стенке
тонкой кишки.
Синтез
холестерина:
включает
35 реакций,идёт
в 3 стадии:
образование
из ацетил-КоА мевалоновой кислоты,образование
из мевалоновой кислоты сквалена,циклизация
сквалена в холестерин.
Холестеринемии:
1)Наследственная.
В
сыворотке крови увеличено содержание
холестерина, β-липопротеинов
Механизм
развития заболевания– отсутствие
или снижение количества рецепторов
клеток к ЛПНП, снижается захват и
катаболизм холестерина из ЛПНП,
увеличивается содержание холестерина
в плазме, оседание холестерина на стенки
сосудов, развитие атеросклеротических
бляшекОсложнения– ранний инфаркт миокарда, ксантоматоз,
инсульт
2)
Алиментарная гиперхолестеринемиявозникает от избытка в питании холестерина
3)Вторичная
гиперхолестеринемиявозникает
при гипотиреозе, сахарном диабете,
подагре, нефротическом синдроме
Атеросклероз:
Заболевание,
связанное с накоплением холестерина
в интиме сосудов с последующей
дегенерацией, отложением в очаг поражения
солей кальция, фиброзированием очага
и тромбозомДиагностические
критерии:гиперлипидемия,
гиперхолестеринемия
изменение
состава и соотношения транспортных
форм холестерина (увеличение ЛПНП и
уменьшение ЛПНП)Снижение
соотношения фосфолипиды
холестерин
Снижение
активности липопротеинлипазыУменьшение
в составе триацилглицеринов
полиненасыщенных жирных кислот и эфиров
холестерина
Способствуют
развитию атеросклероза:
наследственная
предрасположенность
гипертония
сахарный
диабет
ожирение
стрессы
гиподинамия
нарушение
равновесия свертывающей и противосвертывающей
системы крови.
Соседние файлы в предмете Биохимия
- #
- #
Источник
В клетках организма всегда существует потребность в глюкозе:
- для эритроцитов глюкоза является единственным источником энергии,
- нервная ткань потребляет около 120 г глюкозы в сутки и эта величина практически не зависит от интенсивности ее работы. Только в экстремальных ситуациях (длительное голодание) она способна получать энергию из неуглеводных источников (кетоновые тела),
- глюкоза играет весомую роль для поддержания необходимых концентраций метаболитов цикла трикарбоновых кислот (в первую очередь оксалоацетата).
Таким образом, при определенных ситуациях – при низком содержании углеводов в пище, голодании, длительной физической работе, т.е. когда глюкоза крови расходуется и наступает гипогликемия, организм должен иметь возможность синтезировать глюкозу и нормализовать ее концентрацию в крови. Это достигается реакциями глюконеогенеза, идущими в печени.
По определению, глюконеогенез – это синтез глюкозы из неуглеводных компонентов: лактата, пирувата, глицерола, кетокислот цикла Кребса и других кетокислот, из аминокислот.
Необходимость глюконеогенеза и его значение для организма демонстрируют два цикла – глюкозо-лактатный и глюкозо-аланиновый.
Глюкозо-лактатный цикл (цикл Кори)
Глюкозо-лактатный цикл – это циклический процесс, объединяющий реакции глюконеогенеза и реакции анаэробного гликолиза. Глюконеогенез происходит в печени, субстратом для синтеза глюкозы является лактат, поступающий в основном из эритроцитов или мышечной ткани.
В эритроцитах молочная кислота образуется непрерывно, так как для них анаэробный гликолиз является единственным способом образования энергии.
В скелетных мышцах высокое накопление молочной кислоты (лактата) является следствием гликолиза при очень интенсивной, субмаксимальной мощности, работе, при этом внутриклеточный рН снижается до 6,3-6,5. Но даже при работе низкой и средней интенсивности в скелетной мышце всегда образуется некоторое количество лактата.
Убрать молочную кислоту можно только одним способом – превратить ее в пировиноградную кислоту. Однако сама мышечная клетка ни при работе, ни во время отдыха не способна превратить лактат в пируват из-за особенностей изофермента лактатдегидрогеназы-5. Зато клеточная мембрана высоко проницаема для лактата и он движется по градиенту концентрации наружу. Поэтому во время и после нагрузки (при восстановлении) лактат легко удаляется из мышцы. Это происходит довольно быстро, всего через 0,5-1,5 часа в мышце лактата уже нет. Малая часть молочной кислоты выводится с мочой.
Большая часть лактата крови захватывается гепатоцитами, окисляется в пировиноградную кислоту и вступает на путь глюконеогенеза. Глюкоза, образованная в печени, используется самим гепатоцитом или возвращается обратно в мышцы, восстанавливая во время отдыха запасы гликогена. Также она может распределиться по другим органам.
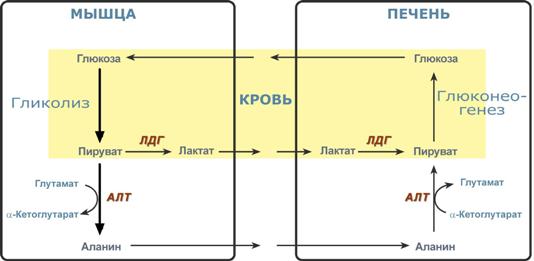
Глюкозо-лактатный (выделен желтым) и глюкозо-аланиновый циклы
Глюкозо-аланиновый цикл
Целью глюкозо-аланинового цикла также является уборка пирувата, но кроме этого решается еще одна немаловажная задача – доставкааминного азота из мышцы в печень.
При мышечной работе и в покое в миоците распадаются белки и образуемые аминокислоты трансаминируются с α-кетоглутаратом и полученный глутамат взаимодействует с пируватом. Образующийся аланин является транспортной формой аминного (аминокислотного) азота и пирувата из мышцы в печень. В гепатоците идет обратная реакция трансаминирования, аминогруппа через глутамат передается на синтез мочевины, пируват используется для синтеза глюкозы.
Кроме мышечной работы, глюкозо-аланиновый цикл активируется во время голодания, когда белки мышц и других тканей распадаются и многие аминокислоты используются в качестве источника энергии, а их азот необходимо доставить в печень.
Источник
Цикл
Кори (глюкозо-лактатный цикл) открыла
чешская ученая, лауреат Нобелевской
премии Тереза
Кори.
Он представляет собой биохимический
транспорт лактата
из мышц в печень и дальнейший синтез
глюкозы
из лактата, катализируемый ферментами
глюконеогенеза:
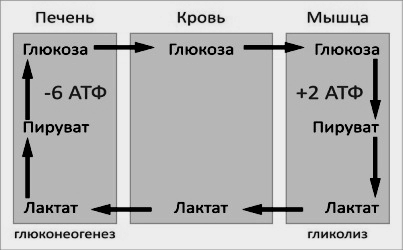
При
интенсивной мышечной работе и в условиях
отсутствия или недостаточного числа
митохондрий
(например, в эритроцитах)
глюкоза
подвергается анаэробному гликолизу
с образованием лактата.
При накоплении лактата в мышцах возникает
лактат-ацидоз, раздражаются чувствительные
нервные окончания, что вызывает боль в
мышцах.
Лактат
переносится кровью в печень и превращается
в пируват, а затем в глюкозу (глюконеогенез),
которая с током крови может возвращаться
в работающую мышцу.
Направление
лактатдегидрогеназной реакции в
работающих мышцах и печени обусловлено
отношением концентраций восстановленной
и окисленной форм НАД+:
отношение НАД+/НАДН
в сокращающейся мышце больше, чем в
печени.
7.7. Спиртовое брожение
Спиртовое брожение
осуществляется дрожжеподобными
организмами, а также некоторыми плесневыми
грибками:
Механизм
реакции близок к гликолизу. Расхождение
начинается после этапа образования
пирувата. При гликолизе пируват при
участии фермента ЛДГ и кофермента НАДН
восстанавливается в лактат. При спиртовом
брожении пируват подвергается
декарбоксилированию, в результате
образуется ацетальдегид, а затем при
восстановлении его – этанол:
При молочнокислом
брожении ПВК не декарбоксилируется, а,
как и при гликолизе в животных тканях,
восстанавливается при участии ЛДГ за
счет водорода НАДН.
7.8. Пентозофосфатный путь превращения глюкозы
Пентозофосфатный
путь –
альтернативный путь окисления глюкозы.
Его функции:
–
поставляет клеткам кофермент НАДФН,
использующийся как донор водорода в
реакциях восстановления;
–
обеспечивает клетки пентозофосфатами
для синтеза нуклеотидов и нуклеиновых
кислот.
Пентозофосфатный
путь не приводит к синтезу АТФ.
Ферменты пути
локализованы в цитозоле.
В
пентозофосфатном пути превращения
глюкозы выделяют окислительный и
неокислительный пути образования
пентоз.
Окислительный
путь включает
две реакции дегидрирования. Коферментом
дегидрогеназ является НАДФ+,
восстанавливающийся в НАДФН. Пентозы
образуются при окислительном
декарбоксилировании.
Неокислительный
путь включает
реакции переноса 2- и 3-х углеродный
фрагментов с одной молекулы на другую.
Этот путь служит для синтеза пентоз.
Процесс обратим, и из пентоз могут
образовываться гексозы.
Пентозофосфатный
путь образования пентоз протекает в
печени, жировой ткани, молочной железе,
коре надпочечников, эритроцитах.
1).
Дегидрирование глюкозо-6-фосфата при
участии глюкозо-6-фос-фатдегидрогеназы
и кофермента НАДФ+
с образованием 6-фосфоглюконо--лактона
и НАДФН:
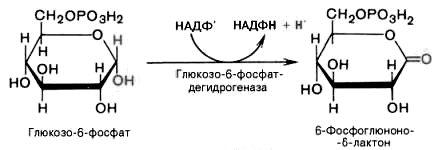
2).
6-фосфоглюконо--лактон
нестабилен и гидролизуется с образованием
6-фосфоглюконата (фермент –
6-фосфоглюконолактоназа):
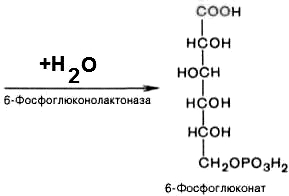
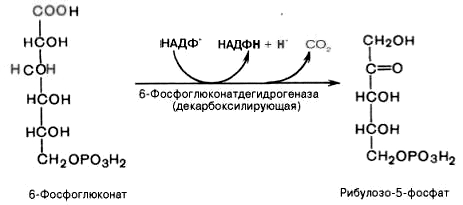
3).
Дегидрирование и декарбоксилирование
6-фосфоглюконата с образованием
рибулозо-5-фосфата (пентоза) и НАДФН при
участии декарбоксилирующей
6-фосфоглюконатдегидрогеназы:
4).
Под действием эпимеразы из рибулозо-5-фосфата
образуется ксилулозо-5-фосфат (пентоза).
Под влиянием изомеразы рибулозо-5-фосфат
превращается в рибозо-5-фосфат (пентоза).
Между формами пентозофосфатов
устанавливается равновесие:
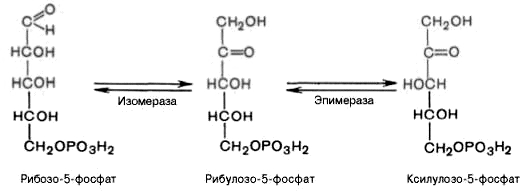
На
этом этапе пентозофосфатный путь может
быть завершен. При других условиях
наступает неокислительная стадия
пентозофосфатного цикла, протекающая
в анаэробных условиях. Она заключается
в переносе двух- и трехуглеродных
фрагментов от одной молекулы к другой.
При этом образуются вещества, характерные
для гликолиза (фруктозо-6-фосфат,
фруктозо-1,6-бисфосфат, фосфотриозы), и
вещества, специфические для пентозофосфатного
пути (седогептулозо-7-фосфат,
пентозо-5-фосфаты, эритрозо-4-фосфат).
Шесть
молекул
глюкозо-6-фосфата в пентозофосфатном
цикле
образуют 6 молекул
рибулозо-5-фосфата и 6 молекул
СО2.
Из 6 молекул
рибулозо-5-фосфата регенерируется 5
молекул
глюкозо-6-фосфата:
Промежуточные
продукты цикла (фруктозо-6-фосфат и
глицеральдегид-3-фосфат) включаются в
гликолиз.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Глюконеогенез – синтез глюкозы из неуглеводных продуктов de novo. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Протекает в основном в печени и менее интенс. в корковом в-ве почек, в слиз. об-ке кишеч.Большинство р-ций глюконеогенеза протекает за счёт обратимых р-ций гликолиза и катализируется теми же ферментами. Однако 3 реакции необратимы. На этих стадиях р-ции глюконеогенеза протекают другими путями.
ПВК включ. в глюконеогенез, а образ-я глюкоза поступает в кровь и поглощ. скелет. м-цами – “глюкозо-лактатным циклом”, или “циклом Кори”, –обесп. утилизацию лактата; предотвращает его накопление- опасное снижение рН (лактоацидоз). Часть ПВК, обр. из лактата, окисляется печенью. Энергия ок. может исп. для синтеза АТФ, необхо. для р-ций глюконеогенеза. Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Аланин из мышц переносится кровью в печень, где преобразуется в ПВК, который частич. окисляется и частично включ. в глюкозонеогенез.
99.Глюконеогенез.см.выше и в метаболизме*
100-102. Аэробное окисление глюкозы(см.85).
103-104. Челночные механизмы транспорта.
*малат-аспартатный челнок. Перенос водорода из цитозоля НАДН в митохондрии происходит при участии специальных механизмов, называющихся челночными. Суть этих механизмов сводится к тому, что НАДН в цитозоле восстанавливает некоторое соединение, способное проникать в митохондрию; в митохондрии это соединение окисляется, восстанавливая внутримитохондриальный НАД+, и вновь переходит в цитозоль. Самая активная малат-аспартатная система, действующая в митохондриях печени, почек и сердца. На каждую пару электронов цитозольной НАДН, переданную на кислород по этой системе, образуется 3 молекулы АТФ.
В скелетных мышцах и мозге перенос восстановительных эквивалентов от цитозольной НАДН осуществляет глицеролфосфатная система. При этом восстановительные эквиваленты передаются в цепь переноса электронов через комплекс II, и поэтому синтезируется только 2 молекулы АТФ.
Глицеро-фосфатный челнок:
105. Роль инсулина и глюкагона в регуляции энергетического метаболизма при нормальном питании и при голодании.Инсулин и глюкагон играют главную роль в регуляции метаболизма при смене абсорбтивного и постабсорбтивного периодов и при голодании.Абсорбтивный период: Увеличение отношения инсулин/глюкагон вызывает ускорение использования метаболитов для запасания энергоносителей: происходит синтез гликогена, жиров и белков. Режим запасания включается после приёма пищи и сменяется режимом мобилизации запасов после завершения пищеварения.
Голодание: В отсутствие пищи в крови снижается уровень глюкозы, ам-к и ТАГ. инсулинглюкагоновый индекс снижается, и повышается концентрация контринсулярных гормонов, в первую очередь кортизола. Сущ.2 наиболее встречающиеся формы нарушения переваривания дисахари-дов в кишечнике – дефект лактазы(β-гликози-дазного комплекса) и сахаразы (сахаразо-изомальтазного комплекса непереноси-мостьлактозы и сахарозы. Отсутствие гидролиза соответствующих дисахаридов приводит к осмотическому эффекту и задержке воды в просвете кишечника.
Кроме этого, сахара активно потребляются микрофлорой толстого кишечника и метаболизируют с образованием органических кислот (масляная, молочная) и газов. Из-за этого симптомами лактазной или сахаразной недостаточности являются диарея, срыгивания, метеоризм, вспучивание живота, его спазмы и боли, атопический дерматит.
Сахарный диабет – заболевание, возникающее вследствие абсолютного или относительного дефицита инсулина. При сахарном диабете, как правило, соотношение инсулин/глюкагон снижено. При этом ослабевает стимуляция процессов депонирования гликогена и жиров, и усиливается мобилизация запасов энергоносителей. Печень, мышцы и жировая ткань даже после приёма пищи функционируют в режиме постабсорбтивного состояния.
Источник
Цикл
Кори (глюкозо-лактатный цикл) открыла
чешская ученая, лауреат Нобелевской
премии Тереза
Кори.
Он представляет собой биохимический
транспорт лактата
из мышц в печень и дальнейший синтез
глюкозы
из лактата, катализируемый ферментами
глюконеогенеза:
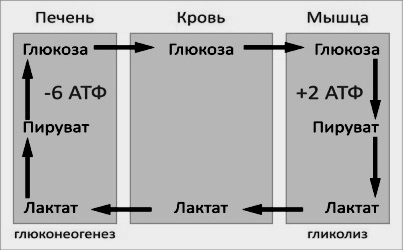
При
интенсивной мышечной работе и в условиях
отсутствия или недостаточного числа
митохондрий
(например, в эритроцитах)
глюкоза
подвергается анаэробному гликолизу
с образованием лактата.
При накоплении лактата в мышцах возникает
лактат-ацидоз, раздражаются чувствительные
нервные окончания, что вызывает боль в
мышцах.
Лактат
переносится кровью в печень и превращается
в пируват, а затем в глюкозу (глюконеогенез),
которая с током крови может возвращаться
в работающую мышцу.
Направление
лактатдегидрогеназной реакции в
работающих мышцах и печени обусловлено
отношением концентраций восстановленной
и окисленной форм НАД+:
отношение НАД+/НАДН
в сокращающейся мышце больше, чем в
печени.
7.7. Спиртовое брожение
Спиртовое
брожение осуществляется дрожжеподобными
организмами, а также некоторыми плесневыми
грибками:
Механизм
реакции близок к гликолизу. Расхождение
начинается после этапа образования
пирувата. При гликолизе пируват при
участии фермента ЛДГ и кофермента НАДН
восстанавливается в лактат. При спиртовом
брожении пируват подвергается
декарбоксилированию, в результате
образуется ацетальдегид, а затем при
восстановлении его – этанол:
При
молочнокислом брожении ПВК не
декарбоксилируется, а, как и при гликолизе
в животных тканях, восстанавливается
при участии ЛДГ за счет водорода НАДН.
7.8. Пентозофосфатный путь превращения глюкозы
Пентозофосфатный
путь –
альтернативный путь окисления глюкозы.
Его функции:
–
поставляет клеткам кофермент НАДФН,
использующийся как донор водорода в
реакциях восстановления;
–
обеспечивает клетки пентозофосфатами
для синтеза нуклеотидов и нуклеиновых
кислот.
Пентозофосфатный
путь не приводит к синтезу АТФ.
Ферменты пути
локализованы в цитозоле.
В
пентозофосфатном пути превращения
глюкозы выделяют окислительный и
неокислительный пути образования
пентоз.
Окислительный
путь включает
две реакции дегидрирования. Коферментом
дегидрогеназ является НАДФ+,
восстанавливающийся в НАДФН. Пентозы
образуются при окислительном
декарбоксилировании.
Неокислительный
путь включает
реакции переноса 2- и 3-х углеродный
фрагментов с одной молекулы на другую.
Этот путь служит для синтеза пентоз.
Процесс обратим, и из пентоз могут
образовываться гексозы.
Пентозофосфатный
путь образования пентоз протекает в
печени, жировой ткани, молочной железе,
коре надпочечников, эритроцитах.
1).
Дегидрирование глюкозо-6-фосфата при
участии глюкозо-6-фос-фатдегидрогеназы
и кофермента НАДФ+
с образованием 6-фосфоглюконо--лактона
и НАДФН:
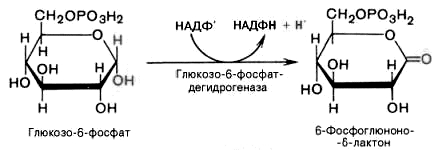
2).
6-фосфоглюконо--лактон
нестабилен и гидролизуется с образованием
6-фосфоглюконата (фермент –
6-фосфоглюконолактоназа):
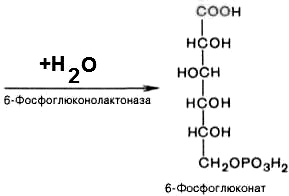
3).
Дегидрирование и декарбоксилирование
6-фосфоглюконата с образованием
рибулозо-5-фосфата (пентоза) и НАДФН при
участии декарбоксилирующей
6-фосфоглюконатдегидрогеназы:
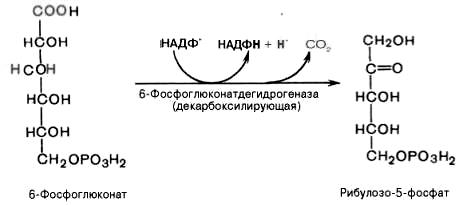
4).
Под действием эпимеразы из рибулозо-5-фосфата
образуется ксилулозо-5-фосфат (пентоза).
Под влиянием изомеразы рибулозо-5-фосфат
превращается в рибозо-5-фосфат (пентоза).
Между формами пентозофосфатов
устанавливается равновесие:
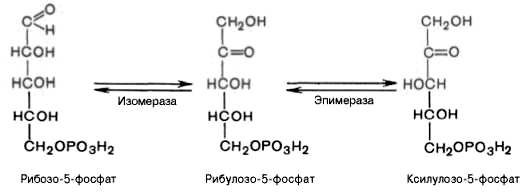
На
этом этапе пентозофосфатный путь может
быть завершен. При других условиях
наступает неокислительная стадия
пентозофосфатного цикла, протекающая
в анаэробных условиях. Она заключается
в переносе двух- и трехуглеродных
фрагментов от одной молекулы к другой.
При этом образуются вещества, характерные
для гликолиза (фруктозо-6-фосфат,
фруктозо-1,6-бисфосфат, фосфотриозы), и
вещества, специфические для пентозофосфатного
пути (седогептулозо-7-фосфат,
пентозо-5-фосфаты, эритрозо-4-фосфат).
Шесть
молекул
глюкозо-6-фосфата в пентозофосфатном
цикле
образуют 6 молекул
рибулозо-5-фосфата и 6 молекул
СО2.
Из 6 молекул
рибулозо-5-фосфата регенерируется 5
молекул
глюкозо-6-фосфата:
Промежуточные
продукты цикла (фруктозо-6-фосфат и
глицеральдегид-3-фосфат) включаются в
гликолиз.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
