Что такое диверсионный колит
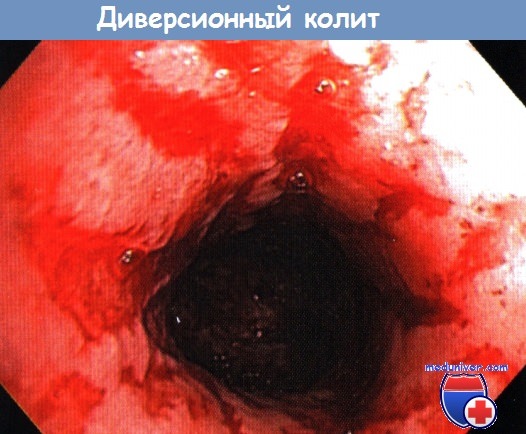
Диверсионный колит – причины, признаки, лечениеДиверсионный колит – обратимые морфологические (и симптоматические) изменения в толстой кишке, развивающиеся при отсутствии нутриентов в отключенной кишке в результате формирования проксимальной стомы. Типичные причины: состояние после отключающей илеостомии/колостомии, операции Гартмана. Патогенез диверсионного колита: а) Эпидемиология. В определенной степени диверсионный колит присутствует во всех случаях отключения толстой кишки (100% заболеваемость), но только у небольшой части пациентов носит симптоматический характер. б) Симптомы диверсионного колита: ректальные кровотечения, слизистое или слизисто-гнойное отделяемое, иногда колики. в) Дифференциальный диагноз: г) Патоморфология: д) Обследование при диверсионном колите Дополнительные исследования (необязательные):
е) Классификация: ж) Лечение без операции диверсионного колита: з) Операция при диверсионном колите Хирургический подход: и) Результаты лечения диверсионного колита. В целом доброкачественное течение. к) Наблюдение и дальнейшее лечение: – Вернуться в оглавление раздела “Хирургия” Оглавление темы “Болезни толстой кишки”:
|
Источник
Полный текст статьи:
Эпидемиология. Распространенность диверсионного колита у стомированных пациентов чрезвычайно высока и составляет 74–91% [1, 3, 9]. Считается, что у пациентов с предшествующим хроническим воспалительным заболеванием кишечника (ХВЗК) частота развития диверсионного колита выше, но, согласно результатам исследования Son и соавторов о диверсионном колите у пациентов, оперированных по поводу рака прямой кишки, частота развития составила 100% [7, 8]. Связи между диверсионным колитом, возрастом, полом, типом стомы или способом выполненного оперативного вмешательства нет [3, 9].
Патогенез. Основные механизмы, лежащие в основе диверсионного колита, по-прежнему до конца не ясны. Главное звено в патогенезе этого заболевания — бактериальный дисбаланс, развивающийся вследствие нарушения нормального пассажа кала, который приводит к нарушению защитной функции слизистой оболочки и снижению количества короткоцепочечных жирных кислот (КЦЖК). КЦЖК участвуют в метаболизме колоноцитов, покрывая около 70% их энергетических потребностей, и недостаток этих кислот приводит к нарушению энергетического обмена в эпителии толстой кишки [1]. С другой стороны, КЦЖК расслабляют гладкие мышцы сосудов — и их дефицит может вызывать повышение тонуса сосудов, что приводит к относительной ишемии слизистой и стенки толстой кишки (ишемическая теория) [9]. Основные теории патогенеза диверсионного колита представлены на рис. 1.
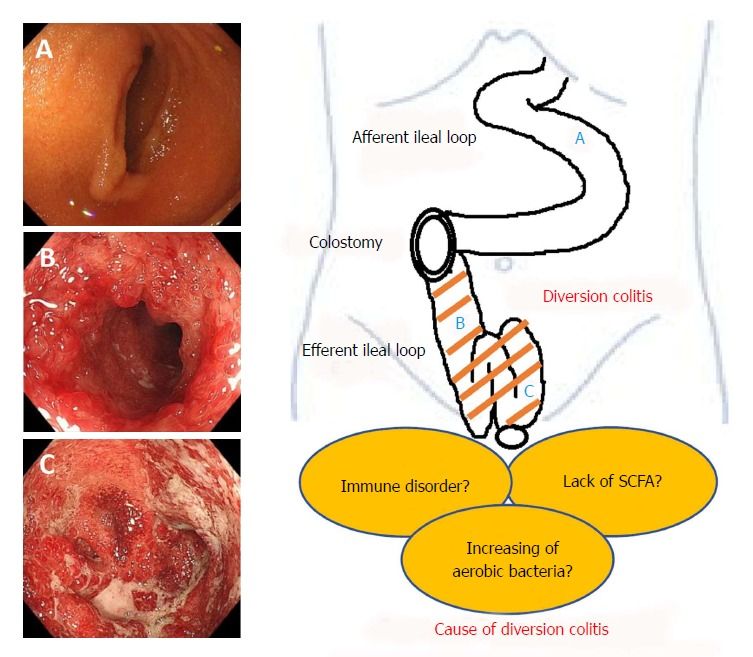
Рис. 1. Основные теории патогенеза диверсионного колита [9].
Клиническая картина. Клинические проявления возникают примерно у 30% больных без ХВЗК, но у пациентов с болезнью Крона встречаются в 33% случаев, а при язвенном колите — 87%.[Оэ2] Симптомы диверсионного колита возникают в течение 1–36 месяцев после наложения колостомы [3, 9]. Пациенты с диверсионным колитом жалуются на выделение слизи и/или крови, тенезмы, боли в животе, чувство тяжести или боль в прямой кишке [1, 7]. Патологические выделения из прямой кишки — наиболее распространенный симптом (40%), на втором месте по встречаемости — боли в животе и тенезмы (15%) [9]. Наиболее информативный в этом случае диагностический метод — ректороманоскопия и колоноскопия с гистологическим исследованием биоптата слизистой и удаленных операционных препаратов из отключенных отделов ободочной и прямой кишки [1].
Эндоскопическая картина. Макроскопические изменения в отключенной толстой кишке могут носить как непрерывный, так и сегментарный характер [9]. Диверсионный колит представлен отеком, зернистостью, петехиальными кровоизлияниями, контактной кровоточивостью слизистой, смазанностью сосудистого рисунка и напоминает эндоскопическую картину язвенного колита с умеренной степенью активности [1].
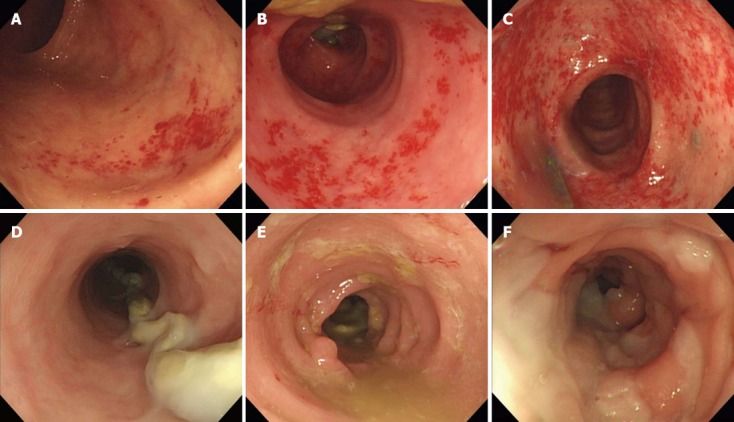
Пристеночно отмечаются налеты слизи. Son с соавторами в своей работе оценивали по эндоскопической картине в отдельности выраженность отека (0–3 балла), внутрислизистых кровоизлияний (0–3 балла) и контактную кровоточивость (0–1 балл). Впоследствии баллы суммировались (0–7 баллов). По общему баллу диверсионный колит был разделен на слабый (0–2 балла), умеренный (3–5 баллов) и тяжелый (6–7 баллов) (рис. 2) [8].
Рисунок 2. Эндоскопические проявления диверсионного колита [8].
Пример основных эндоскопических результатов при диверсионном колите в зависимости от относительной тяжести.
A, B, C. Петехиальные кровоизлияния (A — 1 балл; B — 2 балла; C — 3 балла).
D, E, F. Отек (D — 1 балл; E — 2 балла; F — 3 балла).
Подготовка к колоноскопии пациентов, перенесших операцию на толстой кишке. Мною найдено небольшое количество ресурсов, посвященных проблеме подготовки данной группы пациентов. В отечественной литературе эта проблема освещена крайне скудно.
Пациентам с разгрузочными илеостомами прием пероральных препаратов для очистки кишечника не показан. Таким больным проводят промывание толстой кишки через илеостому, которое может быть дополнено очистительными клизмами, это обычно требует госпитализации в хирургическое отделение [12]. На сайте gnck.ru уточняется, что специальная подготовка пациентам с разгрузочной илеостомой не показана [13]. Однако в нашей практике мы довольно часто наблюдаем неадекватную подготовку толстой кишки к исследованию даже после проведения очистительных клизм. Для пациентов с петлевой колостомой рекомендуется проведение стандартной подготовки пероральными препаратами для очистки кишечника в комбинации с промыванием отключенных отделов через колостому. Пациенты с концевыми колостомами (после операций типа Гартмана) должны проходить стандартную подготовку пероральными препаратами для очистки кишечника в комбинации с очистительными клизмами. Пациентам после субтотальной резекции рекомендована одноэтапная быстрая подготовка с последующей очистительной клизмой — как для сигмоскопии. Нестомированным пациентам после различных вариантов резекции толстой и прямой кишки и брюшно-анальной резекции показана стандартная пероральная подготовка [12].
На сегодняшний день стандартной считается двухэтапная подготовка или одноэтапная в день исследования полным объемом полиэтиленгликоля. Исследование Liu и соавторов показало, что уменьшение стандартного объема ПЭГ с 4 л до 2 л в сплит-режиме у пациентов с оперированной толстой кишкой приводит к снижению качества подготовки (89,4% против 66,7%, P < 0,001) [6].
Действенная альтернатива полнообъемным препаратам ПЭГ — применение малообъемного препарата ПЭГ с аскорбатным комплексом («МОВИПРЕП®»). Применение препарата «МОВИПРЕП®» предпочтительнее для амбулаторных пациентов, сопряжено с меньшим количеством таких нежелательных явлений, как тошнота и рвота, а также с большей приверженностью пациентов [2, 4, 5, 10, 11]. В проведенном многоцентровом рандомизированном клиническим исследовании в России по оценке подготовки пациентов по утренней и двухэтапной схеме применения препарата МОВИПРЕП®, показано, что обоих схемах наблюдается почти в 100% случаях эффективная подготовка кишечника, включая правые отделы [14].
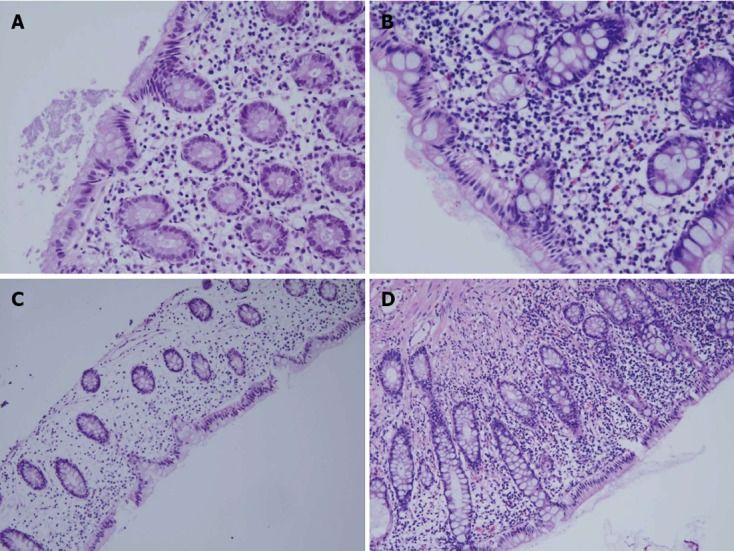
Гистологическая картина. Гистологические изменения в отключенной кишке присутствуют у всех стомированных пациентов [1, 8, 9]. В биоптатах слизистой при диверсионном колите выявляются признаки острого или хронического воспаления, эозинофильная инфильтрация, нарушение архитектоники крипт, фолликулярная лимфоидная гиперплазия и крипта-абсцессы [1, 8, 9]. Son и соавторы [8] также использовали шкалу оценки тяжести диверсионного колита, оценивая эти признаки по отдельности: острое воспаление (0–1 балл); хроническое воспаление (0–2 балла); эозинофильная инфильтрация (0–2 балла); нарушение архитектоники крипт (0–1 балл); фолликулярная гиперплазия (0–1 балл); крипта-абсцессы (0–1 балл) — с возможной суммой общего балла от 0 до 8. По общему баллу диверсионный колит был разделен на слабый (1–3 балла), умеренный (4–6 баллов) и тяжелый (7–8 баллов) (см. рис. 3).
Рисунок 3. Гистологическая картина диверсионного колита [8].
Пример основных гистологических результатов при диверсионном колите в зависимости от относительной тяжести.
А, B. Эозинофильная инфильтрация (A — 1 балл; B — 2 балла; окраска гематоксилином и эозином, увеличение 400x).
C, D. Хроническое воспаление с мононуклеарными макрофагами, лимфоцитами и плазматическими клетками (C — 1 балл; D — 2 балла; окраска гематоксилином и эозином, увеличение 200x).
Лечение. Цель лечения — уменьшение или устранение симптомов [3, 9]. Ликвидация коло- либо илеостомы приводит к излечению, однако Son с соавторами указывают, что у пациентов с тяжелым диверсионным колитом после ликвидации стомы может возникнуть диарея [8]. Фармакологические методы лечения необходимы для симптомных пациентов с постоянными стомами и пациентов, у которых ликвидация стомы не может быть проведена по причинам технических трудностей, плохой функции анального сфинктера или стойкого перианального сепсиса. На сегодняшний день не существует единых подходов к терапии диверсионного колита у таких пациентов. Используются препараты КЦЖК, 5-аминосалициловой кислоты, клизмы с кортикостероидами или волокнами [1, 3, 9]. Существуют единичные сообщения о применении фекотрансплантации [9] и спрея декстрозы [7, 9].
Выводы
Диверсионный колит – неспецифическое воспаление, возникающее в отключенной кишке после наложения стомы. Данное состояние развивается у всех стомированных пациентов, но при этом симптомы (выделение слизи и/или крови, тенезмы, боли в животе, чувство тяжести или боль в прямой кишке) возникают только у 30% человек. Диагностика диверсионного колита основана на данных колоноскопии с гистологическим исследованием биоптата. Эндоскопические признаки диверсионного колита: отек, зернистость, петехиальные кровоизлияния, контактная кровоточивость слизистой, смазанность сосудистого рисунка. Гистологическая картина представлена признаками острого или хронического воспаления, эозинофильной инфильтрацией, нарушением архитектоники крипт, фолликулярной лимфоидной гиперплазией и крипта-абсцессами. Основной метод лечения диверсионного колита – ликвидация стомы. Единых подходов к медикаментозному лечению на сегодняшний день нет.
[Оэ2] ХВЗК представлены болезнью Крона и язвенным колитом. У пациентов с данными заболеваниями клинические проявления бывают чаще, чем у пациентов с другой патологией.
Источник
Гришаев А.В., врач-эндоскопист ОГБУЗ «Клиническая больница скорой медицинской помощи»,
Пасынкова Т.А. врач-эндоскопист, поликлиника №4.
г. Смоленск
При выключении из пассажа толстой кишки или ее части, в отключенных отделах развиваются воспалительные изменения. При формировании временной илео- или колостомы, ее ликвидация и проведение реконструктивно-восстановительной операции происходят в сроки, как правило, не менее чем через 6-8 месяцев. Отключенные отделы кишечника после формирования стомы не участвуют в пищеварении и находятся в «нефизиологическом состоянии», отмечается наличие процессов приводящих к воспалительным изменениям в стенке кишки. Впервые подобное состояние описано B.C. Morson в 1972г. В 1981 году D.J. Glotzer ввел термин «diversion colitis» или «колит отключенной кишки» (КОК). У пациентов, перенесших операции отключения каловой струи и ранее не имевших ни клинических, ни морфологических признаков воспалительных заболеваний толстой кишки, в отключенной ее части были выявлены выраженные воспалительные изменения. Частота выявления воспалительных изменений в отключенных отделах по данным разных авторов, колеблется от 71% до 100%. Существует прямая зависимость между сроками отключения и выраженностью воспалительных изменений. Воспалительные изменения развиваются в сроки до 3 месяцев после формирования стомы в 47%, до 6 месяцев – 73%, после 7 мес – в 100% случев (по данным Г.М. Китчиева, С.И. Ачкасов с соавт.).
Проявления неспецифичны, выраженность их напрямую зависит от срока отключения, характера основного заболевания и тяжести его осложнений. Отмечается качественное и количественное изменение микрофлоры, нарушение процессов обмена в слизистой оболочке, нарушение продукции слизи и изменение ее состава. Защитные возможности слизистой снижаются, концентрация повреждающих агентов увеличивается. Колоноциты подвергаются воздействию протеолитических ферментов, антигенов, эндогенных токсинов на фоне снижения трофики тканей, активизируются процессы апоптоза колоноцитов и тормозится их пролиферация и дифференцировка. Совокупность этих воздействий приводит к активному проникновению антигенов, токсинов, микроорганизмов через слой колоноцитов в собственную пластинку слизистой, подслизистую основу и сосудистое русло, запуская каскад воспалительных реакций, которые выражаются в отеке, перестройке сосудистого русла, ранимости и кровоточивости слизистой. Совокупность этих воспалительных изменений составляет понятие «колит отключенной кишки» (диверсионный колит).
Нами обследовано 35 пациентов (19 мужчин и 16 женщин в возрасте 39 до 75 лет). У всех пациентов диагностический алгоритм включал выполнение эндоскопического осмотра видеоколоноскопом высокого разрешения с забором биопсийного материала для патоморфологической оценки. Использовалась эндоскопическая видеосистема «Pentax» EС 3890Li, EPKi 5000. Выполнена оценка морфофункционального состояния слизистой оболочки прямой кишки у больных со стомой в условиях стационара и поликлиники.
По степени выраженности эндоскопических проявлений пациенты выделены 4 группы: с отсутствием явлений воспаления, минимальными, умеренными и значительной выраженности воспалительных проявлений. У пациентов при визуальной оценке выявлены признаки проктита у 29 человек, 6 – без визуальных проявлений. У 29 пациентов с признаками проктита выделено три степени выраженности КОК, минимальная – 9 (срок отключения до 4 месяцев), умеренная – 15 (срок отключения до 6-9 месяцев), ярко выраженная – 5 (9-12 мес.). Отсутствие явлений воспаления (6 пациентов) – слизистая розовая, блестящая, количество слизи незначительное, стенки расправляются без особых усилий инсуфляцией воздуха, сосудистый рисунок сохранен. Минимально выраженный проктит (9 пациентов) – слизистая розовая с единичными петехиями, участки гиперемии, тонус несколько снижен, складки местами сглажены, легко расправляются при инсуфляции воздуха, сосудистый рисунок местами смазан, в просвете присутствует небольшое количество слизи, контакная ранимость не возникает. Умерено выраженный колит (15 пациентов) – тонус снижен, в просвете достаточное количество слизи, затрудняющей осмотр, слизистая бледного вида, умеренно атрофичная, на фоне розового оттенка отмечается умеренная гиперемия, отек, зернистость, сосудистый рисунок смазан, складки сглажены, местами – мелкоточечные геморрагии, контактная кровоточивость присутствует, но мало выражена. Значительно выраженные воспалительные изменения (5 пацинтов) – тонус кишечной стенки снижен, складки сглажены, выраженная гиперемия, воспалительная инфильтрация слизистой, отек, значительная контактная кровоточивость, нередко болезненность при исследовании, культя зачастую спазмирована, при контакте эндоскопа со стенкой образовываются множественные геморрагии, местами сливающиеся, в просвете больное количество грязно-серой слизи.
По результатам морфологического исследования биоптатов отмечались структурные изменения слизистой оболочки различной степени выраженности: полнокровие капилляров, отек и слизистой, гиперплазия бокаловидных клеток, деформация крипт, склероз, атрофия подслизистой основы, лимфоплазмоцитарная инфильтрация собственной пластинки слизистой.
Клинические проявления отмечаемые пациентами: ложные позывы на дефекацию,
дискомфорт и чувство тяжести в промежности и прямой кишки, патологические выделения из отключенных отделов толстой кишки (слизистые у ~2/3 и слизисто-геморрагические ~1/3). Усиление частоты и выраженности симптомов увеличивается по мере увеличения сроков отключения толстой кишки из естественного пассажа.
Эндоскопические признаки диверсионного колита определяются практически у всех пациентов с кишечной стомой после выключения естественного пассажа кишечного содержимого. Симптоматика должна интерпретироваться врачами как проявления самостоятельного воспалительного заболевания. Выраженность воспалительных изменений при диверсионном колите, удлинение фазы заживления раны и замедление процессов образования рубца, может быть неблагоприятным фактором при проведении реконструктивно-восстановительных операций, что в свою очередь сопряжено с риском осложнений, формирование межкишечного анастомоза между сегментами с имеющимися явлениями активного воспаления увеличивает вероятность расхождения кишечных швов.Выполнение эндоскопического исследования позволяет выявлять патологические изменения у стомированных пациентов, оценить возможность выполнения лечебных мероприятий,позволяет определить дальнейшую тактику лечения, прогнозировать вероятность осложненийв реконструктивно-восстановительномпериоде.

Источник
